第10页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
14. 眼镜是人们常用的护眼工具。如图是一款变色眼镜的示意图。
(变色眼镜示意图:标注①铜螺丝、②塑料脚套、③钛合金镜腿、④玻璃镜片)
(1)所标物质中属于金属单质的是______。
(2)该款变色眼镜的玻璃里加入了溴化银($AgBr$)和氧化铜。在强光照射下,溴化银分解成溴单质($Br_2$)和银,玻璃颜色变深,该反应的化学方程式为______;当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅,氧化铜在该反应中起______作用。
(变色眼镜示意图:标注①铜螺丝、②塑料脚套、③钛合金镜腿、④玻璃镜片)

(1)所标物质中属于金属单质的是______。
(2)该款变色眼镜的玻璃里加入了溴化银($AgBr$)和氧化铜。在强光照射下,溴化银分解成溴单质($Br_2$)和银,玻璃颜色变深,该反应的化学方程式为______;当光线变暗时,溴和银在氧化铜作用下,重新生成溴化银,玻璃颜色变浅,氧化铜在该反应中起______作用。
答案:
(1)①
(2)$2AgBr\xlongequal{强光}2Ag + Br_2$;催化
(1)①
(2)$2AgBr\xlongequal{强光}2Ag + Br_2$;催化
15. 科学课外活动中,老师为大家演示了如图①所示的趣味实验——“魔棒生烟”,该实验原理的微观示意图如图②所示。
(图①:两根玻璃棒分别蘸有浓盐酸和浓氨水,靠近产生白烟;图②:氨气分子+氯化氢分子→氯化铵分子微观示意图)
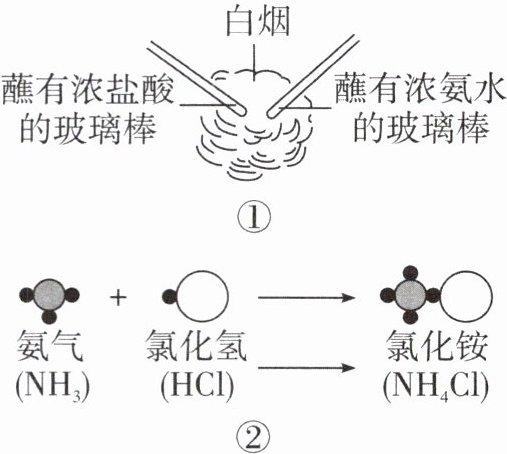
(1)图②反应属于基本反应类型中的______反应。
(2)小科根据实验原理,又设计了如图③所示的实验装置,用该装置与用玻璃棒做实验相比,明显的优点是______(写出一点即可)。
(图①:两根玻璃棒分别蘸有浓盐酸和浓氨水,靠近产生白烟;图②:氨气分子+氯化氢分子→氯化铵分子微观示意图)

(1)图②反应属于基本反应类型中的______反应。
(2)小科根据实验原理,又设计了如图③所示的实验装置,用该装置与用玻璃棒做实验相比,明显的优点是______(写出一点即可)。
答案:
(1)化合
(2)减少污染(或能更清晰地看到白烟产生的过程等)
(1)化合
(2)减少污染(或能更清晰地看到白烟产生的过程等)
16. 根据下列装置图,回答有关问题:
(装置图:A为固液混合常温型发生装置,B为向上排空气法收集装置,C为向下排空气法收集装置,D为排水法收集装置,E为洗气装置(盛浓硫酸) ,F为带可抽动铜丝的试管(内有$H_2O_2$溶液))
,F为带可抽动铜丝的试管(内有$H_2O_2$溶液))
(1)实验室用过氧化氢制取氧气的化学方程式为______,若要制取并收集一瓶干燥的氧气,应选用装置的连接顺序为______(填字母),检验氧气是否收集满的方法为______。
(2)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂。现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过______处理。改进后的发生装置如图F所示(已略去夹持装置)。
① 铜丝绕成螺旋状的作用是______(填字母)。
A. 收集到更多的$O_2$
B. 加快反应速率
C. 没有影响
② 与装置A比较,改进后装置的优点是______。
(装置图:A为固液混合常温型发生装置,B为向上排空气法收集装置,C为向下排空气法收集装置,D为排水法收集装置,E为洗气装置(盛浓硫酸)
 ,F为带可抽动铜丝的试管(内有$H_2O_2$溶液))
,F为带可抽动铜丝的试管(内有$H_2O_2$溶液))(1)实验室用过氧化氢制取氧气的化学方程式为______,若要制取并收集一瓶干燥的氧气,应选用装置的连接顺序为______(填字母),检验氧气是否收集满的方法为______。
(2)实验改进:查阅资料发现,氧化铜可以用作过氧化氢分解制氧气的催化剂。现有一根洁净的铜丝,实验前先将其绕成螺旋状,再经过______处理。改进后的发生装置如图F所示(已略去夹持装置)。
① 铜丝绕成螺旋状的作用是______(填字母)。
A. 收集到更多的$O_2$
B. 加快反应速率
C. 没有影响
② 与装置A比较,改进后装置的优点是______。
答案:
(1)$2H_{2}O_{2}\xlongequal {MnO_{2}}2H_{2}O+O_{2}\uparrow $;A→E→B;将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满。
(2)加热;①B;②可以控制反应的发生与停止。
(1)$2H_{2}O_{2}\xlongequal {MnO_{2}}2H_{2}O+O_{2}\uparrow $;A→E→B;将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满。
(2)加热;①B;②可以控制反应的发生与停止。
17. 在一定条件下,Mg和$MgH_2$的相互转化可以实现氢气的储存和释放,其工作原理如图所示。
(工作原理图:Mg与$H_2$在350℃、3 MPa下储存生成$MgH_2$,$MgH_2$在287℃、0.1 MPa下释放生成Mg和$H_2$)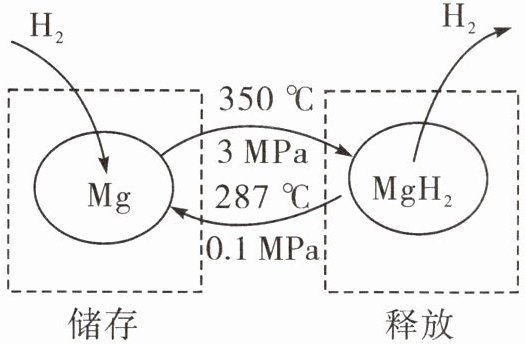
(1)① 氢气储存时发生反应的化学方程式为______。
② 氢气很容易逃逸,若氢气储存效率为10%,储存1 kg氢气,至少需要Mg的质量为______kg。
(2)① 氢气释放时发生反应的化学方程式为______。
② 理论上,52 kg $MgH_2$最多能释放氢气的质量为______kg。
(工作原理图:Mg与$H_2$在350℃、3 MPa下储存生成$MgH_2$,$MgH_2$在287℃、0.1 MPa下释放生成Mg和$H_2$)

(1)① 氢气储存时发生反应的化学方程式为______。
② 氢气很容易逃逸,若氢气储存效率为10%,储存1 kg氢气,至少需要Mg的质量为______kg。
(2)① 氢气释放时发生反应的化学方程式为______。
② 理论上,52 kg $MgH_2$最多能释放氢气的质量为______kg。
答案:
(1)①$Mg+H_2\xlongequal{350^{\circ}C、3MPa}MgH_2$;②12。
(2)①$MgH_2\xlongequal{287^{\circ}C、0.1MPa}Mg + H_2\uparrow$;②4。
(1)①$Mg+H_2\xlongequal{350^{\circ}C、3MPa}MgH_2$;②12。
(2)①$MgH_2\xlongequal{287^{\circ}C、0.1MPa}Mg + H_2\uparrow$;②4。
查看更多完整答案,请扫码查看


