2025年暑假作业明天出版社高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假作业明天出版社高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
1. 下列装置中,哪些能构成原电池? 其他不能构成原电池的原因是什么?
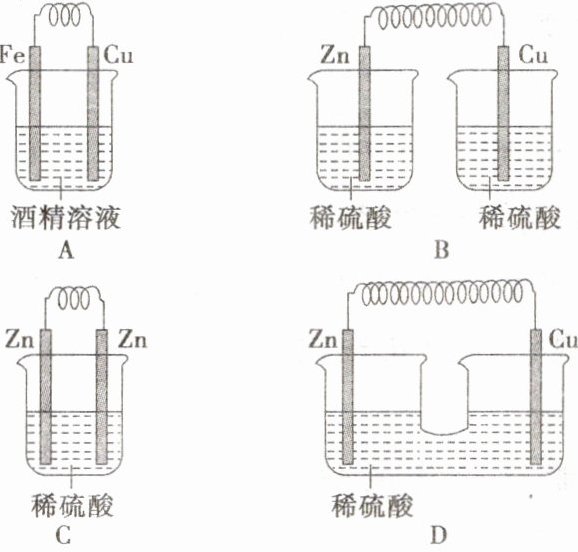

答案:
提示:装置D能构成原电池;装置A不能构成原电池,原因是酒精为非电解质;装置B不能构成原电池,原因是没有形成闭合回路;装置C不能构成原电池,原因是两个电极的金属活泼性相同。
2. 原电池工作时,电子和离子分别怎样移动?
答案:
提示:电子是从负极经过导线移向正极;在原电池电解质溶液中,阳离子移向正极,阴离子移向负极。
3. 相对于普通锌锰电池来讲,碱性锌锰电池有什么优点?
答案:
提示:碱性锌锰电池是将普通锌锰电池中的NH₄Cl换成湿的KOH,这样可延长电池的寿命和提高其性能。
4. 写出氢氧燃料电池反应的化学方程式,由此分析两极反应物分别是什么。
答案:
提示:在2H₂+O₂=2H₂O反应中,化合价变化H₂→H₂O,氢由0→+1,O₂→H₂O,氧由0→-2,H₂发生氧化反应,O₂发生还原反应,H₂为负极反应物,O₂为正极反应物。
例1 某学生用如图装置研究原电池原理,下列有关说法错误的是 (
A.图(3)中 Zn 片增重质量与 Cu 片减轻质量的比为$65:64$
B.图(2)中如果两极上都有气体产生,则说明 Zn 片不纯
C.图(1)中铜片上没有气体产生
D.图(2)与图(3)中正极生成物的质量之比为$1:32$时,Zn 片减轻的质量相等
A
)A.图(3)中 Zn 片增重质量与 Cu 片减轻质量的比为$65:64$
B.图(2)中如果两极上都有气体产生,则说明 Zn 片不纯
C.图(1)中铜片上没有气体产生
D.图(2)与图(3)中正极生成物的质量之比为$1:32$时,Zn 片减轻的质量相等
答案:
解析:图
(3)中Zn片作负极,发生氧化反应而溶解,质量减轻,Cu片作正极,Cu²⁺在此电极上发生还原反应析出Cu,质量增加,A错误;图
(2)中Zn作负极,铜作正极,溶液中的H⁺在铜电极上生成H₂,若Zn片不纯,会形成另一个原电池,Zn片表面也有气体生成,B正确;Cu与稀硫酸不反应,C正确;图
(2)与图
(3)中正极生成物分别是H₂和Cu,两者质量比为1:32时,物质的量之比n(H₂):n(Cu)=1:1,转移电子的物质的量也相等,消耗锌片的质量相等,D正确。答案:A
(3)中Zn片作负极,发生氧化反应而溶解,质量减轻,Cu片作正极,Cu²⁺在此电极上发生还原反应析出Cu,质量增加,A错误;图
(2)中Zn作负极,铜作正极,溶液中的H⁺在铜电极上生成H₂,若Zn片不纯,会形成另一个原电池,Zn片表面也有气体生成,B正确;Cu与稀硫酸不反应,C正确;图
(2)与图
(3)中正极生成物分别是H₂和Cu,两者质量比为1:32时,物质的量之比n(H₂):n(Cu)=1:1,转移电子的物质的量也相等,消耗锌片的质量相等,D正确。答案:A
例2 汽车的启动电源常用铅蓄电池,其放电时的原电池反应如下:$PbO_{2}+Pb+2H_{2}SO_{4}= 2PbSO_{4}+2H_{2}O$。根据此反应判断,下列叙述中正确的是 (
A.Pb 是正极
B.$PbO_{2}$得电子,被氧化
C.负极反应是$Pb+SO_{4}^{2-}-2e^{-}= PbSO_{4}$
D.电池放电时,溶液的酸性增强
C
)A.Pb 是正极
B.$PbO_{2}$得电子,被氧化
C.负极反应是$Pb+SO_{4}^{2-}-2e^{-}= PbSO_{4}$
D.电池放电时,溶液的酸性增强
答案:
解析:从铅蓄电池的放电反应可以看出:放电过程中Pb失去电子变为Pb²⁺,发生氧化反应,因而Pb是负极;PbO₂得到电子发生还原反应,被还原;反应过程中消耗了H₂SO₄,使溶液的酸性减弱。答案:C
例3 燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b 均为惰性电极。下列叙述不正确的是 (
A.a 极是负极,该电极上发生氧化反应
B.b 极反应是$O_{2}+4OH^{-}-4e^{-}= 2H_{2}O$
C.总反应的化学方程式为$2H_{2}+O_{2}= 2H_{2}O$
D.氢氧燃料电池是一种具有应用前景的绿色电源
B
)A.a 极是负极,该电极上发生氧化反应
B.b 极反应是$O_{2}+4OH^{-}-4e^{-}= 2H_{2}O$
C.总反应的化学方程式为$2H_{2}+O_{2}= 2H_{2}O$
D.氢氧燃料电池是一种具有应用前景的绿色电源
答案:
解析:a极通H₂为负极,电极反应式为2H₂+4OH⁻-4e⁻=4H₂O,发生氧化反应,A正确;b极通O₂为正极,电极反应式为O₂+2H₂O+4e⁻=4OH⁻,B不正确;正、负极电极反应式相加得总反应为2H₂+O₂=2H₂O,C正确;氢氧燃料电池的能量高,且产物为水,对环境无污染,故是具有应用前景的绿色电源,D正确。答案:B
1. 下图所示装置中,能够组成原电池的是 (
C
)
答案:
C
2. 下列有关电池的说法正确的是 (
A.铅蓄电池不属于二次电池
B.原电池工作时一定有氧化还原反应发生
C.废旧电池可埋入土壤,作为肥料
D.氢氧燃料电池,通入氢气的电极为电池的正极
B
)A.铅蓄电池不属于二次电池
B.原电池工作时一定有氧化还原反应发生
C.废旧电池可埋入土壤,作为肥料
D.氢氧燃料电池,通入氢气的电极为电池的正极
答案:
B 铅蓄电池不属于二次电池;原电池工作时一定有氧化还原反应发生;废旧电池可埋入土壤,作为肥料;氢氧燃料电池,通入氢气的电极为电池的正极。
查看更多完整答案,请扫码查看


