第63页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
13. (2024·云南)酸、碱、盐是几类重要化合物,与人类日常生活和生产关系十分密切。
(1)现有以下三种物质:
A. 盐酸
B. 氢氧化钠
C. 氯化钠
①可用于金属表面除锈的是________(填字母序号,下同);可用作调味品的是______;可用作某些气体的干燥剂的是________。
②分别取上述三种物质的溶液于三支试管中,用一种试剂分别滴加到试管中就能将三种物质鉴别出来,这种试剂是____________________。
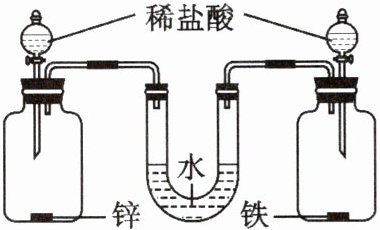
(2)兴趣小组按如图所示装置(气密性良好)进行实验。两个广口瓶中分别放有0.2 g的锌和铁,U形管两端液面相平,将等体积的足量稀盐酸同时加入广口瓶中,关闭活塞。反应结束,恢复至室温,U形管两端液面____________(填“左高右低”“左低右高”或“相平”)。
(3)酸和碱能发生中和反应。为验证稀盐酸能和氢氧化钙发生反应,实验小组在不使用酸碱指示剂的情况下,进行如下探究:
①将0.2 g氢氧化钙粉末加入试管中,加入1 mL水,充分振荡,固体未完全溶解;②再加入2 mL稀盐酸,充分振荡,得到澄清溶液;由此证明反应发生。小组同学讨论后认为上述实验不足以证明反应发生,原因是____________________,于是增加如下对照实验:重复上述实验①,再加入2 mL____________,充分振荡,观察到____________,最终证明了稀盐酸能和氢氧化钙发生反应。
(1)现有以下三种物质:
A. 盐酸
B. 氢氧化钠
C. 氯化钠
①可用于金属表面除锈的是________(填字母序号,下同);可用作调味品的是______;可用作某些气体的干燥剂的是________。
②分别取上述三种物质的溶液于三支试管中,用一种试剂分别滴加到试管中就能将三种物质鉴别出来,这种试剂是____________________。
(2)兴趣小组按如图所示装置(气密性良好)进行实验。两个广口瓶中分别放有0.2 g的锌和铁,U形管两端液面相平,将等体积的足量稀盐酸同时加入广口瓶中,关闭活塞。反应结束,恢复至室温,U形管两端液面____________(填“左高右低”“左低右高”或“相平”)。

(3)酸和碱能发生中和反应。为验证稀盐酸能和氢氧化钙发生反应,实验小组在不使用酸碱指示剂的情况下,进行如下探究:
①将0.2 g氢氧化钙粉末加入试管中,加入1 mL水,充分振荡,固体未完全溶解;②再加入2 mL稀盐酸,充分振荡,得到澄清溶液;由此证明反应发生。小组同学讨论后认为上述实验不足以证明反应发生,原因是____________________,于是增加如下对照实验:重复上述实验①,再加入2 mL____________,充分振荡,观察到____________,最终证明了稀盐酸能和氢氧化钙发生反应。
答案:
A@@C@@B@@紫色石蕊溶液(合理即可)@@左高右低@@稀盐酸中含水,加入稀盐酸后,也可能是未溶解的氢氧化钙继续溶于水,从而得到澄清溶液@@水@@固体未完全溶解
14. (2024·威海改编)
##### 染织工业中的酸和碱
酸和碱都是重要的化工原料,可用于纺织、印染等。染织工业的基本流程为:碱煮→酸洗→漂白→染色→质检,其中蕴含了丰富的化学知识。
**【碱煮原理】**
“碱煮”可除去布料表面的油污,使布料表面变得更加光滑、有光泽。古人利用贝壳和草木灰为原料制备氢氧化钾溶液洗涤布料,其过程是:贝壳灼烧得到贝壳灰,加水混合制成石灰乳,再与草木灰水混合,过滤即得。(贝壳的主要成分为碳酸钙,草木灰的主要成分是碳酸钾)
(1)实践发现石灰乳和草木灰水都能用来洗涤布料,但将两者混合之后洗涤效果更好。为探究原因,进行如下实验:用pH计测草木灰水的pH为11.2,石灰乳的pH为12.1,两者混合后上层清液的pH为12.8。分析上述实验数据可知,混合后溶液碱性______(填“增强”或“减弱”),请用化学方程式解释原因:____________________。
(2)为保持较好的洗涤效果,制得的氢氧化钾溶液须密封保存。
①小明猜想氢氧化钾与氢氧化钠性质相似,也能和二氧化碳反应,他的依据是二者都含有______(用符号表示)。
②为验证猜想,进行实验探究(如图所示):向A、B两个相同规格且充满COsub>2/sub>的瓶中分别注入等体积的氢氧化钾溶液和蒸馏水,充分反应后放在水平桌面上(U形管内为红墨水),观察到____________________现象,则猜想正确。
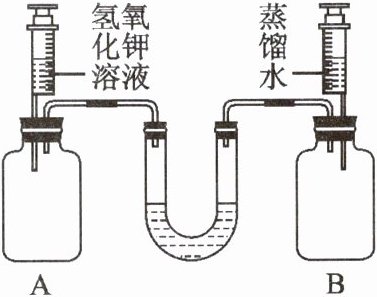
③欲探究实验后A瓶中溶液的溶质成分,请设计实验方案:____________________。
**【酸洗工艺】**
碱煮之后的布料表面残留的碱液、铁锈斑会影响布料的手感和后续工艺,需要进行“酸洗”。
(3)写出用稀硫酸除去铁锈斑反应的化学方程式:____________________。
(4)用稀硫酸“酸洗”后的布料必须充分水洗至呈中性才能烘干,若用稀盐酸则无需水洗,其原因是____________________。
**【染色奥秘】**
草木染是一种非遗染色技艺,是利用天然植物汁液给漂白后的布料染色。经过植物汁液染色后的布料还可以借助不同的酸性、碱性溶液进行调色。
为探究调色原理,以紫薯汁为例,进行如下实验:
|向紫薯汁中加入的溶液|白醋|盐酸|食盐水|草木灰水|石灰水|
|----|----|----|----|----|----|
|加入溶液后的颜色|红色|红色|紫色|绿色|绿色|
(5)请分析酸性、碱性溶液能对染色后的布料进行调色的原因:____________________。
##### 染织工业中的酸和碱
酸和碱都是重要的化工原料,可用于纺织、印染等。染织工业的基本流程为:碱煮→酸洗→漂白→染色→质检,其中蕴含了丰富的化学知识。
**【碱煮原理】**
“碱煮”可除去布料表面的油污,使布料表面变得更加光滑、有光泽。古人利用贝壳和草木灰为原料制备氢氧化钾溶液洗涤布料,其过程是:贝壳灼烧得到贝壳灰,加水混合制成石灰乳,再与草木灰水混合,过滤即得。(贝壳的主要成分为碳酸钙,草木灰的主要成分是碳酸钾)
(1)实践发现石灰乳和草木灰水都能用来洗涤布料,但将两者混合之后洗涤效果更好。为探究原因,进行如下实验:用pH计测草木灰水的pH为11.2,石灰乳的pH为12.1,两者混合后上层清液的pH为12.8。分析上述实验数据可知,混合后溶液碱性______(填“增强”或“减弱”),请用化学方程式解释原因:____________________。
(2)为保持较好的洗涤效果,制得的氢氧化钾溶液须密封保存。
①小明猜想氢氧化钾与氢氧化钠性质相似,也能和二氧化碳反应,他的依据是二者都含有______(用符号表示)。
②为验证猜想,进行实验探究(如图所示):向A、B两个相同规格且充满COsub>2/sub>的瓶中分别注入等体积的氢氧化钾溶液和蒸馏水,充分反应后放在水平桌面上(U形管内为红墨水),观察到____________________现象,则猜想正确。

③欲探究实验后A瓶中溶液的溶质成分,请设计实验方案:____________________。
**【酸洗工艺】**
碱煮之后的布料表面残留的碱液、铁锈斑会影响布料的手感和后续工艺,需要进行“酸洗”。
(3)写出用稀硫酸除去铁锈斑反应的化学方程式:____________________。
(4)用稀硫酸“酸洗”后的布料必须充分水洗至呈中性才能烘干,若用稀盐酸则无需水洗,其原因是____________________。
**【染色奥秘】**
草木染是一种非遗染色技艺,是利用天然植物汁液给漂白后的布料染色。经过植物汁液染色后的布料还可以借助不同的酸性、碱性溶液进行调色。
为探究调色原理,以紫薯汁为例,进行如下实验:
|向紫薯汁中加入的溶液|白醋|盐酸|食盐水|草木灰水|石灰水|
|----|----|----|----|----|----|
|加入溶液后的颜色|红色|红色|紫色|绿色|绿色|
(5)请分析酸性、碱性溶液能对染色后的布料进行调色的原因:____________________。
答案:
增强@@K₂CO₃ + Ca(OH)₂ = CaCO₃↓ + 2KOH@@OH⁻@@U形管中左侧液面高于右侧液面@@取少量待测液于试管,加入足量氯化钙溶液至不再产生白色沉淀(A中含有碳酸钾);再向静置后的上述试管中,滴加少量酚酞溶液,如果溶液变红,则说明含有氢氧化钾,A中溶质是氢氧化钾和碳酸钾;如果溶液没有变红,则说明A中没有氢氧化钾,只有碳酸钾(合理即可)@@Fe₂O₃ + 3H₂SO₄ = Fe₂(SO₄)₃ + 3H₂O@@在烘干过程中氯化氢会挥发掉@@天然植物汁液遇到酸性、碱性溶液会显示不同的颜色
查看更多完整答案,请扫码查看


