第55页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
9. (2024·江西)向盛有一定量氢氧化钙溶液的烧杯中通入适量的二氧化碳气体,反应过程中相关量$Y$与反应时间的关系如图所示,则$Y$可以表示 ( )
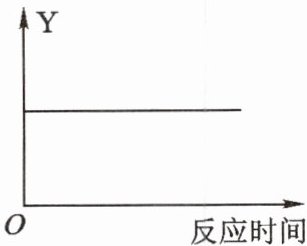
A. 烧杯内水的质量
B. 烧杯内溶液的质量
C. 烧杯内物质的总质量
D. 烧杯内物质中氢元素的总质量

A. 烧杯内水的质量
B. 烧杯内溶液的质量
C. 烧杯内物质的总质量
D. 烧杯内物质中氢元素的总质量
答案:
D
10. 碱在生产生活中的应用。

(1)(2024·山西)下图是西气东输第1站。此设备可完成天然气的收集、处理和输送,处理环节可将混合气中的$CO_2$、$N_2$等除去。实验室里除去$CO_2$通常使用氢氧化钠溶液,发生反应的化学方程式为$2NaOH + CO_2 = Na_2CO_3 + H_2O$。
(2)(2024·上海)水泥反碱也称水泥起霜,是一种墙面出现白霜的现象,已知墙体在下雨天会出现泛白现象。过程如图所示。氢氧化钙和二氧化碳反应的化学方程式为$Ca(OH)_2 + CO_2 = CaCO_3↓ + H_2O$。下雨天墙体出现泛白现象的原因是氢氧化钙随水迁移到墙表面,与空气中的二氧化碳反应生成碳酸钙白色沉淀。
(3)氨水($NH_3·H_2O$)可以电离为$NH_4^+$和$OH^-$,能用氨水来中和硫酸厂排出的含硫酸的废水,得到的硫酸铵[$(NH_4)_2SO_4$]是一种化学肥料,写出此反应的化学方程式:$2NH_3·H_2O + H_2SO_4 = (NH_4)_2SO_4 + 2H_2O$。


(1)(2024·山西)下图是西气东输第1站。此设备可完成天然气的收集、处理和输送,处理环节可将混合气中的$CO_2$、$N_2$等除去。实验室里除去$CO_2$通常使用氢氧化钠溶液,发生反应的化学方程式为$2NaOH + CO_2 = Na_2CO_3 + H_2O$。
(2)(2024·上海)水泥反碱也称水泥起霜,是一种墙面出现白霜的现象,已知墙体在下雨天会出现泛白现象。过程如图所示。氢氧化钙和二氧化碳反应的化学方程式为$Ca(OH)_2 + CO_2 = CaCO_3↓ + H_2O$。下雨天墙体出现泛白现象的原因是氢氧化钙随水迁移到墙表面,与空气中的二氧化碳反应生成碳酸钙白色沉淀。
(3)氨水($NH_3·H_2O$)可以电离为$NH_4^+$和$OH^-$,能用氨水来中和硫酸厂排出的含硫酸的废水,得到的硫酸铵[$(NH_4)_2SO_4$]是一种化学肥料,写出此反应的化学方程式:$2NH_3·H_2O + H_2SO_4 = (NH_4)_2SO_4 + 2H_2O$。

答案:
2NaOH + CO₂ = Na₂CO₃ + H₂O@@Ca(OH)₂ + CO₂ = CaCO₃↓ + H₂O@@墙体中的石灰随水迁移到墙面,然后与空气中的二氧化碳反应,生成了白色的碳酸钙@@2NH₃·H₂O + H₂SO₄ = (NH₄)₂SO₄ + 2H₂O
11. (2023·山西)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在小组合作学习过程中,对氢氧化钠的相关问题,以结构图的形式进行了如下梳理。联系实际,解决问题:
(1)氢氧化钠在生活中可用来______。
(2)氢氧化钠在空气中吸水后的热量变化为______。
(3)氢氧化钠使用时必须十分小心,原因是______。
(4)检验氢氧化钠溶液的酸碱度,最简单的方法是______。
(5)向氢氧化钠溶液中滴加硫酸铜溶液,发生反应的化学方程式为______。

(1)氢氧化钠在生活中可用来______。
(2)氢氧化钠在空气中吸水后的热量变化为______。
(3)氢氧化钠使用时必须十分小心,原因是______。
(4)检验氢氧化钠溶液的酸碱度,最简单的方法是______。
(5)向氢氧化钠溶液中滴加硫酸铜溶液,发生反应的化学方程式为______。

答案:
去除油污(合理即可)@@放热@@氢氧化钠具有强腐蚀性@@用pH试纸检测@@CuSO₄ + 2NaOH = Cu(OH)₂↓ + Na₂SO₄
12. 海洋是人类巨大的资源宝库,下图为从海水中提取金属镁的简易流程图。(已知:贝壳的主要成分是$CaCO_3$,其在高温条件下可以分解成生石灰和二氧化碳)
(1)海洋中含量最多的物质是______。
(2)实验室中进行操作Ⅰ时,玻璃棒的作用是______。
(3)生石灰转化为石灰乳的过程是______反应。
(4)上述流程中未涉及的反应类型是______反应。
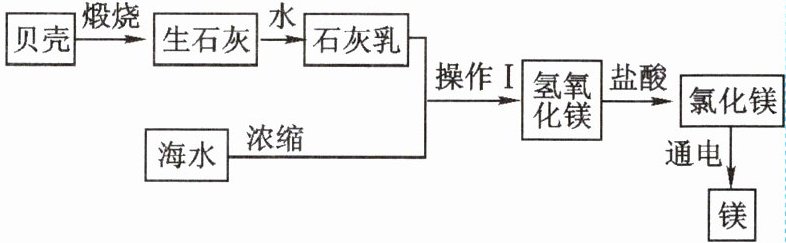
(1)海洋中含量最多的物质是______。
(2)实验室中进行操作Ⅰ时,玻璃棒的作用是______。
(3)生石灰转化为石灰乳的过程是______反应。
(4)上述流程中未涉及的反应类型是______反应。

答案:
水@@引流@@放热@@置换
查看更多完整答案,请扫码查看


