第19页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
13. 食盐的主要成分是NaCl。据记载,古人用“煎盐法”制取食盐的主要步骤有:①制卤水;②测卤水浓度;③煎卤得粗盐;④用“花水”冲洗粗盐得精品盐。
制取卤水的方法有两种:
①刮土淋卤:将结有盐霜的土,聚集成堆,清水浇注,卤水从堆底流出。
②草木灰淋卤:先将草木灰浸入海水,然后晾晒至现出白光,再用海水淋之,得卤水。
(1)卤水中的溶剂是 (填化学用语),卤水中大量存在的阴离子是
(填化学用语),卤水中大量存在的阴离子是 (填化学用语)。
(填化学用语)。
(2)卤水入锅前,将石莲子或鸡蛋投入卤水中,检验卤水的浓度,石莲子或者鸡蛋沉至卤水底部的为淡卤,半飘浮的为半淡卤,浮立于水面的为成卤,其中溶质质量分数最大的是 (填“淡卤”“半淡卤”或“成卤”)。
(填“淡卤”“半淡卤”或“成卤”)。
(3)以成卤入锅煎盐,有白色晶体析出时,此时卤水是氯化钠的 (填“饱和”或“不饱和”)溶液,草木灰的性质与活性炭相似,草木灰淋卤制作出的盐更洁白,是因为草木灰具有
(填“饱和”或“不饱和”)溶液,草木灰的性质与活性炭相似,草木灰淋卤制作出的盐更洁白,是因为草木灰具有 作用。
作用。
(4)经调查发现,“花水”是NaCl的饱和溶液,用“花水”冲洗粗盐而不用淡水冲洗的原因是
制取卤水的方法有两种:
①刮土淋卤:将结有盐霜的土,聚集成堆,清水浇注,卤水从堆底流出。
②草木灰淋卤:先将草木灰浸入海水,然后晾晒至现出白光,再用海水淋之,得卤水。
(1)卤水中的溶剂是
 (填化学用语),卤水中大量存在的阴离子是
(填化学用语),卤水中大量存在的阴离子是 (填化学用语)。
(填化学用语)。(2)卤水入锅前,将石莲子或鸡蛋投入卤水中,检验卤水的浓度,石莲子或者鸡蛋沉至卤水底部的为淡卤,半飘浮的为半淡卤,浮立于水面的为成卤,其中溶质质量分数最大的是
 (填“淡卤”“半淡卤”或“成卤”)。
(填“淡卤”“半淡卤”或“成卤”)。(3)以成卤入锅煎盐,有白色晶体析出时,此时卤水是氯化钠的
 (填“饱和”或“不饱和”)溶液,草木灰的性质与活性炭相似,草木灰淋卤制作出的盐更洁白,是因为草木灰具有
(填“饱和”或“不饱和”)溶液,草木灰的性质与活性炭相似,草木灰淋卤制作出的盐更洁白,是因为草木灰具有 作用。
作用。(4)经调查发现,“花水”是NaCl的饱和溶液,用“花水”冲洗粗盐而不用淡水冲洗的原因是

答案:
$H_{2}O$@@$Cl^{-}$@@成卤@@饱和@@吸附@@减少食盐因溶解而造成的损失
14. 建造南昌舰的特种钢材,需要用富铁矿石(含铁量高于50%)来冶炼。研学实践小组为测出某地赤铁矿石(主要成分是Fe₂O₃)中的含铁量,进行实验:取20g赤铁矿石样品,逐渐加入稀盐酸充分反应,实验的相关数据如图所示(假设杂质不溶于水也不与酸反应)。已知:该反应的原理为Fe₂O₃ + 6HCl = 2FeCl₃ + 3H₂O;FeCl₃易溶于水。
(1)20g赤铁矿石样品中氧化铁的质量为
(2)该样品中铁元素的质量分数为 由此判断出该赤铁矿石
由此判断出该赤铁矿石 (填“属于”或“不属于”)富铁矿石。
(填“属于”或“不属于”)富铁矿石。
(3)计算实验中所用稀盐酸的溶质质量分数。(写出计算过程)
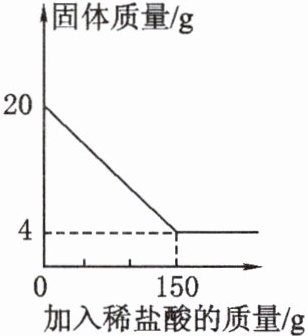
(1)20g赤铁矿石样品中氧化铁的质量为

(2)该样品中铁元素的质量分数为
 由此判断出该赤铁矿石
由此判断出该赤铁矿石 (填“属于”或“不属于”)富铁矿石。
(填“属于”或“不属于”)富铁矿石。(3)计算实验中所用稀盐酸的溶质质量分数。(写出计算过程)

答案:
14.(1)16 g (2)56% 属于 (3)解:设参加反应的氯化氢的质量为x。 $Fe_{2}O_{3}+6HCl = 2FeCl_{3}+3H_{2}O$ 160 219 16 g x $\frac{160}{219}=\frac{16 g}{x}$ $x = 21.9 g$ 实验中所用稀盐酸的溶质质量分数为: $\frac{21.9 g}{150 g}×100\% = 14.6\%$ 答:实验中所用稀盐酸的溶质质量分数为14.6%。
查看更多完整答案,请扫码查看


