第10页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
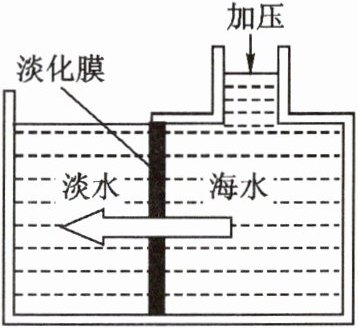
11. 海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子则不能通过淡化膜,从而得到淡水。对加压后右侧海水成分的变化进行分析,正确的是 ( )
A. 溶质质量增加
B. 溶剂质量减少
C. 溶液质量不变
D. 溶质质量分数减小

A. 溶质质量增加
B. 溶剂质量减少
C. 溶液质量不变
D. 溶质质量分数减小
答案:
B
12. 有100 g 10%的硝酸钾溶液,要使其溶质质量分数变为20%,有以下三种方法,按要求填空。
(1)继续加硝酸钾。所需硝酸钾的质量为________g。
(2)蒸发水分。需蒸发水的质量为______g。
(3)与溶质质量分数大于20%的浓硝酸钾溶液混合。如混入25%的硝酸钾溶液,所需该溶液的质量为________g。
(1)继续加硝酸钾。所需硝酸钾的质量为________g。
(2)蒸发水分。需蒸发水的质量为______g。
(3)与溶质质量分数大于20%的浓硝酸钾溶液混合。如混入25%的硝酸钾溶液,所需该溶液的质量为________g。
答案:
12.5@@50@@200
13. 下表是氢氧化钠溶液的密度与其溶质质量分数对照表(20 ℃)。

回答下列问题:
(1)20 ℃时,随着溶质质量分数增大,氢氧化钠溶液的密度逐渐________。
(2)配制100 g溶质质量分数为10%的氢氧化钠溶液,需要氢氧化钠固体________。
(3)20 ℃时溶质质量分数为10%的氢氧化钠溶液,体积为100 mL时的质量为______。
(4)现需配制400 g溶质质量分数为10%的氢氧化钠溶液,需要溶质质量分数为20%的氢氧化钠溶液________。

回答下列问题:
(1)20 ℃时,随着溶质质量分数增大,氢氧化钠溶液的密度逐渐________。
(2)配制100 g溶质质量分数为10%的氢氧化钠溶液,需要氢氧化钠固体________。
(3)20 ℃时溶质质量分数为10%的氢氧化钠溶液,体积为100 mL时的质量为______。
(4)现需配制400 g溶质质量分数为10%的氢氧化钠溶液,需要溶质质量分数为20%的氢氧化钠溶液________。
答案:
增大@@10 g@@111 g@@200 g
14. 实验室中浓硫酸试剂瓶上的标签如下图所示。
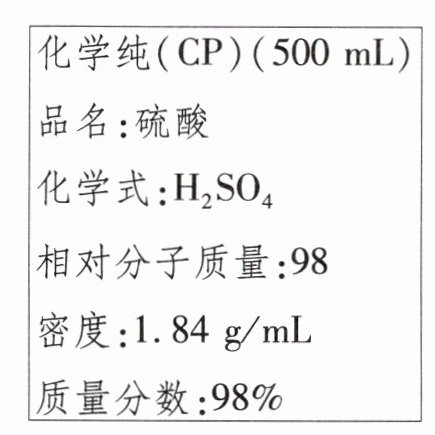
根据图示有关信息回答下列问题:
(1)请你写出计算该瓶硫酸溶液中所含硫酸质量的计算式:____________________________(不要求计算结果)。
(2)实验室欲配制500 g质量分数为19.6%的稀硫酸,需要这种浓硫酸的体积为多少?需要加入水的体积为多少?

根据图示有关信息回答下列问题:
(1)请你写出计算该瓶硫酸溶液中所含硫酸质量的计算式:____________________________(不要求计算结果)。
(2)实验室欲配制500 g质量分数为19.6%的稀硫酸,需要这种浓硫酸的体积为多少?需要加入水的体积为多少?
答案:
$500\ mL×1.84\ g/mL×98\%$@@解:所需浓硫酸的质量为:$(500\ g×19.6\%)÷98\% = 100\ g$
所需浓硫酸的体积为:$100\ g÷1.84\ g/mL\approx54.3\ mL$
所需水的体积为:$(500\ g - 100\ g)÷1\ g/mL = 400\ mL$
答:配制500 g溶质质量分数为19.6%的稀硫酸,需要98%的浓硫酸约54.3 mL,需要水400 mL。
查看更多完整答案,请扫码查看


