第29页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
4. (2024·福建)请参加“氯化钠欢乐之旅”的实践活动。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中$NaCl$的质量分数逐渐_________(填“增大”或“减小”)。
任务二 提纯粗盐
(2)粗盐提纯的有关操作如图所示。
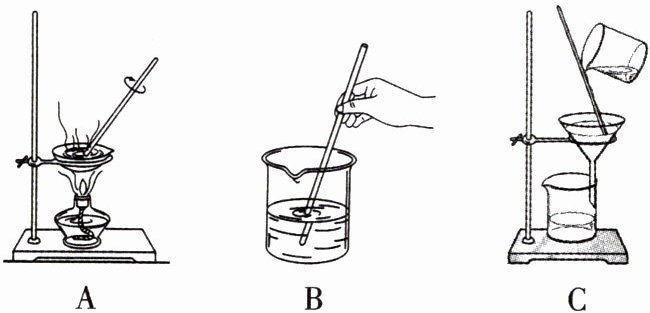
①正确的操作顺序是_________(填标号)。
②操作A中,当加热到蒸发皿中出现______________时,停止加热。
③操作C中,玻璃棒的作用是____________________。
任务三 应用食盐
(3)农业上常用质量分数为16%的$NaCl$溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和________________。
(4)$NaCl$是一种重要的化工原料。从元素守恒的视角,以$NaCl$为基本原料,可能制取的物质有______(写一种)。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中$NaCl$的质量分数逐渐_________(填“增大”或“减小”)。
任务二 提纯粗盐
(2)粗盐提纯的有关操作如图所示。

①正确的操作顺序是_________(填标号)。
②操作A中,当加热到蒸发皿中出现______________时,停止加热。
③操作C中,玻璃棒的作用是____________________。
任务三 应用食盐
(3)农业上常用质量分数为16%的$NaCl$溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和________________。
(4)$NaCl$是一种重要的化工原料。从元素守恒的视角,以$NaCl$为基本原料,可能制取的物质有______(写一种)。
答案:
增大@@BCA@@较多固体@@引流@@量筒@@NaOH(或$Cl_{2}$)
5. (2024·陕西)小明同学在测定某氯化钠溶液的溶质质量分数时,用两只烧杯各取80g待测溶液分别进行了如图所示的实验。已知:20℃时,氯化钠的溶解度为36g。

(1)20℃时,100g水中最多溶解氯化钠的质量是______g。
(2)20℃时,$A_{1}$、$A_{2}$中的溶液是氯化钠的___________(填“饱和”或“不饱和”)溶液。
(3)$B_{1}$、$B_{2}$中溶液的溶质与溶剂的质量比___________(填“相等”或“不相等”)。
(4)$x$的值为______。
(5)由上述实验可得出待测氯化钠溶液的溶质质量分数为________。

(1)20℃时,100g水中最多溶解氯化钠的质量是______g。
(2)20℃时,$A_{1}$、$A_{2}$中的溶液是氯化钠的___________(填“饱和”或“不饱和”)溶液。
(3)$B_{1}$、$B_{2}$中溶液的溶质与溶剂的质量比___________(填“相等”或“不相等”)。
(4)$x$的值为______。
(5)由上述实验可得出待测氯化钠溶液的溶质质量分数为________。
答案:
36@@不饱和@@相等@@2.4@@25%
[提示:(2)20 °C 时,氯化钠的溶解度为 36 g。若$A_{1}$是饱和溶液,则蒸发的 10 g 水与析出的氯化钠固体会形成饱和溶液,析出的氯化钠固体质量为 10 g×$\frac{36 g}{100 g}$ = 3.6 g,3.6 g>2 g,说明$A_{1}$中的溶液是不饱和溶液。溶液具有均一性,故$A_{2}$中的溶液也是不饱和溶液。(3)根据图示可知,$B_{1}$、$B_{2}$中的溶液都是饱和溶液,相同温度下溶质与溶剂的质量比相等。(4)$B_{1}$溶液的质量为 80 g - 10 g - 2 g = 68 g,则该饱和溶液中氯化钠的质量为 68 g×$\frac{36 g}{100 g + 36 g}$ = 18 g,水的质量为 68 g - 18 g = 50 g,则$A_{1}$溶液中水的质量为 50 g + 10 g = 60 g,氯化钠固体质量为 18 g + 2 g = 20 g。溶液具有均一性,$A_{1}$与$A_{2}$中溶液的溶质、溶剂质量相等。20 °C 时,60 g 水最多溶解氯化钠的质量为 60 g×$\frac{36 g}{100 g}$ = 21.6 g,20 g + 4 g - 21.6 g = 2.4 g,故 x 的值为 2.4。(5)根据第(4)小题分析可知,待测氯化钠溶液的溶质质量分数为$\frac{20 g}{20 g + 60 g}$×100% = 25%]
[提示:(2)20 °C 时,氯化钠的溶解度为 36 g。若$A_{1}$是饱和溶液,则蒸发的 10 g 水与析出的氯化钠固体会形成饱和溶液,析出的氯化钠固体质量为 10 g×$\frac{36 g}{100 g}$ = 3.6 g,3.6 g>2 g,说明$A_{1}$中的溶液是不饱和溶液。溶液具有均一性,故$A_{2}$中的溶液也是不饱和溶液。(3)根据图示可知,$B_{1}$、$B_{2}$中的溶液都是饱和溶液,相同温度下溶质与溶剂的质量比相等。(4)$B_{1}$溶液的质量为 80 g - 10 g - 2 g = 68 g,则该饱和溶液中氯化钠的质量为 68 g×$\frac{36 g}{100 g + 36 g}$ = 18 g,水的质量为 68 g - 18 g = 50 g,则$A_{1}$溶液中水的质量为 50 g + 10 g = 60 g,氯化钠固体质量为 18 g + 2 g = 20 g。溶液具有均一性,$A_{1}$与$A_{2}$中溶液的溶质、溶剂质量相等。20 °C 时,60 g 水最多溶解氯化钠的质量为 60 g×$\frac{36 g}{100 g}$ = 21.6 g,20 g + 4 g - 21.6 g = 2.4 g,故 x 的值为 2.4。(5)根据第(4)小题分析可知,待测氯化钠溶液的溶质质量分数为$\frac{20 g}{20 g + 60 g}$×100% = 25%]
6. (2024·重庆,改编)某课外活动小组学习了溶液的知识后进行了如下实验:(固体M不含结晶水,忽略实验过程中溶剂的蒸发)
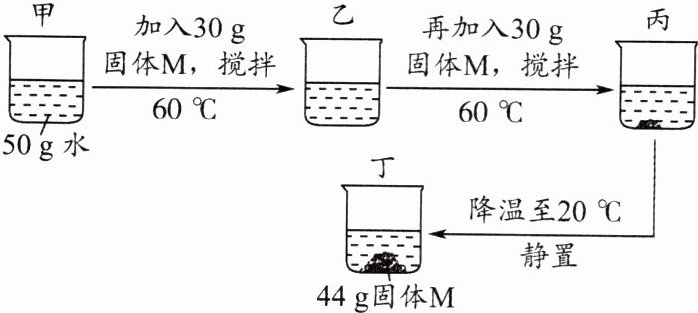
请回答下列问题:
(1)丁中溶液的质量为______g。
(2)下图为实验过程中烧杯内液体质量随时间的变化关系。

①溶液开始降温的时间是______s(填“$t_{1}$”或“$t_{2}$”)。
②丙中溶质与溶剂的质量比为________。
③乙中的溶液为___________(填“饱和”或“不饱和”)溶液。
④0~$t_{2}$s时间段内,下列说法正确的是_________(填标号)。
A. $b$点到$c$点溶剂质量不变
B. $c$点表示丁中溶液的质量
C. $a$点所示溶液为不饱和溶液

请回答下列问题:
(1)丁中溶液的质量为______g。
(2)下图为实验过程中烧杯内液体质量随时间的变化关系。

①溶液开始降温的时间是______s(填“$t_{1}$”或“$t_{2}$”)。
②丙中溶质与溶剂的质量比为________。
③乙中的溶液为___________(填“饱和”或“不饱和”)溶液。
④0~$t_{2}$s时间段内,下列说法正确的是_________(填标号)。
A. $b$点到$c$点溶剂质量不变
B. $c$点表示丁中溶液的质量
C. $a$点所示溶液为不饱和溶液
答案:
66@@$t_{1}$@@11 : 10@@不饱和@@ABC
查看更多完整答案,请扫码查看


