第21页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
7. B (2024·成都)有关金属的实验如图,能达到相应目的的是 ( )
A. 比较合金与其组分金属的硬度
B. 验证锌、铁和铜的金属活动性顺序
C. 证明铜生锈与CO₂、O₂和H₂O有关
D. 验证质量守恒定律



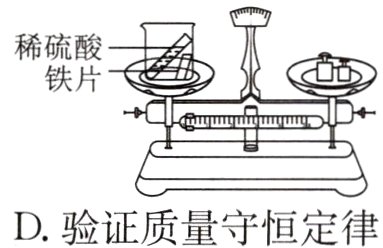
A. 比较合金与其组分金属的硬度
B. 验证锌、铁和铜的金属活动性顺序
C. 证明铜生锈与CO₂、O₂和H₂O有关
D. 验证质量守恒定律




答案:
B
8. B 化学学习小组对某工业废水进行实验探究,部分过程如图。下列有关说法正确的是 ( )
A. 步骤①置换出Fe、Ag两种单质
B. 操作a需要漏斗、酒精灯等仪器
C. 实验能探明三种金属活动性强弱
D. 步骤④加盐酸是为了除去Cu粉
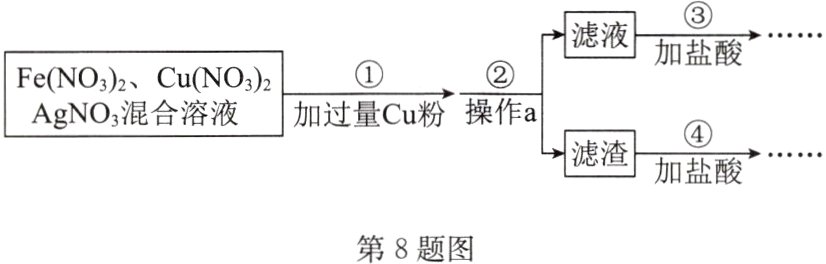
A. 步骤①置换出Fe、Ag两种单质
B. 操作a需要漏斗、酒精灯等仪器
C. 实验能探明三种金属活动性强弱
D. 步骤④加盐酸是为了除去Cu粉

答案:
C
9. B 下列现象和事实,可用金属活动性作出合理解释的是 ( )
①金属镁在空气中比铝更容易燃烧,说明镁比铝的活动性强
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配制农药波尔多液时,不能用铁制容器
④尽管金属的种类很多,但在自然界中,仅有少数金属(银、铂、金)能以单质形式存在
A. ①②
B. ①③④
C. ③④
D. ①②③④
①金属镁在空气中比铝更容易燃烧,说明镁比铝的活动性强
②金属铝比金属锌更耐腐蚀,说明锌比铝活动性强
③用硫酸铜、石灰水配制农药波尔多液时,不能用铁制容器
④尽管金属的种类很多,但在自然界中,仅有少数金属(银、铂、金)能以单质形式存在
A. ①②
B. ①③④
C. ③④
D. ①②③④
答案:
B
10. B 一定质量的锌、铁分别和等量的盐酸反应,产生氢气的质量与时间的关系如图所示,下列说法不正确的是 ( )
A. t₁ min时,产生氢气的质量锌比铁大
B. t₁ min时,产生氢气的速率锌比铁大
C. t₂ min时,参加反应的锌的质量与铁相同
D. t₂ min时,锌、铁消耗的盐酸质量相同
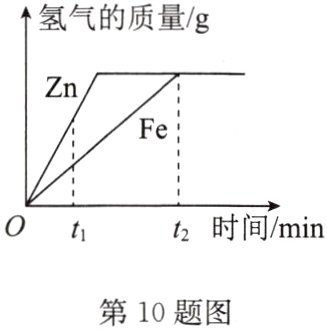
A. t₁ min时,产生氢气的质量锌比铁大
B. t₁ min时,产生氢气的速率锌比铁大
C. t₂ min时,参加反应的锌的质量与铁相同
D. t₂ min时,锌、铁消耗的盐酸质量相同

答案:
C
11. B (2023·河南)某金属混合物由Mg、Al、Zn、Fe四种金属中的两种组成。4 g该金属混合物与足量的盐酸充分反应,得到0.2 g氢气,则该金属混合物的组成不可能是 ( )
A. Mg和Al
B. Fe和Al
C. Fe和Mg
D. Mg和Zn
A. Mg和Al
B. Fe和Al
C. Fe和Mg
D. Mg和Zn
答案:
A 点拨:设生成0.2 g氢气需要金属的质量分别为锌的质量为x,镁的质量为y,铁的质量为a,铝的质量为b;则:
$Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$
65 2
x 0.2 g
$\frac{65}{2}=\frac{x}{0.2 g}$ $x = 6.5 g$
$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$
24 2
y 0.2 g
$\frac{24}{2}=\frac{y}{0.2 g}$ $y = 2.4 g$
$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
56 2
a 0.2 g
$\frac{56}{2}=\frac{a}{0.2 g}$ $a = 5.6 g$
$2Al + 6HCl = 2AlCl_{3} + 3H_{2}\uparrow$
54 6
b 0.2 g
$\frac{54}{6}=\frac{b}{0.2 g}$ $b = 1.8 g$
某金属混合物由Mg、Al、Zn、Fe四种金属中的两种组成。4 g该金属混合物与足量的盐酸充分反应,得到0.2 g氢气,则该金属混合物的组成不可能是Mg和Al,因为Mg和Al这两种金属需要的质量都小于4 g。
$Zn + 2HCl = ZnCl_{2} + H_{2}\uparrow$
65 2
x 0.2 g
$\frac{65}{2}=\frac{x}{0.2 g}$ $x = 6.5 g$
$Mg + 2HCl = MgCl_{2} + H_{2}\uparrow$
24 2
y 0.2 g
$\frac{24}{2}=\frac{y}{0.2 g}$ $y = 2.4 g$
$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
56 2
a 0.2 g
$\frac{56}{2}=\frac{a}{0.2 g}$ $a = 5.6 g$
$2Al + 6HCl = 2AlCl_{3} + 3H_{2}\uparrow$
54 6
b 0.2 g
$\frac{54}{6}=\frac{b}{0.2 g}$ $b = 1.8 g$
某金属混合物由Mg、Al、Zn、Fe四种金属中的两种组成。4 g该金属混合物与足量的盐酸充分反应,得到0.2 g氢气,则该金属混合物的组成不可能是Mg和Al,因为Mg和Al这两种金属需要的质量都小于4 g。
查看更多完整答案,请扫码查看


