第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
12. B (2023·定远县模拟)化学反应的快慢与许多因素有关,控制变量法是科学探究中常用的方法。某兴趣小组设计以下实验探究影响金属与酸反应快慢的因素。
【实验一】取四份等质量的铁分别与足量的稀盐酸进行反应,反应温度如下表所示。如图甲为反应时间与产生气体体积的关系曲线。

|实验|温度/℃|铁的质量及规格|
|----|----|----|
|a|40|10 g 200目铁粉|
|b|30|10 g 200目铁粉|
|c|30|10 g直径0.2 mm铁丝|
|d|20|10 g直径0.2 mm铁丝|
(1)铁与稀盐酸反应的化学方程式为______________________________。
(2)对比图甲中实验a和b的曲线,得出的结论是______________________________,若要比较金属铁的表面积对反应快慢的影响,应选择的实验组别是_______。
(3)实验中观察到气体产生速率“逐渐变快又变慢”,“逐渐变快”的原因是________________。
【实验二】常温时,用足量的镁、锌、铁三种金属分别与同体积同浓度的盐酸反应。实验装置如图乙所示,压强变化如图丙所示(压强越大,表示产生氢气的量越多)。

(4)实验中,还需要控制的变量是________________。
(5)实验得出的结论是金属与酸反应的速率与________________有关。
【实验一】取四份等质量的铁分别与足量的稀盐酸进行反应,反应温度如下表所示。如图甲为反应时间与产生气体体积的关系曲线。

|实验|温度/℃|铁的质量及规格|
|----|----|----|
|a|40|10 g 200目铁粉|
|b|30|10 g 200目铁粉|
|c|30|10 g直径0.2 mm铁丝|
|d|20|10 g直径0.2 mm铁丝|
(1)铁与稀盐酸反应的化学方程式为______________________________。
(2)对比图甲中实验a和b的曲线,得出的结论是______________________________,若要比较金属铁的表面积对反应快慢的影响,应选择的实验组别是_______。
(3)实验中观察到气体产生速率“逐渐变快又变慢”,“逐渐变快”的原因是________________。
【实验二】常温时,用足量的镁、锌、铁三种金属分别与同体积同浓度的盐酸反应。实验装置如图乙所示,压强变化如图丙所示(压强越大,表示产生氢气的量越多)。

(4)实验中,还需要控制的变量是________________。
(5)实验得出的结论是金属与酸反应的速率与________________有关。
答案:
12.
(1)$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(2)相同条件下,温度越高,金属与酸反应速率越快 b、c
(3)铁与稀盐酸反应放热,反应速率加快
(4)金属颗粒的大小
(5)金属的活动性
(1)$Fe + 2HCl = FeCl_{2} + H_{2}\uparrow$
(2)相同条件下,温度越高,金属与酸反应速率越快 b、c
(3)铁与稀盐酸反应放热,反应速率加快
(4)金属颗粒的大小
(5)金属的活动性
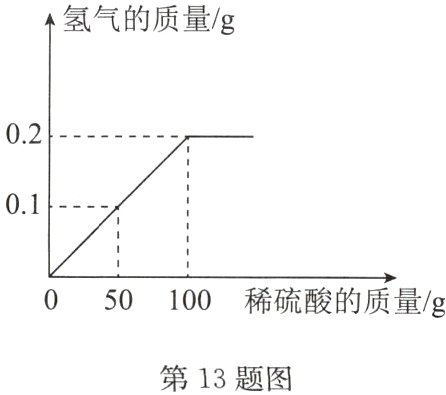
13. C (2023·容县模拟)某项目学习小组为测定铜锌合金中锌的质量分数,向盛有30 g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示,回答下列问题:
(1)充分反应后生成氢气的质量为_______g。
(2)合金样品中锌的质量分数是多少?(结果精确到0.1%)
(1)充分反应后生成氢气的质量为_______g。
(2)合金样品中锌的质量分数是多少?(结果精确到0.1%)

答案:
13.
(1)0.2
(2)21.7%
(1)0.2
(2)21.7%
查看更多完整答案,请扫码查看


