第75页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
13. B 下面是某小组同学学习氢氧化钠和稀盐酸反应时的记录:在盛有氢氧化钠溶液的烧杯中,插入一支温度计测量溶液的温度。用胶头滴管吸取10%的稀盐酸逐滴加入氢氧化钠溶液中。
(1)探究实验中的能量变化
在实验过程中,随着稀盐酸的不断滴入,溶液的温度逐渐升高,你认为溶液温度升高的原因是______________________________。
(2)探究反应终点问题
用什么方法证明此反应已恰好完全进行?
小红说:在实验后所得溶液中滴入几滴无色酚酞溶液,若溶液颜色没有变化,则反应恰好完全进行。
小文说:在氢氧化钠溶液中预先滴入几滴无色酚酞溶液,然后再加入稀盐酸,若溶液颜色刚好变成无色,则反应恰好完全进行。
你认为他们的说法中,不正确的是______,理由是________________________。
(3)关于实验中的细节和意外情况
①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是________________________;
②实验过程中,要用玻璃棒不断搅拌,这样做的目的是________________________;
③小凤在她的实验过程中意外发现有气泡出现,你认为可能的原因是________________。
(1)探究实验中的能量变化
在实验过程中,随着稀盐酸的不断滴入,溶液的温度逐渐升高,你认为溶液温度升高的原因是______________________________。
(2)探究反应终点问题
用什么方法证明此反应已恰好完全进行?
小红说:在实验后所得溶液中滴入几滴无色酚酞溶液,若溶液颜色没有变化,则反应恰好完全进行。
小文说:在氢氧化钠溶液中预先滴入几滴无色酚酞溶液,然后再加入稀盐酸,若溶液颜色刚好变成无色,则反应恰好完全进行。
你认为他们的说法中,不正确的是______,理由是________________________。
(3)关于实验中的细节和意外情况
①实验中,稀盐酸必须用胶头滴管逐滴滴加,这样做的目的是________________________;
②实验过程中,要用玻璃棒不断搅拌,这样做的目的是________________________;
③小凤在她的实验过程中意外发现有气泡出现,你认为可能的原因是________________。
答案:
13.
(1)中和反应放出热量
(2)小红 如果盐酸过量,加入酚酞溶液,溶液也不变色
(3)①防止盐酸过量 ②使反应充分、快速 ③NaOH溶液已变质
(1)中和反应放出热量
(2)小红 如果盐酸过量,加入酚酞溶液,溶液也不变色
(3)①防止盐酸过量 ②使反应充分、快速 ③NaOH溶液已变质
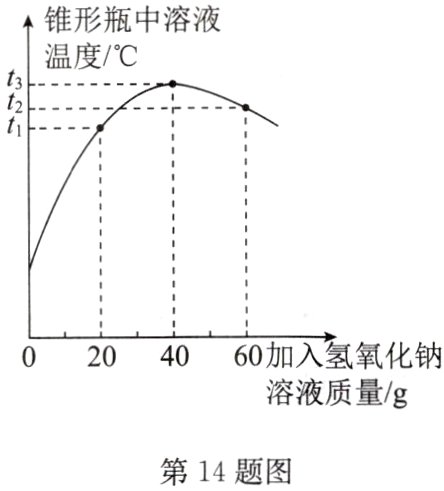
14. C 化学小组参与“铅蓄废电池中硫酸回收”的研学项目,回收时需要测定电池废液中硫酸的质量分数。向装有50 g废液的锥形瓶中加入质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等电子设备采集信息并绘制成如图(杂质可溶但不参加反应),请据图回答相关问题。
(1)该反应是______(填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为______℃。
(3)计算废液中硫酸的质量分数。(写出计算过程)
(1)该反应是______(填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为______℃。
(3)计算废液中硫酸的质量分数。(写出计算过程)

答案:
14.
(1)放热
(2)$t_3$
(3)19.6%(过程见点拨)
点拨:
(3)设废液中硫酸的质量为 $x$。
$2NaOH + H_2SO_4 = Na_2SO_4 + 2H_2O$
80 98
$40 g×20\%$ $x$
$\frac{80}{98} = \frac{40 g×20\%}{x}$ $x = 9.8 g$。
废液中硫酸的质量分数为 $\frac{9.8 g}{50 g}×100\% = 19.6\%$。
(1)放热
(2)$t_3$
(3)19.6%(过程见点拨)
点拨:
(3)设废液中硫酸的质量为 $x$。
$2NaOH + H_2SO_4 = Na_2SO_4 + 2H_2O$
80 98
$40 g×20\%$ $x$
$\frac{80}{98} = \frac{40 g×20\%}{x}$ $x = 9.8 g$。
废液中硫酸的质量分数为 $\frac{9.8 g}{50 g}×100\% = 19.6\%$。
查看更多完整答案,请扫码查看


