第30页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
9 [中]同学们对含有$K_2SO_4、$$K_2SO_3、$$K_2S$的混合物中各元素的含量进行探究,经测定,其中氧元素的质量分数为32%,则含有的钾元素的质量分数为(
A.70.9%
B.54.9%
C.48.2%
D.34.2%
C
)A.70.9%
B.54.9%
C.48.2%
D.34.2%
答案:
9.C 【解析】
识图解题
氧元素的质量分数为32%
钾元素与硫元素的质量分数之和为1 - 32%=68%
由K₂SO₄、K₂SO₃、K₂S的化学式可知,混合物中钾原子与硫原子的个数比为2:1,钾元素与硫元素的质量比为(39×2):32=39:16
钾元素的质量分数为68%×(39/39 + 16×100%)≈48.2%。
识图解题
氧元素的质量分数为32%
钾元素与硫元素的质量分数之和为1 - 32%=68%
由K₂SO₄、K₂SO₃、K₂S的化学式可知,混合物中钾原子与硫原子的个数比为2:1,钾元素与硫元素的质量比为(39×2):32=39:16
钾元素的质量分数为68%×(39/39 + 16×100%)≈48.2%。
10 [2024四川巴中质检](1)请用化学符号填空。
①氦元素:
②镁离子:
(2)下列化学符号中,数字“3”可表示不同的含义,其中表示一个离子所带电荷数的是
$①3Cl_2 ②SO_3 ③Al^3+ ④3K$
①氦元素:
He
;②镁离子:
Mg²⁺
;(2)下列化学符号中,数字“3”可表示不同的含义,其中表示一个离子所带电荷数的是
③
(填序号,下同),表示一个分子中所含原子个数的是②
。$①3Cl_2 ②SO_3 ③Al^3+ ④3K$
答案:
10.
(1)①He ②Mg²⁺
(2)③ ②
【解析】
(1)①氦元素的化学符号为He。②镁离子的化学符号为Mg²⁺。
(2)Al³⁺中的“3”表示一个铝离子带有3个单位的正电荷。SO₃中的“3”表示1个三氧化硫分子中含有3个氧原子。
(1)①He ②Mg²⁺
(2)③ ②
【解析】
(1)①氦元素的化学符号为He。②镁离子的化学符号为Mg²⁺。
(2)Al³⁺中的“3”表示一个铝离子带有3个单位的正电荷。SO₃中的“3”表示1个三氧化硫分子中含有3个氧原子。
11 [2024四川广安中考]金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、C、D、E的微粒结构示意图如图所示。元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分。
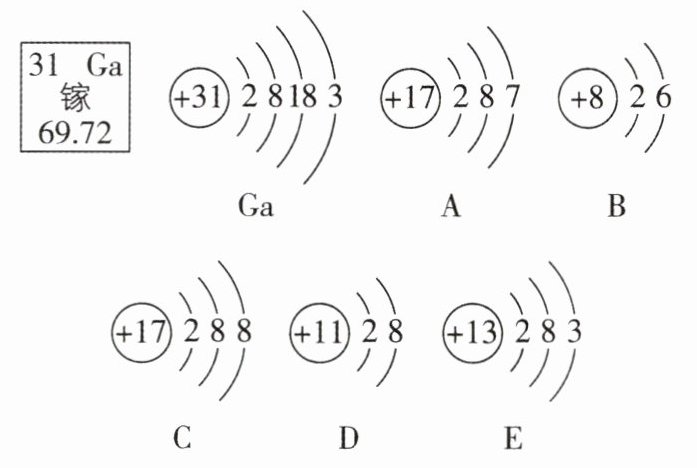
回答下列问题。
(1)镓元素位于元素周期表第______
(2)在元素周期表中,镓元素与A元素所占方格颜色______
(3)图中,一共涉及______
(4)E失去3个电子,形成阳离子,该离子符号为______

回答下列问题。
(1)镓元素位于元素周期表第______
四
周期。(2)在元素周期表中,镓元素与A元素所占方格颜色______
不同
(填“相同”或“不同”)。(3)图中,一共涉及______
5
种元素。(4)E失去3个电子,形成阳离子,该离子符号为______
Al³⁺
。
答案:
11.
(1)四
(2)不同
(3)5
(4)Al³⁺
【解析】
(1)元素所在元素周期表中周期数等于对应原子核外电子层数,镓元素的原子核外有4个电子层,则在元素周期表中,镓元素位于第四周期。
(2)元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分,A的核内质子数为17,是氯元素,为非金属元素,镓元素属于金属元素,则在元素周期表中,镓元素与A元素所占方格颜色不同。
(3)不同种元素最本质的区别是质子数不同,A和C核内质子数相同,属于同一种元素,图中共涉及5种元素。
(4)E为铝原子,铝原子失去3个电子,形成带3个单位正电荷的铝离子,其离子符号为Al³⁺。
关键点拨
a是一个H原子,b是由一个H原子和一个D原子组成的物质,c是由两个H原子和一个D原子组成的物质,d是由两个H原子组成的物质,e是一个D原子。
易错警示
“3K”中的“3”表示原子个数,不表示一个分子中所含原子的个数。
(1)四
(2)不同
(3)5
(4)Al³⁺
【解析】
(1)元素所在元素周期表中周期数等于对应原子核外电子层数,镓元素的原子核外有4个电子层,则在元素周期表中,镓元素位于第四周期。
(2)元素周期表中,金属元素、非金属元素和稀有气体元素常用不同颜色区分,A的核内质子数为17,是氯元素,为非金属元素,镓元素属于金属元素,则在元素周期表中,镓元素与A元素所占方格颜色不同。
(3)不同种元素最本质的区别是质子数不同,A和C核内质子数相同,属于同一种元素,图中共涉及5种元素。
(4)E为铝原子,铝原子失去3个电子,形成带3个单位正电荷的铝离子,其离子符号为Al³⁺。
关键点拨
a是一个H原子,b是由一个H原子和一个D原子组成的物质,c是由两个H原子和一个D原子组成的物质,d是由两个H原子组成的物质,e是一个D原子。
易错警示
“3K”中的“3”表示原子个数,不表示一个分子中所含原子的个数。
12 [2025江西吉安期中,中]如图为某品牌巧克力说明书的部分内容,查阅资料得知配料表中香兰素又名香草醛,其化学式为$C_8H_8O_3。$香兰素是一种使用广泛的香料,食品厂商在生产时使用香兰素必须遵守一定的使用剂量要求。

(1)香兰素的相对分子质量为______
(2)香兰素中碳、氢、氧元素的质量比为______
(3)香兰素中碳元素的质量分数为______
(4)若小明同学每天食用2块该巧克力(一块10g),根据配料表中数据分析计算,小明一天最多摄入香兰素的质量为______
(5)计算608kg香兰素中含有碳元素的质量(写出计算过程)。

(1)香兰素的相对分子质量为______
152
。(2)香兰素中碳、氢、氧元素的质量比为______
12:1:6
。(3)香兰素中碳元素的质量分数为______
63.2%
(结果保留至0.1%)。(4)若小明同学每天食用2块该巧克力(一块10g),根据配料表中数据分析计算,小明一天最多摄入香兰素的质量为______
19.4
mg。(5)计算608kg香兰素中含有碳元素的质量(写出计算过程)。
解:608kg香兰素中含有碳元素的质量为608kg×(12×8/152×100%)=384kg。答:608kg香兰素中含有碳元素的质量为384kg。
答案:
12.
(1)152
(2)12:1:6
(3)63.2%
(4)19.4
(5)解:608kg香兰素中含有碳元素的质量为608kg×(12×8/152×100%)=384kg。答:608kg香兰素中含有碳元素的质量为384kg。
【解析】
(1)香兰素的相对分子质量为12×8+1×8+16×3=152。
(2)香兰素中碳、氢、氧三种元素的质量比为(12×8):(1×8):(16×3)=12:1:6。
(3)香兰素中碳元素的质量分数为12×8/152×100%≈63.2%。
(4)若小明同学每天食用2块该巧克力,一块巧克力10g,该巧克力中香兰素含量≤970mg/kg,则小明一天最多摄入香兰素的质量为970mg/kg×2×0.01kg=19.4mg。
(1)152
(2)12:1:6
(3)63.2%
(4)19.4
(5)解:608kg香兰素中含有碳元素的质量为608kg×(12×8/152×100%)=384kg。答:608kg香兰素中含有碳元素的质量为384kg。
【解析】
(1)香兰素的相对分子质量为12×8+1×8+16×3=152。
(2)香兰素中碳、氢、氧三种元素的质量比为(12×8):(1×8):(16×3)=12:1:6。
(3)香兰素中碳元素的质量分数为12×8/152×100%≈63.2%。
(4)若小明同学每天食用2块该巧克力,一块巧克力10g,该巧克力中香兰素含量≤970mg/kg,则小明一天最多摄入香兰素的质量为970mg/kg×2×0.01kg=19.4mg。
查看更多完整答案,请扫码查看


