第15页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
1 [2024山东烟台期中]如图为某原子的结构示意图。下列有关叙述错误的是(
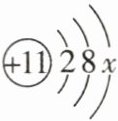
A.$x= 1$
B.该原子属于活泼的非金属原子
C.该原子在化学反应中容易失去电子
D.该原子能与氯原子发生化学反应
B
)
A.$x= 1$
B.该原子属于活泼的非金属原子
C.该原子在化学反应中容易失去电子
D.该原子能与氯原子发生化学反应
答案:
B [解析]原子中,质子数=核外电子数,11=2+8+x,x=1,A正确。该原子为钠原子,属于活泼的金属原子,B错误。该原子的最外层电子数是1,小于4,在化学反应中易失去1个电子而形成阳离子,C正确。该原子能与氯原子发生化学反应,生成氯化钠,D正确。
下列关于$Fe$、$Fe^{2+}$、$Fe^{3+}$说法中,不正确的是(
A.它们的核电荷数相同
B.它们的质子数相同,中子数不同
C.它们的核外电子数不同
D.它们的质量相近
B
)A.它们的核电荷数相同
B.它们的质子数相同,中子数不同
C.它们的核外电子数不同
D.它们的质量相近
答案:
B [解析]一个铁原子失去2个电子形成$Fe^{2+}$、一个铁原子失去3个电子形成$Fe^{3+}$,由此可知,Fe、$Fe^{2+}$、$Fe^{3+}$中质子数、中子数和核电荷数相同,A、C正确,B错误;Fe、$Fe^{2+}$、$Fe^{3+}$的电子数不同,但电子质量远小于中子和质子质量,可忽略不计,所以它们的质量相近,D正确。
3 [2024山东青岛质检]已知一个硫原子的质量为$m$g,其相对原子质量为32,则一个相对原子质量为152的铕(Eu)原子的质量为(
A.$\frac{152m}{32}$
B.$\frac{152m}{12}g$
C.$\frac{152m}{32}g$
D.$\frac{152m}{12}$
C
)A.$\frac{152m}{32}$
B.$\frac{152m}{12}g$
C.$\frac{152m}{32}g$
D.$\frac{152m}{12}$
答案:
C [解析]已知一个硫原子的质量为mg,其相对原子质量为32,设一个相对原子质量为152的铕(Eu)原子的质量为x,则$\frac{mg}{x}=\frac{32}{152}$,$x=\frac{152m}{32}g$。故选C。
4 [2025山东聊城质检]化学上可用符号“$_{Z}^{A}M$”表示原子的组成,其中M代表元素符号,$Z$表示原子核内质子数,$A$表示原子核内质子数与中子数之和。已知$_{a}^{b}X^{n+}和_{c}^{d}Y^{m-}$的核外电子排布完全相同,则下列关系正确的是(
A.$b-a= d-c$
B.$a-n= c+m$
C.$a+n= c-m$
D.$b-n= d+m$
B
)A.$b-a= d-c$
B.$a-n= c+m$
C.$a+n= c-m$
D.$b-n= d+m$
答案:
B [解析]由题干信息可知两种离子的核外电子排布完全相同,则$_{a}X^{n+}$、$_{c}Y^{m - }$的核外电子数相等,$_{a}X^{n+}$质子数为a,则所含核外电子数为$a - n$,$_{c}Y^{m - }$质子数为c,所含核外电子数为$c + m$,则有$a - n = c + m$。故选B。
如图是四种粒子的结构示意图,下列说法正确的是(
A.③可以通过得到电子变成④
B.②在化学反应中容易失去电子
C.①④的结构相对稳定
D.④是一种阴离子
C
)A.③可以通过得到电子变成④
B.②在化学反应中容易失去电子
C.①④的结构相对稳定
D.④是一种阴离子
答案:
C [解析]③④的质子数相同,③的最外层电子数为1,小于4,在化学变化中易失去1个电子形成④,A不正确;②的最外层电子数是7,大于4,在化学反应中容易得到电子,B不正确;①④的最外层电子数都是8,属于相对稳定结构,C正确;④的质子数为11,大于核外电子数,是一种阳离子,D不正确。
6 已知粒子种类判断粒子结构[2025山东泰安期中]根据所学的化学知识回答下列问题。
(1)已知某粒子(原子或离子)的核外共有2个电子层,其结构示意图如图所示。
①若该粒子为原子,则$m= $______。
②若该粒子为阴离子,则$m-2$______(填“>”“<”或“=”)x。
(2)若某原子的相对原子质量为23,核内质子数比中子数少一个,则该原子对应的阳离子的核外电子数为______。

(1)已知某粒子(原子或离子)的核外共有2个电子层,其结构示意图如图所示。
①若该粒子为原子,则$m= $______。
②若该粒子为阴离子,则$m-2$______(填“>”“<”或“=”)x。
(2)若某原子的相对原子质量为23,核内质子数比中子数少一个,则该原子对应的阳离子的核外电子数为______。

答案:
(1)①$2 + x$ ②<
(2)10[解析]
(1)①在原子中,质子数=核外电子数,则$m = 2 + x$。②阴离子是由原子得到电子形成的,则$m < 2 + x$,即$m - 2 < x$。
(2)相对原子质量≈质子数+中子数,则该原子的质子数为$\frac{23 - 1}{2}=11$,该原子的结构示意图为 ,易失去1个电子形成阳离子,即该原子对应的阳离子的核外电子数为10。
,易失去1个电子形成阳离子,即该原子对应的阳离子的核外电子数为10。
(1)①$2 + x$ ②<
(2)10[解析]
(1)①在原子中,质子数=核外电子数,则$m = 2 + x$。②阴离子是由原子得到电子形成的,则$m < 2 + x$,即$m - 2 < x$。
(2)相对原子质量≈质子数+中子数,则该原子的质子数为$\frac{23 - 1}{2}=11$,该原子的结构示意图为
 ,易失去1个电子形成阳离子,即该原子对应的阳离子的核外电子数为10。
,易失去1个电子形成阳离子,即该原子对应的阳离子的核外电子数为10。 (1)铁的相对原子质量为
(2)铁原子核内的质子数为
56
(结果保留整数)。(2)铁原子核内的质子数为
26
,核外电子数为26
,中子数为30
。
答案:
(1)56
(2)26 26 30[解析]
(1)根据相对原子质量的定义可得,铁的相对原子质量为$\frac{9.288×10^{-26}kg}{1.993×10^{-26}kg×\frac{1}{12}}\approx 56$。
(2)设铁原子核内的质子数为x,根据相对原子质量≈质子数+中子数,得$x+(x + 4)=56$,解得$x = 26$,即铁原子核内的质子数为26,由于原子中质子数=核外电子数,所以核外电子数为26,中子数为$26 + 4 = 30$。
(1)56
(2)26 26 30[解析]
(1)根据相对原子质量的定义可得,铁的相对原子质量为$\frac{9.288×10^{-26}kg}{1.993×10^{-26}kg×\frac{1}{12}}\approx 56$。
(2)设铁原子核内的质子数为x,根据相对原子质量≈质子数+中子数,得$x+(x + 4)=56$,解得$x = 26$,即铁原子核内的质子数为26,由于原子中质子数=核外电子数,所以核外电子数为26,中子数为$26 + 4 = 30$。
(1)若该粒子带两个单位正电荷,$x$的值为
(2)若该粒子带两个单位负电荷,$x$的值为
(3)若该粒子为原子,$x$的值为
(4)最外层电子数为8的粒子
12
,该粒子符号为$Mg^{2 + }$
。(2)若该粒子带两个单位负电荷,$x$的值为
8
,该粒子符号为$O^{2 - }$
。(3)若该粒子为原子,$x$的值为
10
,其粒子符号为Ne
。(4)最外层电子数为8的粒子
不一定
(填“一定”或“不一定”)是稀有气体的原子。
答案:
(1)12 $Mg^{2 + }$
(2)8 $O^{2 - }$
(3)10 Ne
(4)不一定[解析]
(1)若该粒子带两个单位正电荷,说明该粒子是原子失去2个电子形成的,x的值为$2 + 8 + 2 = 12$;该粒子质子数=12,核外电子数=10,质子数>核外电子数,为镁离子,符号为$Mg^{2 + }$。
(2)若该粒子带两个单位负电荷,说明该粒子是原子得到2个电子形成的,x的值为$2 + 8 - 2 = 8$;该粒子质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,符号为$O^{2 - }$。
(3)原子中,质子数=核外电子数,x的值为$2 + 8 = 10$,为氖原子,符号为Ne。
(4)最外层电子数为8的粒子不一定是稀有气体的原子,也可能是离子。易错警示解题过程中需要注意的是题图中的粒子结构示意图可以表示原子、阳离子或阴离子,然后根据不同的情况进行相关判断。易错警示最外层有8个电子的结构属于相对稳定结构,氦原子的最外层有2个电子,但其原子核外只有一个电子层,故其也具有相对稳定结构。关键点拨质子数=核外电子数的是原子,质子数>核外电子数的是阳离子,质子数<核外电子数的是阴离子。
(1)12 $Mg^{2 + }$
(2)8 $O^{2 - }$
(3)10 Ne
(4)不一定[解析]
(1)若该粒子带两个单位正电荷,说明该粒子是原子失去2个电子形成的,x的值为$2 + 8 + 2 = 12$;该粒子质子数=12,核外电子数=10,质子数>核外电子数,为镁离子,符号为$Mg^{2 + }$。
(2)若该粒子带两个单位负电荷,说明该粒子是原子得到2个电子形成的,x的值为$2 + 8 - 2 = 8$;该粒子质子数=8,核外电子数=10,质子数<核外电子数,为氧离子,符号为$O^{2 - }$。
(3)原子中,质子数=核外电子数,x的值为$2 + 8 = 10$,为氖原子,符号为Ne。
(4)最外层电子数为8的粒子不一定是稀有气体的原子,也可能是离子。易错警示解题过程中需要注意的是题图中的粒子结构示意图可以表示原子、阳离子或阴离子,然后根据不同的情况进行相关判断。易错警示最外层有8个电子的结构属于相对稳定结构,氦原子的最外层有2个电子,但其原子核外只有一个电子层,故其也具有相对稳定结构。关键点拨质子数=核外电子数的是原子,质子数>核外电子数的是阳离子,质子数<核外电子数的是阴离子。
查看更多完整答案,请扫码查看


