第24页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
1[2025山东威海期中]某高尔夫球杆制造公司因错误使用溴丙烷清洗杆头造成多名员工身体不适。已知丙烷分子$(C_3H_8)$中一个氢原子被一个溴原子取代即为溴丙烷,则溴丙烷的相对分子质量应为(
A.95
B.97
C.123
D.155
C
)A.95
B.97
C.123
D.155
答案:
C 【解析】丙烷的化学式为C₃H₈,已知丙烷分子中的一个氢原子被一个溴原子所取代,即为溴丙烷,则溴丙烷的化学式为C₃H₇Br,溴丙烷的相对分子质量应为12×3+1×7+80=123。
2[2024山东济南质检]乙醇的分子结构如图所示,下列叙述正确的是(
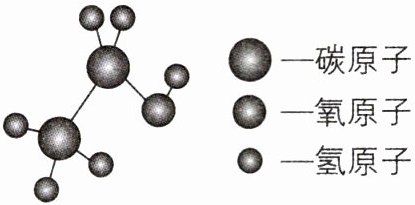
A.乙醇分子是由3种元素组成的化合物
B.一个乙醇分子中含有9个原子
C.乙醇分子中碳、氧元素的质量比为2:1
D.乙醇分子中氧元素的质量分数最大
B
)
A.乙醇分子是由3种元素组成的化合物
B.一个乙醇分子中含有9个原子
C.乙醇分子中碳、氧元素的质量比为2:1
D.乙醇分子中氧元素的质量分数最大
答案:
B 【解析】分子是由原子构成的,物质是由元素组成的,乙醇是由3种元素组成的化合物,A 错误;由图可知,一个乙醇分子中含有9个原子,B 正确;乙醇分子中碳、氧元素的质量比为(12×2):16=3:2,C 错误;乙醇分子中,碳、氢、氧元素的质量比为(12×2):(1×6):16=12:3:8,其中碳元素的质量分数最大,D 错误。
现有$Na_2SO_4、$$Al_2(SO_4)_3、$$MgSO_4$三种固体的混合物,测得其中的氧元素的质量分数为m%,则混合物中金属元素的质量分数为(
A.(100-3m)%
B.(100-m)%
C.(100-1.5m)%
D.(100-0.5m)%
C
)A.(100-3m)%
B.(100-m)%
C.(100-1.5m)%
D.(100-0.5m)%
答案:
C 【解析】该混合物中硫、氧原子个数比是1:4,则其中硫、氧元素质量比为32:(16×4)=1:2,因为氧元素的质量分数为m%,则硫元素的质量分数为0.5m%,所以混合物中金属元素的质量分数为1-m%-0.5m%=(100-1.5m)%。故选 C。
某化合物由碳、氢两种元素组成,其中碳、氢元素的质量比为4:1。若该化合物的相对分子质量为30,则该化合物的化学式为(
$A.CH_3 B.C_2H_6 C.CH_1_8 D.C_4H$
B
)$A.CH_3 B.C_2H_6 C.CH_1_8 D.C_4H$
答案:
B 【解析】设该化合物的化学式为CₓHᵧ。由题意可得{12x:y=4:1,12x+y=30}解得x=2,y=6,因此该化合物的化学式为C₂H₆。
5[2024河南周口期中,中]醋酸的化学式为$CH_3COOH,$某技术员在分析某醋酸溶液中醋酸的含量时,测得溶液中氧元素的质量分数为80%。则100 g该醋酸溶液中,醋酸的质量为(
A.25 g
B.20 g
C.14 g
D.5 g
A
)A.25 g
B.20 g
C.14 g
D.5 g
答案:
A 【解析】设醋酸溶液中水的质量为x,醋酸的质量为y,则水中氧元素的质量为x×(16/18×100%)=8/9x,醋酸中氧元素的质量为y×(16×2)/(12×2+1×4+16×2)×100%=8/15y,溶液中氧元素的质量分数为80%,则(8/9x+8/15y)/(x+y)×100%=80%,解得x/y=3,则该溶液中醋酸的质量为100 g×1/4=25 g。故选 A。
下列说法中,不正确的是(
A.含相等质量铁元素的氧化铁和四氧化三铁的质量比为30:29
B.氯化氢和水的气体混合物10.9 g,其中含氧元素3.2 g,该混合物中氯元素的质量为7.1 g
C.某硝酸铵$(NH_4NO_3)$样品,测知含氮量为37%,该样品中含有的杂质可能是$NH_4HCO_3$
D.在某种氮的氧化物中,若氮元素与氧元素的质量比为7:20,该化合物的化学式为$N_2O_5$
C
)A.含相等质量铁元素的氧化铁和四氧化三铁的质量比为30:29
B.氯化氢和水的气体混合物10.9 g,其中含氧元素3.2 g,该混合物中氯元素的质量为7.1 g
C.某硝酸铵$(NH_4NO_3)$样品,测知含氮量为37%,该样品中含有的杂质可能是$NH_4HCO_3$
D.在某种氮的氧化物中,若氮元素与氧元素的质量比为7:20,该化合物的化学式为$N_2O_5$
答案:
C 【解析】含有相同质量铁元素的氧化铁和四氧化三铁中,铁原子的个数应相等,3Fe₂O₃和2Fe₃O₄中铁原子个数相等,则氧化铁和四氧化三铁的质量比是(3×160):(2×232)=30:29,A 正确;氧元素只存在于水中,氯元素只存在于HCl中,因为水中氢元素与氧元素的质量比为(1×2):16=1:8,若混合物中氧元素的质量为3.2 g,则水中氢元素的质量为3.2 g÷8=0.4 g,氯化氢的质量为10.9 g-3.2 g-0.4 g=7.3 g,所以氯元素的质量为7.3 g×(35.5/(35.5+1)×100%)=7.1 g,B 正确;硝酸铵中,氮元素的质量分数为(14×2)/(14+1×4+14+16×3)×100%=35%,NH₄HCO₃中,氮元素的质量分数为14/(14+1×5+12+16×3)×100%≈17.7%,而该硝酸铵样品中的含氮量为37%,所以该样品中含有杂质不可能是NH₄HCO₃,C 错误;设该氮的氧化物的化学式为NₓOᵧ,则该氧化物中,氮元素与氧元素的质量比为14x/16y=7/20,x/y=2/5,所以该氧化物的化学式为N₂O₅,D 正确。
(1)对乙烯基苯酚的相对分子质量是
(2)y的数值为
(3)24.0 g对乙烯基苯酚中含氧元素的质量为
120
;(2)y的数值为
8
。(3)24.0 g对乙烯基苯酚中含氧元素的质量为
3.2
g。
答案:
(1)120
(2)8
(3)3.2
【解析】
(1)对乙烯基苯酚中,碳元素的质量分数为80%,则对乙烯基苯酚的相对分子质量是(12×8)÷80%=120。
(2)对乙烯基苯酚中,氢、氧两种元素的质量比为1:2,则y:16=1:2,解得y=8。
(3)24.0 g 对乙烯基苯酚中含氧元素的质量为24.0 g×(16/120×100%)=3.2 g。
(1)120
(2)8
(3)3.2
【解析】
(1)对乙烯基苯酚中,碳元素的质量分数为80%,则对乙烯基苯酚的相对分子质量是(12×8)÷80%=120。
(2)对乙烯基苯酚中,氢、氧两种元素的质量比为1:2,则y:16=1:2,解得y=8。
(3)24.0 g 对乙烯基苯酚中含氧元素的质量为24.0 g×(16/120×100%)=3.2 g。
(1)碳酸钙的相对分子质量为
(2)碳酸钙中钙、碳、氧三种元素的原子个数比为
(3)比较两种品牌高钙片中钙的质量分数,品牌甲
(4)如果同为100片装,品牌甲每瓶60元,品牌乙每瓶65元,综合考虑价格和含钙量两个因素,选择品牌
100
。(2)碳酸钙中钙、碳、氧三种元素的原子个数比为
1:1:3
。(3)比较两种品牌高钙片中钙的质量分数,品牌甲
大于
(填“大于”“小于”或“等于”)品牌乙。(4)如果同为100片装,品牌甲每瓶60元,品牌乙每瓶65元,综合考虑价格和含钙量两个因素,选择品牌
甲
(填“甲”或“乙”)更划算,理由是品牌甲含钙量高,价格低
。
答案:
(1)100
(2)1:1:3
(3)大于
(4)甲 品牌甲含钙量高,价格低
【解析】
(1)碳酸钙的化学式为CaCO₃,其相对分子质量为40+12+16×3=100。
(2)碳酸钙中钙、碳、氧三种元素的原子个数比为1:1:3。
(3)品牌甲高钙片中钙的质量分数为(500 mg×10⁻³)/2.5 g×100%=20%,品牌乙高钙片中钙的质量分数为0.75 g/2.5 g×(40/100×100%)=12%,故品牌甲高钙片中钙的质量分数更大。
(4)品牌甲高钙片中钙的质量为100×0.5 g=50 g,品牌乙高钙片中钙的质量为100×2.5 g×12%=30 g,故综合考虑价格和含钙量两个因素,选择品牌甲更划算,因为品牌甲含钙量高,价格低。
(1)100
(2)1:1:3
(3)大于
(4)甲 品牌甲含钙量高,价格低
【解析】
(1)碳酸钙的化学式为CaCO₃,其相对分子质量为40+12+16×3=100。
(2)碳酸钙中钙、碳、氧三种元素的原子个数比为1:1:3。
(3)品牌甲高钙片中钙的质量分数为(500 mg×10⁻³)/2.5 g×100%=20%,品牌乙高钙片中钙的质量分数为0.75 g/2.5 g×(40/100×100%)=12%,故品牌甲高钙片中钙的质量分数更大。
(4)品牌甲高钙片中钙的质量为100×0.5 g=50 g,品牌乙高钙片中钙的质量为100×2.5 g×12%=30 g,故综合考虑价格和含钙量两个因素,选择品牌甲更划算,因为品牌甲含钙量高,价格低。
查看更多完整答案,请扫码查看


