2026年突唯中考中考总复习九年级化学全一册通用版河南专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年突唯中考中考总复习九年级化学全一册通用版河南专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第37页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
考点二$ CO_2$和CO的性质和用途
1. 二氧化碳
(1) 物理性质:无色、无臭的气体,
(2) 化学性质
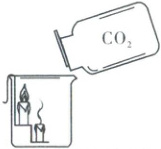
① 不能燃烧也不支持燃烧。如右图所示实验中,下层的蜡烛先熄火。(同时也说明二氧化碳的密度比空气的大)
$CO_2$
② 与水反应的化学方程式为
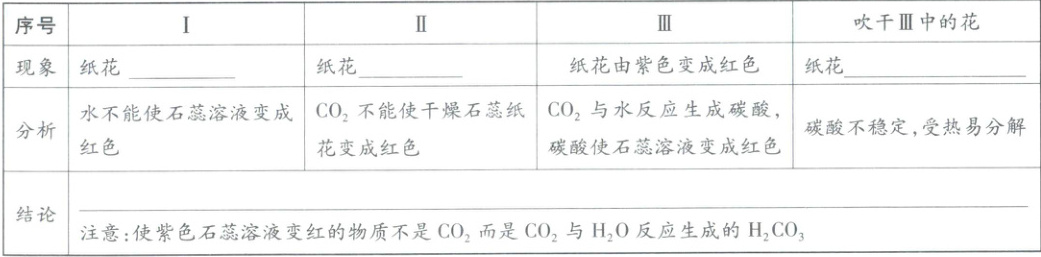
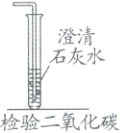
用被石蕊溶液染成紫色的干燥的纸花做如下实验:

③ 与碱溶液的反应:
a. CO_2能使澄清石灰水变浑浊[用来检验CO_2;Ca(OH)_2溶液在空气中变质的反应],化学方程式为
$澄清石灰水 检验二氧化碳$
b. CO_2能与氢氧化钠溶液反应(NaOH在空气中变质的反应),化学方程式为
④ 与碳反应:
⑤ CO_2没有毒性,但不能供给呼吸。
(3) 用途
① 能够与其他物质反应$\longrightarrow$化工原料;
② 能溶于水$\longrightarrow$碳酸饮料;
③ 光合作用$\longrightarrow$
④ 密度比空气大,
⑤ 干冰升华吸热$\longrightarrow$
2. 一氧化碳
(1) 物理性质:无色、无臭的气体,难溶于水,密度比空气略小。
(2) 化学性质
① 可燃性:
② 还原性:
与氧化铜反应
用赤铁矿石(含$Fe_2O_3)$炼铁,化学方程式为
③ 毒性:一氧化碳极易与人体血液中的血红蛋白结合,使血红蛋白不能再与氧气结合,造成人体缺氧,严重时危及生命。因此,冬天在用煤炉取暖时,一定要注意室内通风,防止一氧化碳中毒。
注意:在CO的有关实验中要进行尾气处理,如
(3) 用途:作气体燃料、冶炼金属。
3. CO与$CO_2$的区别与联系
(1) 区别:CO与$CO_2$的化学性质不同(原因为
(2) 联系:在一定条件下,二者可以相互转化,有关反应的化学方程式:
温馨提示
$CO_2$与CO的鉴别与除杂
$(1) CO_2$不是空气污染物,自然界中不可或缺。
(2) 常见的组成元素相同的化合物有CO和$CO_2;$$H_2O$和$H_2O_2$等。它们的化学性质不同,是因为它们的分子构成不同。
$(3) CO_2$与CO的鉴别与除杂。
① 两种气体的鉴别方法。(依据两者的性质差异,且有明显现象发生)
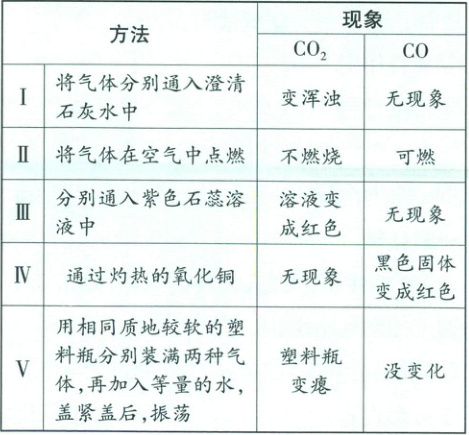

注意:除去$CO_2$中混有的少量CO不能用点燃混合气体的方法。因为$CO_2$不支持燃烧,在$CO_2$存在的条件下,少量的CO不易被点燃,另外$O_2$的量不好把握,在气体除杂时,尽量不选用气体类除杂试剂。
1. 二氧化碳
(1) 物理性质:无色、无臭的气体,
能
溶于水,密度比空气大
。固态二氧化碳叫干冰
,易升华。
(2) 化学性质
① 不能燃烧也不支持燃烧。如右图所示实验中,下层的蜡烛先熄火。(同时也说明二氧化碳的密度比空气的大)
$CO_2$
② 与水反应的化学方程式为
CO₂ + H₂O = H₂CO₃
;碳酸不稳定,受热易分解,化学方程式为H₂CO₃ = CO₂↑ + H₂O
。用被石蕊溶液染成紫色的干燥的纸花做如下实验:



③ 与碱溶液的反应:
a. CO_2能使澄清石灰水变浑浊[用来检验CO_2;Ca(OH)_2溶液在空气中变质的反应],化学方程式为
CO₂ + Ca(OH)₂ = CaCO₃↓ + H₂O
。$澄清石灰水 检验二氧化碳$
b. CO_2能与氢氧化钠溶液反应(NaOH在空气中变质的反应),化学方程式为
2NaOH + CO₂ = Na₂CO₃ + H₂O
。④ 与碳反应:
$CO₂ + C \xlongequal{高温} 2CO$
。⑤ CO_2没有毒性,但不能供给呼吸。
(3) 用途
① 能够与其他物质反应$\longrightarrow$化工原料;
② 能溶于水$\longrightarrow$碳酸饮料;
③ 光合作用$\longrightarrow$
气体肥料
;④ 密度比空气大,
不能燃烧也不支持燃烧
$\longrightarrow$灭火;⑤ 干冰升华吸热$\longrightarrow$
人工增雨
,制冷剂
等。2. 一氧化碳
(1) 物理性质:无色、无臭的气体,难溶于水,密度比空气略小。
(2) 化学性质
① 可燃性:
$2CO + O₂ \xlongequal{点燃} 2CO₂$
(写化学方程式,下同)。② 还原性:
与氧化铜反应
$CuO + CO \xlongequal{△} Cu + CO₂$
;用赤铁矿石(含$Fe_2O_3)$炼铁,化学方程式为
$Fe₂O₃ + 3CO \xlongequal{高温} 2Fe + 3CO₂$
;用磁铁矿石(含$Fe_3O_4)$炼铁,化学方程式为$Fe₃O₄ + 4CO \xlongequal{高温} 3Fe + 4CO₂$
。③ 毒性:一氧化碳极易与人体血液中的血红蛋白结合,使血红蛋白不能再与氧气结合,造成人体缺氧,严重时危及生命。因此,冬天在用煤炉取暖时,一定要注意室内通风,防止一氧化碳中毒。
注意:在CO的有关实验中要进行尾气处理,如
点燃
或用气球收集
集中处理。(3) 用途:作气体燃料、冶炼金属。
3. CO与$CO_2$的区别与联系
(1) 区别:CO与$CO_2$的化学性质不同(原因为
分子构成不同
);(2) 联系:在一定条件下,二者可以相互转化,有关反应的化学方程式:
$2CO + O₂ \xlongequal{点燃} 2CO₂$
;$CO₂ + C \xlongequal{高温} 2CO$
。温馨提示
$CO_2$与CO的鉴别与除杂
$(1) CO_2$不是空气污染物,自然界中不可或缺。
(2) 常见的组成元素相同的化合物有CO和$CO_2;$$H_2O$和$H_2O_2$等。它们的化学性质不同,是因为它们的分子构成不同。
$(3) CO_2$与CO的鉴别与除杂。
① 两种气体的鉴别方法。(依据两者的性质差异,且有明显现象发生)


注意:除去$CO_2$中混有的少量CO不能用点燃混合气体的方法。因为$CO_2$不支持燃烧,在$CO_2$存在的条件下,少量的CO不易被点燃,另外$O_2$的量不好把握,在气体除杂时,尽量不选用气体类除杂试剂。
答案:
考点二
1:
(1)能 大 干冰
(2)②CO₂ + H₂O = H₂CO₃ H₂CO₃ = CO₂↑ + H₂O
不变色 不变色 由红色变成紫色
二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变成红色;碳酸不稳定,受热易分解成CO₂和H₂O
③a. CO₂ + Ca(OH)₂ = CaCO₃↓ + H₂O
b. 2NaOH + CO₂ = Na₂CO₃ + H₂O
$④CO₂ + C \xlongequal{高温} 2CO$
(3)③气体肥料 ④不能燃烧也不支持燃烧 ⑤人工增雨 制冷剂
2:$(2)①2CO + O₂ \xlongequal{点燃} 2CO₂ ②CuO + CO \xlongequal{△} Cu + CO₂$
$Fe₂O₃ + 3CO \xlongequal{高温} 2Fe + 3CO₂ Fe₃O₄ + 4CO \xlongequal{高温} 3Fe + 4CO₂$
注意:点燃 用气球收集
3:
(1)分子构成不同
$(2)2CO + O₂ \xlongequal{点燃} 2CO₂ CO₂ + C \xlongequal{高温} 2CO$
1:
(1)能 大 干冰
(2)②CO₂ + H₂O = H₂CO₃ H₂CO₃ = CO₂↑ + H₂O
不变色 不变色 由红色变成紫色
二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变成红色;碳酸不稳定,受热易分解成CO₂和H₂O
③a. CO₂ + Ca(OH)₂ = CaCO₃↓ + H₂O
b. 2NaOH + CO₂ = Na₂CO₃ + H₂O
$④CO₂ + C \xlongequal{高温} 2CO$
(3)③气体肥料 ④不能燃烧也不支持燃烧 ⑤人工增雨 制冷剂
2:$(2)①2CO + O₂ \xlongequal{点燃} 2CO₂ ②CuO + CO \xlongequal{△} Cu + CO₂$
$Fe₂O₃ + 3CO \xlongequal{高温} 2Fe + 3CO₂ Fe₃O₄ + 4CO \xlongequal{高温} 3Fe + 4CO₂$
注意:点燃 用气球收集
3:
(1)分子构成不同
$(2)2CO + O₂ \xlongequal{点燃} 2CO₂ CO₂ + C \xlongequal{高温} 2CO$
查看更多完整答案,请扫码查看


