2025年零失误分层训练高中化学必修第二册人教版黑吉辽内蒙古专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年零失误分层训练高中化学必修第二册人教版黑吉辽内蒙古专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第42页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
9.【题型二、三】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1) 下图为氢氧燃料电池的构造示意图,由此判断X极为电池的

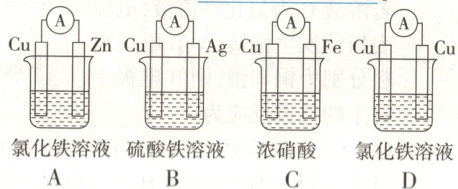
(2) 为了验证${Fe^3+}$与${Cu^2+}$氧化性强弱,设计一个实验装置,下列装置既能产生电流又能达到实验目的的是 。
(1) 下图为氢氧燃料电池的构造示意图,由此判断X极为电池的
负
极,${OH^-}$向负
(填“正”或“负”)极做定向移动,Y极的电极反应式为$O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$
,电路中每转移$0.2\ {mol}$电子,标准状况下正极上消耗气体的体积是1.12
${L}$。
(2) 为了验证${Fe^3+}$与${Cu^2+}$氧化性强弱,设计一个实验装置,下列装置既能产生电流又能达到实验目的的是 。

答案:
9.
(1)负 $O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$
(2)B[提示:
(1)$H_2$作还原剂,是负极,$X$极为电池的负极,$OH^-$向负极做定向移动,$O_2$得电子,是正极,$Y$极的电极反应式为$O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$,电路中每转移$0.2mol$电子,标准状况下正极上消耗气体的体积是$0.2mol×\frac{22.4L· mol^{-1}}{4}=1.12L$。
(2)锌较活泼,能与$Fe^{3+}$反应,能形成原电池,但是不能证明$Fe^{3+}$与$Cu^{2+}$氧化性强弱,A错误;$Fe^{3+}$与$Cu$反应,能形成原电池,也能验证$Fe^{3+}$与$Cu^{2+}$氧化性强弱,B正确;铁遇到浓硝酸后钝化,$Cu$作负极,能形成原电池,但是不能证明$Fe^{3+}$与$Cu^{2+}$氧化性强弱,C错误;两电极相同,不能形成原电池,D错误。]
(1)负 $O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$
(2)B[提示:
(1)$H_2$作还原剂,是负极,$X$极为电池的负极,$OH^-$向负极做定向移动,$O_2$得电子,是正极,$Y$极的电极反应式为$O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$,电路中每转移$0.2mol$电子,标准状况下正极上消耗气体的体积是$0.2mol×\frac{22.4L· mol^{-1}}{4}=1.12L$。
(2)锌较活泼,能与$Fe^{3+}$反应,能形成原电池,但是不能证明$Fe^{3+}$与$Cu^{2+}$氧化性强弱,A错误;$Fe^{3+}$与$Cu$反应,能形成原电池,也能验证$Fe^{3+}$与$Cu^{2+}$氧化性强弱,B正确;铁遇到浓硝酸后钝化,$Cu$作负极,能形成原电池,但是不能证明$Fe^{3+}$与$Cu^{2+}$氧化性强弱,C错误;两电极相同,不能形成原电池,D错误。]
1. 肼(${N2H4}$)-空气燃料电池是一种环保型碱性燃料电池,电解质溶液是$20\%\sim30\%$的${KOH}$溶液。电池总反应为${N2H4 + O2 \xlongequal{} N2 + 2H2O}$。下列关于该燃料电池工作时的说法正确的是 (
A.负极的电极反应式为${N2H4 + 4OH^- + 4e^- \xlongequal{} 4H2O + N2}$
B.正极的电极反应式为${O2 + 4H^+ + 4e^- \xlongequal{} 2H2O}$
C.溶液中阴离子向负极移动
D.溶液中$c({OH^-})$保持不变
C
)A.负极的电极反应式为${N2H4 + 4OH^- + 4e^- \xlongequal{} 4H2O + N2}$
B.正极的电极反应式为${O2 + 4H^+ + 4e^- \xlongequal{} 2H2O}$
C.溶液中阴离子向负极移动
D.溶液中$c({OH^-})$保持不变
答案:
1.C[提示:原电池中负极发生氧化反应,碱性条件下负极的电极反应式为$N_2H_4 + 4OH^- - 4e^-\xlongequal\ 4H_2O + N_2$,A项错误;在碱性条件下,正极的电极反应式为$O_2 + 2H_2O + 4e^-\xlongequal\ 4OH^-$,B项错误;原电池工作时,阴离子向负极移动,C项正确;电池的总反应方程式为$N_2H_4 + O_2\xlongequal\ N_2 + 2H_2O$,反应生成水,$c(OH^-)$减小,D项错误。]
2. 减排是各个国家都在为之努力的事,${CO2}$和${SO2}$的处理是许多科学家都在着力研究的重要。有学者想以如图所示装置利用原电池原理将${CO2}$、${SO2}$转化为重要的化工原料。

(1) 若A为${CO2}$,B为${H2}$,C为${CH3OH}$,电池总反应式为${CO2 + 3H2 \xlongequal{} CH3OH + H2O}$,则正极的电极反应式为
(2) 若A为${SO2}$,B为${O2}$,C为${H2SO4}$,则负极的电极反应式为

(1) 若A为${CO2}$,B为${H2}$,C为${CH3OH}$,电池总反应式为${CO2 + 3H2 \xlongequal{} CH3OH + H2O}$,则正极的电极反应式为
$CO_2 + 6H^+ + 6e^-\xlongequal\ CH_3OH + H_2O$
。(2) 若A为${SO2}$,B为${O2}$,C为${H2SO4}$,则负极的电极反应式为
$SO_2 + 2H_2O - 2e^-\xlongequal\ SO_4^{2-} + 4H^+$
,电池的总反应为$2SO_2 + O_2 + 2H_2O\xlongequal\ 2H_2SO_4$
。
答案:
2.
(1)$CO_2 + 6H^+ + 6e^-\xlongequal\ CH_3OH + H_2O$
(2)$SO_2 + 2H_2O - 2e^-\xlongequal\ SO_4^{2-} + 4H^+$ $2SO_2 + O_2 + 2H_2O\xlongequal\ 2H_2SO_4$[提示:
(1)$H_2$在负极失去电子,酸性条件下该电池负极的电极反应式为$H_2 - 2e^-\xlongequal\ 2H^+$,$CO_2$在正极上得到电子,一分子$CO_2$得到6个电子,转化为$CH_3OH$,故可得正极的电极反应式为$CO_2 + 6H^+ + 6e^-\xlongequal\ CH_3OH + H_2O$。
(2)$SO_2$在负极失去电子,可得负极的电极反应式为$SO_2 + 2H_2O - 2e^-\xlongequal\ SO_4^{2-} + 4H^+$。$O_2$在正极上获得电子,可得正极的电极反应式为$O_2 + 4H^+ + 4e^-\xlongequal\ 2H_2O$,使正、负极得失电子总数相等并将正、负极电极反应式相加,可得电池的总反应式为$2SO_2 + O_2 + 2H_2O\xlongequal\ 2H_2SO_4$。]
(1)$CO_2 + 6H^+ + 6e^-\xlongequal\ CH_3OH + H_2O$
(2)$SO_2 + 2H_2O - 2e^-\xlongequal\ SO_4^{2-} + 4H^+$ $2SO_2 + O_2 + 2H_2O\xlongequal\ 2H_2SO_4$[提示:
(1)$H_2$在负极失去电子,酸性条件下该电池负极的电极反应式为$H_2 - 2e^-\xlongequal\ 2H^+$,$CO_2$在正极上得到电子,一分子$CO_2$得到6个电子,转化为$CH_3OH$,故可得正极的电极反应式为$CO_2 + 6H^+ + 6e^-\xlongequal\ CH_3OH + H_2O$。
(2)$SO_2$在负极失去电子,可得负极的电极反应式为$SO_2 + 2H_2O - 2e^-\xlongequal\ SO_4^{2-} + 4H^+$。$O_2$在正极上获得电子,可得正极的电极反应式为$O_2 + 4H^+ + 4e^-\xlongequal\ 2H_2O$,使正、负极得失电子总数相等并将正、负极电极反应式相加,可得电池的总反应式为$2SO_2 + O_2 + 2H_2O\xlongequal\ 2H_2SO_4$。]
查看更多完整答案,请扫码查看


