第83页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
1.理解悟透相关原理和定律对于化学学习非常重要。下列说法正确的是 (
A.所有变化都遵守质量守恒定律
B.电解一段时间后水的质量减小,不能用质量守恒定律解释
C.1 g硫在2 g氧气中充分燃烧可以生成3 g二氧化硫
D.在化学反应中,各物质的质量之比不一定等于其相对分子质量之比
D
)A.所有变化都遵守质量守恒定律
B.电解一段时间后水的质量减小,不能用质量守恒定律解释
C.1 g硫在2 g氧气中充分燃烧可以生成3 g二氧化硫
D.在化学反应中,各物质的质量之比不一定等于其相对分子质量之比
答案:
D
2.如图是兴趣小组设计的验证质量守恒定律的实验,下列说法错误的是 (
 A.实验一中气球的作用是隔绝空气、缓冲压强,铜粉用量不影响实验结果
A.实验一中气球的作用是隔绝空气、缓冲压强,铜粉用量不影响实验结果
B.实验二反应后,天平仍保持平衡(忽略浮力的影响)
C.实验三、四不能用于验证质量守恒定律的原因相同
D.实验四中若将蜡烛置于密闭容器中点燃,可用于验证质量守恒定律
C
)  A.实验一中气球的作用是隔绝空气、缓冲压强,铜粉用量不影响实验结果
A.实验一中气球的作用是隔绝空气、缓冲压强,铜粉用量不影响实验结果B.实验二反应后,天平仍保持平衡(忽略浮力的影响)
C.实验三、四不能用于验证质量守恒定律的原因相同
D.实验四中若将蜡烛置于密闭容器中点燃,可用于验证质量守恒定律
答案:
C
3.(2024秋漳州期末)氢化钠(NaH)与水反应放出氢气并生成另一种物质,该物质可能是 (
A.Na2CO3
B.NaOH
C.H2O
D.CO2
B
)A.Na2CO3
B.NaOH
C.H2O
D.CO2
答案:
B
4.(2024秋重庆期末)雕花玻璃是利用氢氟酸(HF)对玻璃的腐蚀作用制成的,原理是$SiO_2+4HF= X↑+2H_2O,$下列说法错误的是 (
A.X的化学式为$SiF_4$
B.X在常温常压下为气态
C.反应前后元素的种类不变
D.该反应中$SiO_2$和$H_2O$的质量比为10:3
D
)A.X的化学式为$SiF_4$
B.X在常温常压下为气态
C.反应前后元素的种类不变
D.该反应中$SiO_2$和$H_2O$的质量比为10:3
答案:
D
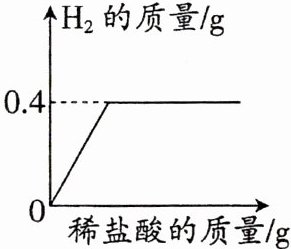
5.为测定某铜、锌混合粉末中锌的质量分数,化学小组取20 g该混合粉末于烧杯中,向其中逐滴加入稀盐酸,产生氢气的质量与加入稀盐酸的质量关系如图。计算该混合粉末中锌的质量分数。
(已知$:Zn+2HCl= ZnCl_2+H_2↑,$铜与稀盐酸不发生反应)
]
(已知$:Zn+2HCl= ZnCl_2+H_2↑,$铜与稀盐酸不发生反应)
]

答案:
解:设20 g该混合粉末中锌的质量为x。${Zn + 2HCl\xlongequal{}ZnCl_{2} + H_{2}\uparrow }$65 2x 0.4 g$\frac{65}{2}=\frac{x}{0.4\ g},x=13\ g$该混合粉末中锌的质量分数为$\frac{13\ g}{20\ g}×100\% = 65\%$答:该混合粉末中锌的质量分数为65%。
查看更多完整答案,请扫码查看


