2025年同步作业本练闯考九年级化学下册人教版安徽专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步作业本练闯考九年级化学下册人教版安徽专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第31页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1.(2024·庐阳区校级模拟)“硝花”是硫酸钠结晶在盐板上的一种现象。兴趣小组自制“硝花”的实验如图,下面分析正确的一项是 ( )
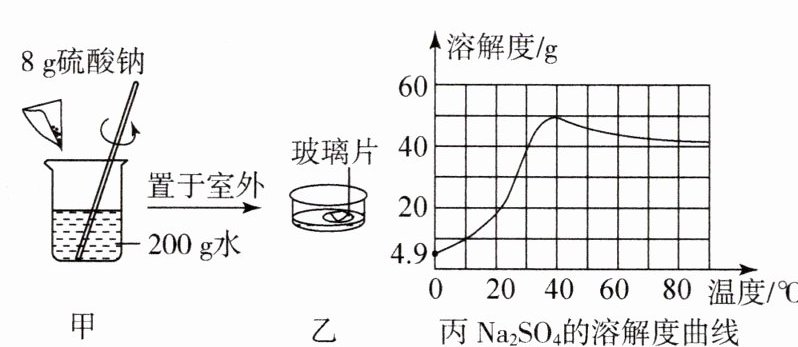
A.图甲中搅拌可以增大$Na_2SO_4$的溶解度
B.图甲所得溶液的溶质质量分数为4%
C.图乙中气温下降到0 ℃有“硝花”析出
D.40 ℃的饱和$Na_2SO_4$溶液降温或升温都会有晶体析出

A.图甲中搅拌可以增大$Na_2SO_4$的溶解度
B.图甲所得溶液的溶质质量分数为4%
C.图乙中气温下降到0 ℃有“硝花”析出
D.40 ℃的饱和$Na_2SO_4$溶液降温或升温都会有晶体析出
答案:
D
2.如图所示为$Ca(OH)_2$和$CO_2$的溶解度曲线,下列说法正确的是 ( )
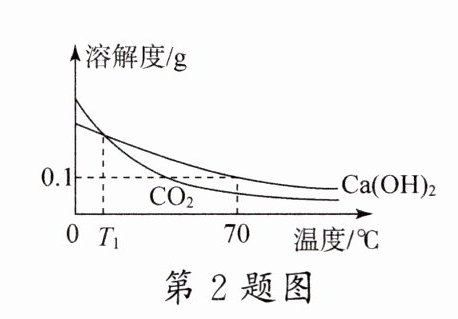
A.$CO_2$的溶解度比$Ca(OH)_2$的溶解度大
B.人在喝碳酸饮料时会打隔是因为二氧化碳的溶解度随温度升高而减小
C.将70 ℃时等质量的$CO_2$和$Ca(OH)_2$饱和溶液降温到$T_1℃$,所得溶液中溶质的质量相等
D.70 ℃时,在1 kg水中加入1.5 g氢氧化钙固体能得到澄清石灰水

A.$CO_2$的溶解度比$Ca(OH)_2$的溶解度大
B.人在喝碳酸饮料时会打隔是因为二氧化碳的溶解度随温度升高而减小
C.将70 ℃时等质量的$CO_2$和$Ca(OH)_2$饱和溶液降温到$T_1℃$,所得溶液中溶质的质量相等
D.70 ℃时,在1 kg水中加入1.5 g氢氧化钙固体能得到澄清石灰水
答案:
B
3.(2024·合肥三模)将34 g晶体W(不含结晶水)投入盛有16 g不同温度水的烧杯中(忽略溶解吸热、放热),充分溶解,测得0 ℃、$t_1℃$、$t_2℃$、$t_3℃$的烧杯中溶液的质量分别如图中a、b、c、d点所示。下列说法错误的是 ( )
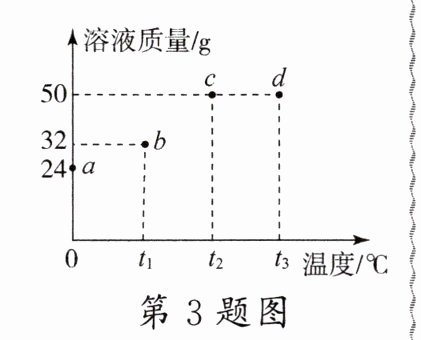
A.在0~$t_2℃$范围内,晶体W溶解度随温度升高而增大
B.$t_1℃$时,晶体W的溶解度是100 g
C.a、b、c、d四点所对应的溶液中,属于饱和溶液的是b、c
D.b、c两点对应的溶液中,溶质质量分数较大的是c

A.在0~$t_2℃$范围内,晶体W溶解度随温度升高而增大
B.$t_1℃$时,晶体W的溶解度是100 g
C.a、b、c、d四点所对应的溶液中,属于饱和溶液的是b、c
D.b、c两点对应的溶液中,溶质质量分数较大的是c
答案:
C
4.硝土中含有硝酸镁、硝酸钙、氯化钠等物质,草木灰的主要成分是碳酸钾,民间曾用硝土和草木灰作原料来制取硝酸钾,其主要生产流程如图甲;某课外小组模仿该生产流程在实验室进行实验,请回答有关问题:
(1)草木灰属于____________(填“纯净物”或“混合物”)。
(2)步骤①中发生反应的化学方程式:$Mg(NO_3)_2+K_2CO_3=X\downarrow+2KNO_3$,则X的化学式为__________。
(3)操作a的名称是________。操作a中需要用到的玻璃仪器有烧杯、____________________。
(4)从图乙可知,氯化钠的溶解度受温度变化影响________,在获得氯化钠晶体时应采取______________的方法,而硝酸钾的溶解度随温度改变变化________,采取______________方法获得硝酸钾晶体更为方便。
(5)步骤④中滤液可重复使用的理由是________。
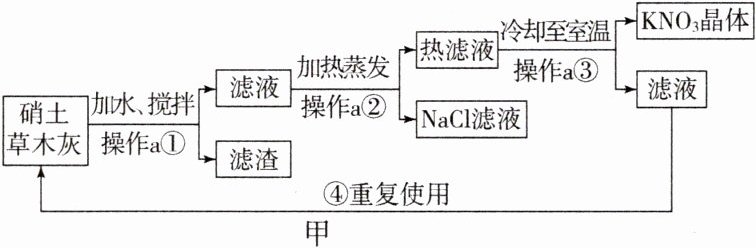
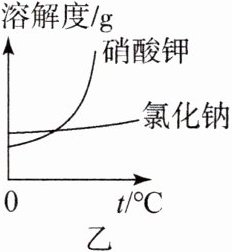
(1)草木灰属于____________(填“纯净物”或“混合物”)。
(2)步骤①中发生反应的化学方程式:$Mg(NO_3)_2+K_2CO_3=X\downarrow+2KNO_3$,则X的化学式为__________。
(3)操作a的名称是________。操作a中需要用到的玻璃仪器有烧杯、____________________。
(4)从图乙可知,氯化钠的溶解度受温度变化影响________,在获得氯化钠晶体时应采取______________的方法,而硝酸钾的溶解度随温度改变变化________,采取______________方法获得硝酸钾晶体更为方便。
(5)步骤④中滤液可重复使用的理由是________。


答案:
(1)混合物
(2)$MgCO_{3}$
(3)过滤;漏斗;玻璃棒
(4)较小;蒸发结晶;较大;降温结晶(或冷却热饱和溶液)
(5)滤液中含有较多的$K_{2}CO_{3}$(或重复利用滤液中的$K_{2}CO_{3}$,节约原料,合理即可)
(1)混合物
(2)$MgCO_{3}$
(3)过滤;漏斗;玻璃棒
(4)较小;蒸发结晶;较大;降温结晶(或冷却热饱和溶液)
(5)滤液中含有较多的$K_{2}CO_{3}$(或重复利用滤液中的$K_{2}CO_{3}$,节约原料,合理即可)
查看更多完整答案,请扫码查看


