第7页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
10. 将50 g 12%的氯化钠溶液和100 g 9%的氯化钠溶液混合。
(1)混合后溶液的溶质质量分数是______。
(2)将上述溶液均分成三份。
① 取其中一份,使溶质质量分数增大1倍,需要加入______g氯化钠。
② 取其中一份,使溶质质量分数增大1倍,需要蒸发______g水。
③ 取其中一份,使溶质质量分数增大1倍,需要加入______g溶质质量分数为30%的氯化钠溶液。
(1)混合后溶液的溶质质量分数是______。
(2)将上述溶液均分成三份。
① 取其中一份,使溶质质量分数增大1倍,需要加入______g氯化钠。
② 取其中一份,使溶质质量分数增大1倍,需要蒸发______g水。
③ 取其中一份,使溶质质量分数增大1倍,需要加入______g溶质质量分数为30%的氯化钠溶液。
答案:
(1) 10%
(2) ① 6.25 ② 25 ③ 50 解析:
(1) 将50 g 12%的氯化钠溶液和100 g 9%的氯化钠溶液混合,所得溶液的溶质质量分数为$\frac{50g×12\% + 100g×9\%}{50g + 100g}×100\% = 10\%$。
(2) 溶液具有均一性,若将溶液均分成三份,每一份的质量为$\frac{50g + 100g}{3} = 50g$,其中溶质质量为$\frac{50g×12\% + 100g×9\%}{3} = 5g$,每一份的溶质质量分数均为10%。① 设需要加入氯化钠的质量为x,则$\frac{5g + x}{50g + x}×100\% = 10\%×2$,$x = 6.25g$。② 设需要蒸发水的质量为y,则$\frac{5g}{50g - y}×100\% = 10\%×2$,$y = 25g$。③ 设需要加入溶质质量分数为30%的氯化钠溶液的质量为z,则$\frac{5g + z×30\%}{50g + z}×100\% = 10\%×2$,$z = 50g$。
(1) 10%
(2) ① 6.25 ② 25 ③ 50 解析:
(1) 将50 g 12%的氯化钠溶液和100 g 9%的氯化钠溶液混合,所得溶液的溶质质量分数为$\frac{50g×12\% + 100g×9\%}{50g + 100g}×100\% = 10\%$。
(2) 溶液具有均一性,若将溶液均分成三份,每一份的质量为$\frac{50g + 100g}{3} = 50g$,其中溶质质量为$\frac{50g×12\% + 100g×9\%}{3} = 5g$,每一份的溶质质量分数均为10%。① 设需要加入氯化钠的质量为x,则$\frac{5g + x}{50g + x}×100\% = 10\%×2$,$x = 6.25g$。② 设需要蒸发水的质量为y,则$\frac{5g}{50g - y}×100\% = 10\%×2$,$y = 25g$。③ 设需要加入溶质质量分数为30%的氯化钠溶液的质量为z,则$\frac{5g + z×30\%}{50g + z}×100\% = 10\%×2$,$z = 50g$。
11. 硫氧粉(Na₂SO₃)可用作脱氧剂,常因氧化而变质生成Na₂SO₄。向20 g可能被氧化的样品中加入溶质质量分数为10%的稀硫酸至恰好不再产生气泡(假设气体全部逸出),消耗98 g稀硫酸。(已知:Na₂SO₃+H₂SO₄=Na₂SO₄+SO₂↑+H₂O)
(1)根据化学式判断Na₂SO₄和Na₂SO₃中钠元素的质量分数较小的是______。
(2)若用5 g溶质质量分数为98%的浓硫酸配制10%的稀硫酸,所需水的质量为______。
(3)求反应后溶液中溶质的质量分数。(结果精确到0.1%)
(1)根据化学式判断Na₂SO₄和Na₂SO₃中钠元素的质量分数较小的是______。
(2)若用5 g溶质质量分数为98%的浓硫酸配制10%的稀硫酸,所需水的质量为______。
(3)求反应后溶液中溶质的质量分数。(结果精确到0.1%)
答案:
(1) $Na_2SO_4$
(2) 44 g
(3) 解:设反应生成硫酸钠的质量为x,生成二氧化硫的质量为y,消耗亚硫酸钠的质量为z。
$Na_2SO_3 + H_2SO_4 = Na_2SO_4 + SO_2↑ + H_2O$
126 98 142 64
z $98g×10\%$ x y
$\frac{98}{142} = \frac{98g×10\%}{x}$ $x = 14.2g$
$\frac{98}{64} = \frac{98g×10\%}{y}$ $y = 6.4g$
$\frac{126}{98} = \frac{z}{98g×10\%}$ $z = 12.6g$
则反应后溶液中溶质的质量分数为$\frac{(20g - 12.6g) + 14.2g}{20g + 98g - 6.4g}×100\% ≈ 19.4\%$。
答:反应后溶液中溶质的质量分数约为19.4%。
解析:
(2) 溶液稀释前后溶质的质量不变,设需要水的质量为a,则有$5g×98\% = (5g + a)×10\%$,解得$a = 44g$。
(1) $Na_2SO_4$
(2) 44 g
(3) 解:设反应生成硫酸钠的质量为x,生成二氧化硫的质量为y,消耗亚硫酸钠的质量为z。
$Na_2SO_3 + H_2SO_4 = Na_2SO_4 + SO_2↑ + H_2O$
126 98 142 64
z $98g×10\%$ x y
$\frac{98}{142} = \frac{98g×10\%}{x}$ $x = 14.2g$
$\frac{98}{64} = \frac{98g×10\%}{y}$ $y = 6.4g$
$\frac{126}{98} = \frac{z}{98g×10\%}$ $z = 12.6g$
则反应后溶液中溶质的质量分数为$\frac{(20g - 12.6g) + 14.2g}{20g + 98g - 6.4g}×100\% ≈ 19.4\%$。
答:反应后溶液中溶质的质量分数约为19.4%。
解析:
(2) 溶液稀释前后溶质的质量不变,设需要水的质量为a,则有$5g×98\% = (5g + a)×10\%$,解得$a = 44g$。
12. 乙醇(C₂H₅OH)的某种水溶液,溶质和溶剂中氢元素对应的原子个数相等,则该溶液中溶质的质量分数为( )
A. 23%
B. 46%
C. 55%
D. 72%
A. 23%
B. 46%
C. 55%
D. 72%
答案:
B 解析:乙醇溶液中溶质的质量分数为$\frac{乙醇的质量}{乙醇的质量 + 水的质量}×100\%$,因此需要判断溶质乙醇与溶剂水的质量关系。每个乙醇($C_2H_5OH$)分子中含6个氢原子,每个水($H_2O$)分子中含2个氢原子,根据溶质和溶剂中氢元素对应的原子个数相等可推算溶液中乙醇与水的质量关系:$C_2H_5OH ~ 6H ~ 3H_2O$,此乙醇溶液中溶质的质量分数为$\frac{46}{46 + 54}×100\% = 46\%$。
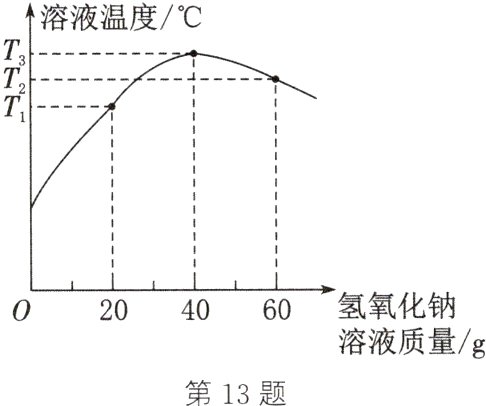
13. 化学小组同学参与“铅蓄废电池中硫酸回收”的研究项目,回收时需要测定电池废液中硫酸的质量分数。向装有50 g废液的锥形瓶中加入溶质质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等电子设备采集信息并绘制成右图,请据图回答相关问题。(化学方程式是2NaOH+H₂SO₄=Na₂SO₄+2H₂O,杂质可溶但不参加反应)
(1)该反应是______(填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为______℃。
(3)计算废液中硫酸的质量分数。(写出计算过程)
(1)该反应是______(填“吸热”或“放热”)反应。
(2)恰好完全反应时,溶液的温度为______℃。
(3)计算废液中硫酸的质量分数。(写出计算过程)

答案:
(1) 放热
(2) $T_3$
(3) 解:设50 g废液中硫酸的质量为x。
$2NaOH + H_2SO_4 = Na_2SO_4 + 2H_2O$
80 98
$40g×20\%$ x
$\frac{80}{98} = \frac{40g×20\%}{x}$ $x = 9.8g$
废液中硫酸的质量分数为$\frac{9.8g}{50g}×100\% = 19.6\%$。
答:废液中硫酸的质量分数为19.6%。
(1) 放热
(2) $T_3$
(3) 解:设50 g废液中硫酸的质量为x。
$2NaOH + H_2SO_4 = Na_2SO_4 + 2H_2O$
80 98
$40g×20\%$ x
$\frac{80}{98} = \frac{40g×20\%}{x}$ $x = 9.8g$
废液中硫酸的质量分数为$\frac{9.8g}{50g}×100\% = 19.6\%$。
答:废液中硫酸的质量分数为19.6%。
查看更多完整答案,请扫码查看


