第41页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
10.(2024·大庆)下列分类正确的是( )
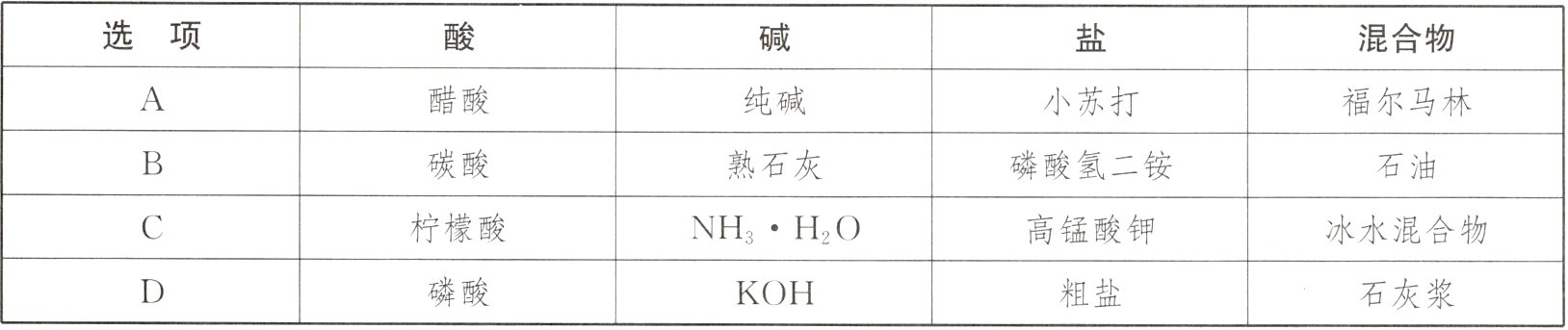

答案:
B
11. 除去下列物质中所含的少量杂质(括号内为杂质),所用试剂和方法正确的是( )
A. O₂(N₂):通过灼热的铜网
B. CO₂(CO):通入氧气后点燃
C. FeSO₄溶液(CuSO₄):加入过量的铁粉,过滤
D. NaCl溶液(Na₂SO₄):加入过量的BaCl₂溶液,过滤
A. O₂(N₂):通过灼热的铜网
B. CO₂(CO):通入氧气后点燃
C. FeSO₄溶液(CuSO₄):加入过量的铁粉,过滤
D. NaCl溶液(Na₂SO₄):加入过量的BaCl₂溶液,过滤
答案:
C
12.(2024·齐齐哈尔)将一定质量的铁粉放入硝酸锌和硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液。下列说法正确的是( )
A. 若滤液呈浅绿色,则滤液中只含有硝酸亚铁
B. 若滤渣中的成分能被磁铁吸引,则滤渣中一定含有两种金属
C. 若向滤液中加入锌片,有固体析出,则滤液中一定含有硝酸银
D. 将所得滤渣洗涤、干燥后称量,质量可能与所加铁粉的质量相等
A. 若滤液呈浅绿色,则滤液中只含有硝酸亚铁
B. 若滤渣中的成分能被磁铁吸引,则滤渣中一定含有两种金属
C. 若向滤液中加入锌片,有固体析出,则滤液中一定含有硝酸银
D. 将所得滤渣洗涤、干燥后称量,质量可能与所加铁粉的质量相等
答案:
B 解析:金属活动性的强弱顺序为锌>铁>银,铁不能和硝酸锌反应,铁和硝酸银反应生成硝酸亚铁和银,锌和硝酸亚铁反应生成铁和硝酸锌。若滤液呈浅绿色,则滤液中一定含有生成的硝酸亚铁和不参与反应的硝酸锌,A不正确。若滤渣中的成分能被磁铁吸引,则滤渣中还有铁,所以滤渣中一定含有银和铁两种金属,B正确。若向滤液中加入锌片,有固体析出,不能说明滤液中一定含有硝酸银,因为滤液中一定有生成的硝酸亚铁,析出的固体可能是锌和硝酸亚铁反应生成的铁,C不正确。由反应Fe + 2AgNO₃ = Fe(NO₃)₂ + 2Ag可知,每56份质量的铁完全反应能置换出216份质量的银,反应后固体质量变大,所以将所得滤渣洗涤、干燥后称量,质量一定大于所加铁粉的质量,D不正确。
13.(2024·临夏改编)浩如烟海的中国古代典籍中记录了许多化学知识,展示了中国古代人民的智慧。西汉古籍《淮南万毕术》中有“曾青得铁则化为铜”这样的记载,从而实现“铁上包铜”,防止铁的锈蚀。其反应的微观示意图如图所示,该反应过程中发生变化的微观粒子是____________。


答案:
铁原子和铜离子
14.(2024·河南)金属与人类的生活密切相关。回答下列有关金属性质的问题。
(1)铝较为活泼,铝制品却很耐腐蚀,原因是______________________________。
(2)现将过量的锌粉加入AgNO₃和Mg(NO₃)₂的混合溶液中,充分反应后,过滤。过滤后留在滤纸上的固体是________。请写出有关反应的化学方程式:________________________。
(1)铝较为活泼,铝制品却很耐腐蚀,原因是______________________________。
(2)现将过量的锌粉加入AgNO₃和Mg(NO₃)₂的混合溶液中,充分反应后,过滤。过滤后留在滤纸上的固体是________。请写出有关反应的化学方程式:________________________。
答案:
(1)铝与氧气反应,其表面生成致密的氧化铝薄膜 (2)银和锌 Zn + 2AgNO₃ = Zn(NO₃)₂ + 2Ag
15.(2024·龙东地区改编)金属材料在人类发展的历史长河中起着非常重要的作用。
(1)探究Mg、Fe、Cu的金属活动性顺序,下列试剂的选择方案正确的是________(填字母)。
A. Mg、Cu、FeSO₄溶液 B. Fe、MgSO₄溶液、CuSO₄溶液
C. Mg、Fe、Cu、稀盐酸 D. Cu、MgSO₄溶液、FeSO₄溶液
(2)向Cu(NO₃)₂溶液中加入Mg、Zn、Ag三种金属,充分反应后过滤,得到无色滤液和滤渣。一定发生反应的化学方程式为______________________________。向滤渣中加入一定量的稀盐酸,有气泡产生,滤渣中一定有________________(填化学式,下同),滤液中可能含有的溶质是________________。
(1)探究Mg、Fe、Cu的金属活动性顺序,下列试剂的选择方案正确的是________(填字母)。
A. Mg、Cu、FeSO₄溶液 B. Fe、MgSO₄溶液、CuSO₄溶液
C. Mg、Fe、Cu、稀盐酸 D. Cu、MgSO₄溶液、FeSO₄溶液
(2)向Cu(NO₃)₂溶液中加入Mg、Zn、Ag三种金属,充分反应后过滤,得到无色滤液和滤渣。一定发生反应的化学方程式为______________________________。向滤渣中加入一定量的稀盐酸,有气泡产生,滤渣中一定有________________(填化学式,下同),滤液中可能含有的溶质是________________。
答案:
(1)ABC (2)Mg + Cu(NO₃)₂ = Cu + Mg(NO₃)₂ Ag、Cu、Zn Zn(NO₃)₂ 解析:(1)根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“活泼置换不活泼”进行分析判断,通过分析方案所能得到的结论,确定是否能得出Mg、Fe、Cu三种金属的活动性顺序。镁与FeSO₄溶液反应置换出铁,说明了活动性:镁>铁;铜与FeSO₄溶液不反应,说明了活动性:铁>铜,由此可得出三种金属活动性:镁>铁>铜,A方案合理。铁与MgSO₄溶液不反应,说明了活动性:镁>铁;铁与CuSO₄溶液反应置换出铜,说明了活动性:铁>铜,由此可得出三种金属活动性:镁>铁>铜,B方案合理。镁与稀盐酸反应生成氢气,说明了活动性:镁>氢;铁与稀盐酸反应生成氢气,说明了活动性:铁>氢;但镁与稀盐酸的反应比铁与稀盐酸的反应更剧烈,则可得活动性:镁>铁;铜与稀盐酸不反应,说明活动性:氢>铜,由此可得出三种金属活动性:镁>铁>铜,C方案合理。Cu与MgSO₄溶液、FeSO₄溶液均不反应,说明铜最不活泼,但无法验证镁和铁的活动性强弱,D方案不合理。(2)四种金属的活动性由强到弱的顺序为Mg、Zn、Cu、Ag,则向Cu(NO₃)₂溶液中加入Mg、Zn、Ag三种金属,镁先与硝酸铜反应生成铜和硝酸镁,若硝酸铜有剩余,则锌再与硝酸铜反应生成铜和硝酸锌,银与硝酸铜不反应,充分反应后过滤,得到无色滤液和滤渣,则硝酸铜已完全反应,滤渣中一定有银、铜,滤液中一定有硝酸镁,一定发生反应的化学方程式为Mg + Cu(NO₃)₂ = Cu + Mg(NO₃)₂;向滤渣中加入一定量的稀盐酸,有气泡产生,则滤渣中还一定有锌,滤液中可能含有的溶质是硝酸锌。
查看更多完整答案,请扫码查看


