第48页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
例1 (2024·榆林模拟)小龙同学利用NaCl、NH₄NO₃、NaOH固体和如图装置进行实验,待两边同时滴入等量水后,观察到U形管内的红墨水左侧液面下降,右侧液面升高。下列有关分析正确的是( )
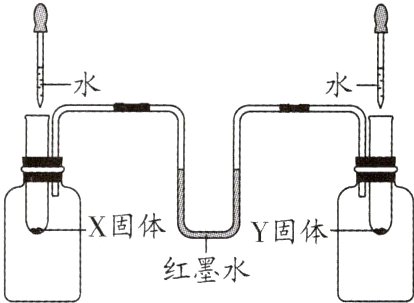
A. X一定是NaOH
B. Y一定是NH₄NO₃
C. X和Y都不可能是NaCl
D. 充分静置后,U形管内的液面会恢复至初始状态

A. X一定是NaOH
B. Y一定是NH₄NO₃
C. X和Y都不可能是NaCl
D. 充分静置后,U形管内的液面会恢复至初始状态
答案:
D 解析:观察到U形管内的红墨水左侧液面下降,右侧液面升高,则说明左侧压强增大,右侧压强不变,或者左侧压强不变,右侧压强减小,或者左侧压强增大,同时右侧压强减小;则X、Y的组合为NaOH、NaCl,或NaCl、NH₄NO₃,或NaOH、NH₄NO₃,A、B、C错误;充分静置后,溶液的温度会恢复至室温,则U形管内的液面会恢复至初始状态,D正确。
变式训练
1.(2024·泉州模拟)某化学兴趣小组同学设计了一个趣味实验装置如图所示,其气密性良好。若要使装置B中的尖嘴导管口有“喷泉”产生,则A中加入的固体和液体可能是( )
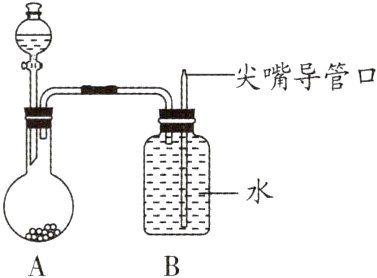
A. 硝酸铵和水
B. 铜和稀硫酸
C. 氯化钠和水
D. 镁和稀硫酸
1.(2024·泉州模拟)某化学兴趣小组同学设计了一个趣味实验装置如图所示,其气密性良好。若要使装置B中的尖嘴导管口有“喷泉”产生,则A中加入的固体和液体可能是( )

A. 硝酸铵和水
B. 铜和稀硫酸
C. 氯化钠和水
D. 镁和稀硫酸
答案:
D 解析:硝酸铵溶于水吸热,温度降低,装置中压强减小,则B中的水会倒吸入A中,B中尖嘴导管口不会产生“喷泉”,A不符合题意;铜和稀硫酸不反应,B中尖嘴导管口不会产生“喷泉”,B不符合题意;氯化钠与水不反应且溶于水,温度基本不变,B中尖嘴导管口不会产生“喷泉”,C不符合题意;镁和硫酸反应生成硫酸镁和氢气,A中气体增多,压强增大,气体会进入B装置中,则B中尖嘴导管口会产生“喷泉”,D符合题意。
例2 (2023·辽宁中考改编)下表是氯化钾的部分溶解度数据:
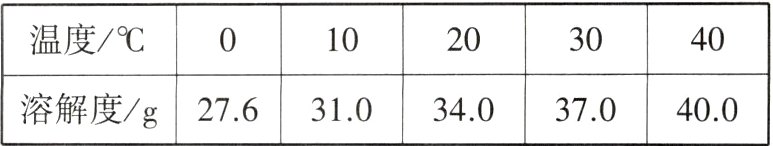
某同学用氯化钾进行了下图所示实验(实验过程中水分损失忽略不计)。下列说法错误的是( )
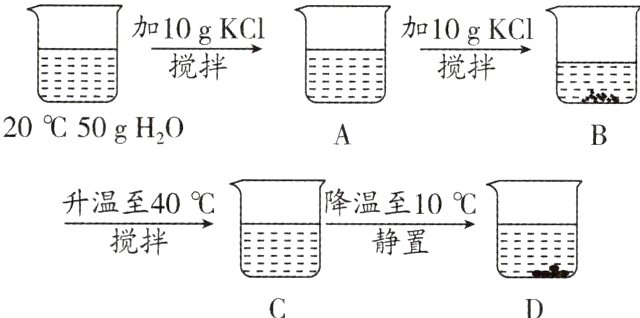
A. B、C、D一定是饱和溶液
B. A、C一定是不饱和溶液
C. D烧杯中析出晶体的质量是4.5 g
D. 若B烧杯升温至30℃时,烧杯中固体的质量是1.5 g

某同学用氯化钾进行了下图所示实验(实验过程中水分损失忽略不计)。下列说法错误的是( )

A. B、C、D一定是饱和溶液
B. A、C一定是不饱和溶液
C. D烧杯中析出晶体的质量是4.5 g
D. 若B烧杯升温至30℃时,烧杯中固体的质量是1.5 g
答案:
B 解析:B、D中明显有未溶解的KCl晶体,故B、D一定为饱和溶液,20℃时KCl的溶解度为34g,故50g水可以溶解17gKCl,但A中只溶解了10gKCl,则A为不饱和溶液,40℃时KCl的溶解度为40g,故50g水可以溶解20gKCl,C中刚好溶解了20gKCl,故C为饱和溶液,故B、C、D一定为饱和溶液,A正确,B错误;10℃时氯化钾的溶解度为31.0g,则50g水中最多溶解15.5g氯化钾,所以D中析出晶体的质量=10g+10g−15.5g=4.5g,C正确;若B烧杯升温至30℃时,30℃时KCl的溶解度为37g,50g水中可溶解18.5gKCl,剩余固体的质量为20g−18.5g=1.5g,D正确。
变式训练
2. 不同温度时,NaCl固体的溶解度如下表所示。
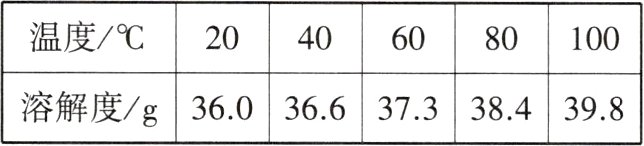
能将NaCl不饱和溶液变为NaCl饱和溶液的方法是( )
A. 加水
B. 升高温度
C. 加入NaCl
D. 倒出部分溶液
2. 不同温度时,NaCl固体的溶解度如下表所示。

能将NaCl不饱和溶液变为NaCl饱和溶液的方法是( )
A. 加水
B. 升高温度
C. 加入NaCl
D. 倒出部分溶液
答案:
C
例3 (2024·扬州中考)《本草纲目》记载:“火药乃焰硝、硫黄、杉木炭所合……”焰硝经处理可得到含少量NaCl的KNO₃溶液,将其蒸发浓缩、冷却结晶、过滤,最终得到较纯净的KNO₃固体。KNO₃和NaCl的溶解度曲线如图所示。下列说法正确的是( )

A. KNO₃的溶解度大于NaCl的溶解度
B. “蒸发浓缩”是为了获得较高温度下NaCl的饱和溶液
C. KNO₃的溶解度随温度降低大幅度减小,所以“冷却结晶”时析出KNO₃晶体
D. “过滤”所得滤液中的溶质只含有NaCl

A. KNO₃的溶解度大于NaCl的溶解度
B. “蒸发浓缩”是为了获得较高温度下NaCl的饱和溶液
C. KNO₃的溶解度随温度降低大幅度减小,所以“冷却结晶”时析出KNO₃晶体
D. “过滤”所得滤液中的溶质只含有NaCl
答案:
C 解析:选项中没有指明温度,无法比较KNO₃和NaCl的溶解度大小,A错误;含少量NaCl的KNO₃溶液,因氯化钠的溶解度受温度变化影响较小,硝酸钾的溶解度受温度变化影响较大,故“蒸发浓缩”是为了获得较高温度下硝酸钾的饱和溶液,B错误;由溶解度曲线可知,KNO₃的溶解度随温度降低大幅减小,所以“冷却结晶”时析出KNO₃晶体,C正确;KNO₃的溶解度随温度降低大幅减小,所以“冷却结晶”时析出KNO₃晶体,则“过滤”所得滤液为硝酸钾的饱和溶液,滤液中的溶质含有NaCl和硝酸钾,D错误。
查看更多完整答案,请扫码查看


