第46页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
1. 海洋资源的合理开发和综合利用对人类具有重要意义,下列说法错误的是(
A.淡化海水可以用蒸馏法
B.潮汐能属于可再生的海洋资源
C.海水含有丰富的氯化钠,它是由分子构成的
D.海底蕴藏着大量“可燃冰”,其主要成分是甲烷水合物
C
)A.淡化海水可以用蒸馏法
B.潮汐能属于可再生的海洋资源
C.海水含有丰富的氯化钠,它是由分子构成的
D.海底蕴藏着大量“可燃冰”,其主要成分是甲烷水合物
答案:
1.C
2. 如图是某兴趣小组在海洋资源的综合利用跨学科实践活动中,用海水样品(含有大量氯化钠,少量氯化镁和泥沙)模拟海水晒盐设计获取粗盐等产品的流程如图所示,根据海水晒盐的原理,下列说法正确的是(

A.在①中,海水中氯化钠的质量逐渐增大
B.①中,海水中水的质量逐渐增大
C.海水进入“储水池”,海水的成分基本不变
D.析出晶体后的母液是氯化钠的不饱和溶液
C
)
A.在①中,海水中氯化钠的质量逐渐增大
B.①中,海水中水的质量逐渐增大
C.海水进入“储水池”,海水的成分基本不变
D.析出晶体后的母液是氯化钠的不饱和溶液
答案:
2.C
3. 化学兴趣小组的同学们利用寒假时间,通过参观场馆、采访专家、实验模拟等形式,就“海洋资源的综合利用”展开了项目式学习。
活动一:认识海洋资源
【查阅资料】
(1) 海洋除蕴含着丰富的水资源外,还可为人类提供的资源是
(2) 海水中的氯、钠、镁、钾、溴等 11 种
活动二:模拟海水晒盐
海水晒盐的目的是从海水中获取 NaCl。同学们在实验室中用海水样品模拟海水晒盐。
【实验模拟】
取少量海水进行过滤。将过滤后的海水倒入蒸发皿中,点燃酒精灯加热海水,同时用玻璃棒不断搅拌。一段时间后有晶体析出,停止加热。
【实验分析】
同学们利用海水中两种主要物质的溶解度表对海水晒盐的过程进行分析。
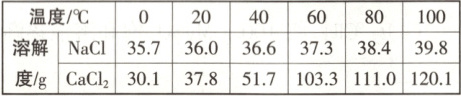
(3) 海水晒盐过程中析出的主要物质是____,原因是____。
活动三:海水晒盐
下图是综合利用海水的流程图,请回答下列问题。
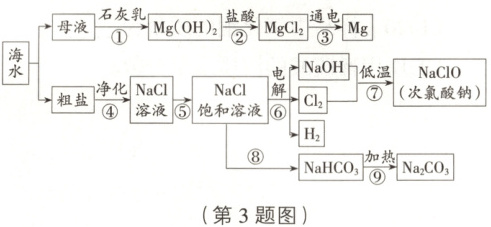
(4) 海水制镁。以上制镁的流程中发生中和反应的化学方程式是
(5) 海水制碱。侯氏制碱法制取的纯碱经常含有氯化钠杂质,某同学取少量纯碱样品加入过量稀盐酸充分反应后,再滴加 AgNO₃溶液观察到有白色沉淀产生,得出样品中含有氯化钠杂质的结论。实验后,经学习小组讨论发现上述方法有误,判断依据是____。
(6) 氯碱工业。步骤⑥发生反应的化学方程式是
活动一:认识海洋资源
【查阅资料】
(1) 海洋除蕴含着丰富的水资源外,还可为人类提供的资源是
化学资源(或矿产资源、生物资源等合理即可)
(写一种)。(2) 海水中的氯、钠、镁、钾、溴等 11 种
元素
(选填“元素”“原子”或“单质”)占海水所溶解物质总质量的 99.8%以上,从中可以提取 50 多种化学物质。活动二:模拟海水晒盐
海水晒盐的目的是从海水中获取 NaCl。同学们在实验室中用海水样品模拟海水晒盐。
【实验模拟】
取少量海水进行过滤。将过滤后的海水倒入蒸发皿中,点燃酒精灯加热海水,同时用玻璃棒不断搅拌。一段时间后有晶体析出,停止加热。
【实验分析】
同学们利用海水中两种主要物质的溶解度表对海水晒盐的过程进行分析。

(3) 海水晒盐过程中析出的主要物质是____,原因是____。
活动三:海水晒盐
下图是综合利用海水的流程图,请回答下列问题。

(4) 海水制镁。以上制镁的流程中发生中和反应的化学方程式是
$Mg(OH)_{2}+2HCl=MgCl_{2}+2H_{2}O$
。(5) 海水制碱。侯氏制碱法制取的纯碱经常含有氯化钠杂质,某同学取少量纯碱样品加入过量稀盐酸充分反应后,再滴加 AgNO₃溶液观察到有白色沉淀产生,得出样品中含有氯化钠杂质的结论。实验后,经学习小组讨论发现上述方法有误,判断依据是____。
(6) 氯碱工业。步骤⑥发生反应的化学方程式是
$2NaCl+2H_{2}O\xlongequal{通电}2NaOH+Cl_{2}\uparrow+H_{2}\uparrow$
。
答案:
3.
(1)化学资源(或矿产资源、生物资源等合理即可)
(2)元素
(3)氯化钠 氯化钠的溶解度受温度影响不大,蒸发过程中结晶析出,氯化钙的溶解度随温度的升高而增加,且受温度影响较大,故蒸发过程中,氯化钙溶解在水中,不易析出
$(4)Mg(OH)_{2}+2HCl=MgCl_{2}+2H_{2}O$
(5)盐酸中也含有$Cl^{-},$也会与$AgNO_{3}$反应产生白色沉淀
$(6)2NaCl+2H_{2}O\xlongequal{通电}2NaOH+Cl_{2}\uparrow+H_{2}\uparrow$
(1)化学资源(或矿产资源、生物资源等合理即可)
(2)元素
(3)氯化钠 氯化钠的溶解度受温度影响不大,蒸发过程中结晶析出,氯化钙的溶解度随温度的升高而增加,且受温度影响较大,故蒸发过程中,氯化钙溶解在水中,不易析出
$(4)Mg(OH)_{2}+2HCl=MgCl_{2}+2H_{2}O$
(5)盐酸中也含有$Cl^{-},$也会与$AgNO_{3}$反应产生白色沉淀
$(6)2NaCl+2H_{2}O\xlongequal{通电}2NaOH+Cl_{2}\uparrow+H_{2}\uparrow$
查看更多完整答案,请扫码查看


