第59页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
8. 某同学绘制了含铁元素的部分物质转化关系图(图中“$\to$”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去)。下列说法中,正确的是(
A.铁丝能在空气中剧烈燃烧实现转化①
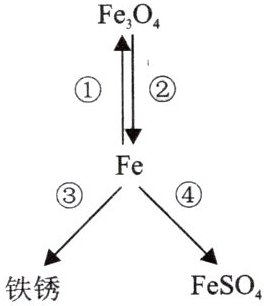
B.转化②可通过$\mathrm{Fe_3O_4}$与$\mathrm{CO}$在常温下反应实现
C.氧气和水同时存在是实现转化③的主要条件
D.通过$\mathrm{Fe}$与$\mathrm{ZnSO_4}$溶液反应可实现转化④
【素养发展】
C
)。A.铁丝能在空气中剧烈燃烧实现转化①

B.转化②可通过$\mathrm{Fe_3O_4}$与$\mathrm{CO}$在常温下反应实现
C.氧气和水同时存在是实现转化③的主要条件
D.通过$\mathrm{Fe}$与$\mathrm{ZnSO_4}$溶液反应可实现转化④
【素养发展】
答案:
8.C
9. 菱锌矿是工业上制备硫酸锌的原料。菱锌矿的主要成分是$\mathrm{ZnCO_3}$,还含有$\mathrm{SiO_2}$和$\mathrm{Fe_2O_3}$等。如图是用碳酸锌样品(杂质为$\mathrm{SiO_2}$和$\mathrm{Fe_2O_3}$;$\mathrm{SiO_2}$难溶于水,也不与稀硫酸反应)模拟工业制备$\mathrm{ZnSO_4}$的流程,已知:锌能将$\mathrm{Fe^{3+}}$转化为$\mathrm{Fe^{2+}}$,再将$\mathrm{Fe^{2+}}$转化为$\mathrm{Fe}$。下列有关说法中,合理的是(
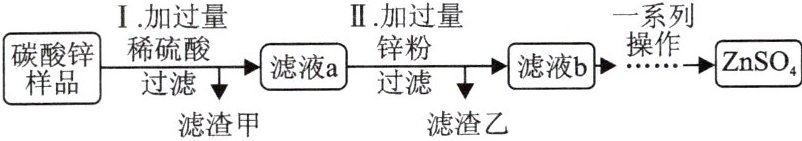
A.滤液a为无色溶液
B.滤渣甲是$\mathrm{SiO_2}$
C.滤渣乙是单质铁
D.步骤Ⅱ无气体生成
B
)。
A.滤液a为无色溶液
B.滤渣甲是$\mathrm{SiO_2}$
C.滤渣乙是单质铁
D.步骤Ⅱ无气体生成
答案:
9.B
10. 如图为我国古代“炼石胆取精华法”制取硫酸的部分场景,其过程为“一炉中以炭烧石胆使作烟,以物扇之,其精华尽入铜盘”。有关反应的化学方程式如下:①$\mathrm{CuSO_4·5H_2O\xlongequal{\triangle}CuO+SO_3\uparrow+5H_2O\uparrow}$;②$\mathrm{SO_3+H_2O=H_2SO_4}$。
(1) 反应①属于
(2) “精华”尽入铜盘而不用铁盘的原因是
(3) 《太土古兑经》中提到“烧石胆皆具蚀气”,可见古人已认识到硫酸具有
(4) 古代用稀硫酸除去兵器上铁锈的原理是
(5) 在混有少量氧化铜的铁粉中加入盐酸,充分反应后过滤,向滤渣中加入盐酸,仍有气泡产生,则滤渣中肯定含有的物质是

(1) 反应①属于
分解反应
(填基本反应类型)。(2) “精华”尽入铜盘而不用铁盘的原因是
“精华”为硫酸,其与铁能反应,而与铜不反应
。(3) 《太土古兑经》中提到“烧石胆皆具蚀气”,可见古人已认识到硫酸具有
腐蚀
性。(4) 古代用稀硫酸除去兵器上铁锈的原理是
Fe₂O₃+3H₂SO₄=Fe₂(SO₄)₃+3H₂O
(用化学方程式表示)。(5) 在混有少量氧化铜的铁粉中加入盐酸,充分反应后过滤,向滤渣中加入盐酸,仍有气泡产生,则滤渣中肯定含有的物质是
Fe、Cu
,滤液中肯定含有溶质的化学式是FeSO₄
。
答案:
10.
(1)分解反应
(2)“精华”为硫酸,其与铁能反应,而与铜不反应
(3)腐蚀
(4)Fe₂O₃+3H₂SO₄=Fe₂(SO₄)₃+3H₂O
(5)Fe、Cu FeSO₄
(1)分解反应
(2)“精华”为硫酸,其与铁能反应,而与铜不反应
(3)腐蚀
(4)Fe₂O₃+3H₂SO₄=Fe₂(SO₄)₃+3H₂O
(5)Fe、Cu FeSO₄
查看更多完整答案,请扫码查看


