第114页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
8. 在两个烧杯中,分别装有质量相等的浓硫酸和浓盐酸。若将它们在空气中放置一段时间,则(
A.浓盐酸的溶液质量增大
B.浓硫酸的溶液质量增大
C.浓盐酸的溶质质量分数不变
D.浓硫酸的溶质质量分数不变
B
)A.浓盐酸的溶液质量增大
B.浓硫酸的溶液质量增大
C.浓盐酸的溶质质量分数不变
D.浓硫酸的溶质质量分数不变
答案:
B
9. (2025·遵义模拟)下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是(
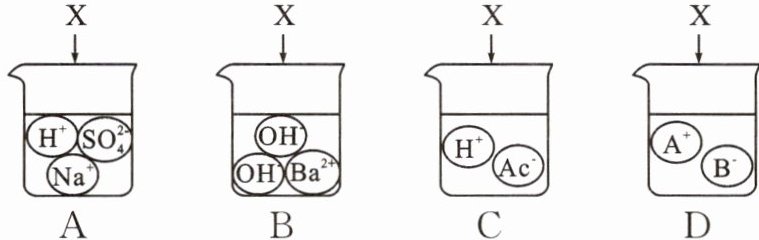
C
)
答案:
C
10. 保存或使用盐酸的合理方法是(
A.密封保存在阴凉处
B.与NaOH等碱类物质放在同一个药品橱内
C.用广口瓶盛放浓盐酸
D.把鼻孔凑在容器口闻浓盐酸的气味
A
)A.密封保存在阴凉处
B.与NaOH等碱类物质放在同一个药品橱内
C.用广口瓶盛放浓盐酸
D.把鼻孔凑在容器口闻浓盐酸的气味
答案:
A
11. 下列关于盐酸的描述,错误的是(
A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
B
)A.浓盐酸有刺激性气味
B.盐酸具有强烈的吸水性
C.盐酸是氯化氢气体的水溶液
D.打开装有浓盐酸的试剂瓶,瓶口处有白雾
答案:
B
12. (2024·汕头一模)稀释浓硫酸时不需要用到的仪器是(
A.烧杯
B.量筒
C.玻璃棒
D.托盘天平
D
)A.烧杯
B.量筒
C.玻璃棒
D.托盘天平
答案:
D
13. (易错题)下列有关浓盐酸和浓硫酸的叙述中,正确的是(
A.打开浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.浓盐酸和浓硫酸都能作干燥剂
C.浓盐酸和浓硫酸敞口放置,溶质的质量分数都会减小
D.浓盐酸和浓硫酸都能使纸张炭化
C
)A.打开浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.浓盐酸和浓硫酸都能作干燥剂
C.浓盐酸和浓硫酸敞口放置,溶质的质量分数都会减小
D.浓盐酸和浓硫酸都能使纸张炭化
答案:
C
14. (学科融合)①醋酸、②乳酸、③碳酸、④盐酸、⑤硫酸、⑥硝酸是我们生活中经常遇到的一些酸,你能分清它们吗?请把它们的序号分别填在下列空格中(每空只能写一种物质):
(1)汽水中含有的酸是
(2)牛奶里含有的酸是
(3)食醋里含有的酸是
(4)由胃分泌的帮助消化食物的酸是
(5)汽车用的铅酸蓄电池中的酸是
(6)最后三种浓酸中,打开瓶盖后肯定不会看到“白雾”的是
(1)汽水中含有的酸是
③
。(2)牛奶里含有的酸是
②
。(3)食醋里含有的酸是
①
。(4)由胃分泌的帮助消化食物的酸是
④
。(5)汽车用的铅酸蓄电池中的酸是
⑤
。(6)最后三种浓酸中,打开瓶盖后肯定不会看到“白雾”的是
⑤
。
答案:
(1)③
(2)②
(3)①
(4)④
(5)⑤
(6)⑤
(1)③
(2)②
(3)①
(4)④
(5)⑤
(6)⑤
15. 如图是浓盐酸试剂瓶上标签的部分内容。请回答:
盐酸(分析纯)
化学式HCl
质量分数36%
密度$1.18g/cm^3$
(1)该浓盐酸的溶质是
(2)现要配制3%的稀盐酸120g,需要这种浓盐酸
(3)使用一段时间后,浓盐酸的溶质质量分数小于36%,原因是
盐酸(分析纯)
化学式HCl
质量分数36%
密度$1.18g/cm^3$
(1)该浓盐酸的溶质是
HCl
(填化学式)。(2)现要配制3%的稀盐酸120g,需要这种浓盐酸
10
g。(3)使用一段时间后,浓盐酸的溶质质量分数小于36%,原因是
浓盐酸具有挥发性,HCl挥发后溶质的质量分数变小
。
答案:
(1)HCl
(2)10
(3)浓盐酸具有挥发性,HCl挥发后溶质的质量分数变小
(1)HCl
(2)10
(3)浓盐酸具有挥发性,HCl挥发后溶质的质量分数变小
16. (教材变式题)实验室中常需要使用硫酸。
(1)用小木棍蘸少量浓硫酸,放置一会儿后,可观察到
(2)98%的浓硫酸稀释为稀硫酸时,一定要将
(3)49g质量分数为20%的稀硫酸与足量锌反应,最多生成氢气的质量是多少?(写出计算过程)
(1)用小木棍蘸少量浓硫酸,放置一会儿后,可观察到
蘸有硫酸的部位变黑
。(2)98%的浓硫酸稀释为稀硫酸时,一定要将
浓硫酸
沿烧杯内壁缓慢地注入盛有水
的烧杯里,并用玻璃棒
不断搅拌,此时触摸烧杯外壁,可发现浓硫酸与水混合产生大量热
。(3)49g质量分数为20%的稀硫酸与足量锌反应,最多生成氢气的质量是多少?(写出计算过程)
解:设最多生成氢气的质量为x。Zn+H₂SO₄=ZnSO₄+H₂↑ 98 2 49 g×20% x $\frac{98}{2}=\frac{49\ g×20\%}{x}$ x=0.2 g 答:最多生成氢气的质量是0.2 g。
答案:
(1)蘸有硫酸的部位变黑
(2)浓硫酸 水 玻璃棒 热
(3)解:设最多生成氢气的质量为x。Zn+H₂SO₄=ZnSO₄+H₂↑ 98 2 49 g×20% x $\frac{98}{2}=\frac{49\ g×20\%}{x}$ x=0.2 g 答:最多生成氢气的质量是0.2 g。
(1)蘸有硫酸的部位变黑
(2)浓硫酸 水 玻璃棒 热
(3)解:设最多生成氢气的质量为x。Zn+H₂SO₄=ZnSO₄+H₂↑ 98 2 49 g×20% x $\frac{98}{2}=\frac{49\ g×20\%}{x}$ x=0.2 g 答:最多生成氢气的质量是0.2 g。
查看更多完整答案,请扫码查看


