2025年暑假生活北京师范大学出版社高二化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假生活北京师范大学出版社高二化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
7. 有关晶体的结构如图 4 - 5 所示,下列说法错误的是(
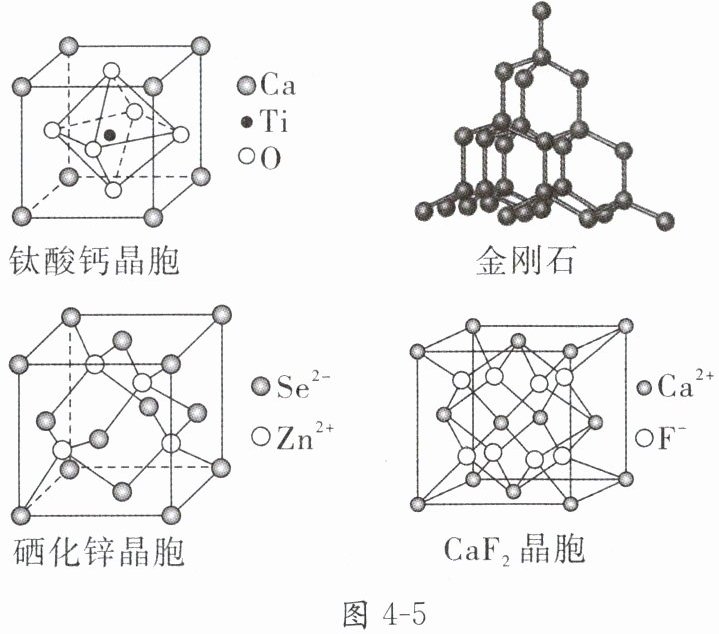
A.钛酸钙的化学式为$ CaTiO_3$
B.在金刚石晶体中,碳原子与碳碳键(C—C)的数目之比为 1:2
C.硒化锌晶体中与 1 个$ Se^2⁻$距离最近且相等的$ Se^2⁻$有 8 个
D.CaF_2中 F⁻与距离最近的 Ca^2⁺所形成的键的夹角为$109^{\circ}28'$
C
)。
A.钛酸钙的化学式为$ CaTiO_3$
B.在金刚石晶体中,碳原子与碳碳键(C—C)的数目之比为 1:2
C.硒化锌晶体中与 1 个$ Se^2⁻$距离最近且相等的$ Se^2⁻$有 8 个
D.CaF_2中 F⁻与距离最近的 Ca^2⁺所形成的键的夹角为$109^{\circ}28'$
答案:
C
8. 配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备某些配位化合物,如$2CoCl_{2}+2NH_{4}Cl+8NH_{3}+H_{2}O_{2}= 2[Co(NH_{3})_{5}Cl]Cl_{2}+2H_{2}O$。下列说法正确的是(
A.该配位化合物的配位数为 5
B.提供孤电子对的成键原子是 N 和 Cl
C.$[Co(NH_{3})_{5}Cl]^{2+}$中存在配位键、共价键和离子键
D.氧化剂$ H_2O_2$是非极性分子
B
)。A.该配位化合物的配位数为 5
B.提供孤电子对的成键原子是 N 和 Cl
C.$[Co(NH_{3})_{5}Cl]^{2+}$中存在配位键、共价键和离子键
D.氧化剂$ H_2O_2$是非极性分子
答案:
B
9. 铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图 4 - 6 所示(黑球代表 Fe,白球代表 Mg),铁镁合金的化学式为
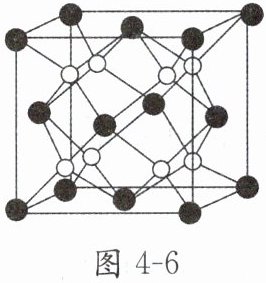
Mg₂Fe(或FeMg₂)
。若该晶胞为正方体,棱长为 a cm,Nₐ为阿伏加德罗常数的值,则镁原子与铁原子间的最短距离为$\frac{\sqrt{3}a}{4}$
cm,晶胞的密度为$\frac{416}{a^{3}N_{A}}$
$g·cm⁻^3$。
答案:
Mg₂Fe(或FeMg₂) $\frac{\sqrt{3}a}{4}$ $\frac{416}{a^{3}N_{A}}$
10. (1) KIO₃晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,棱长为 a nm,晶胞中 K、I、O 分别处于顶角、体心、面心位置,如图 4 - 7 所示。与 K 紧邻的 O 的个数为
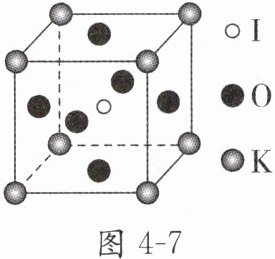
(2) 若 KIO₃晶胞中处于左下角顶角的 K 的坐标参数为(0,0,0),位于下底面面心位置的 O 的坐标参数为$(\frac{1}{2},\frac{1}{2},0)$,在 KIO₃晶胞结构的另一种表示中,I 处于各顶角位置,设左下角顶角的 I 的坐标参数为(0,0,0),则 K 的坐标参数为
12
,已知阿伏加德罗常数的值为 Nₐ,则 KIO₃晶体的密度为$\frac{214}{N_{A}·(a×10^{-7})^{3}}$
g·cm⁻³(列式表示)。
(2) 若 KIO₃晶胞中处于左下角顶角的 K 的坐标参数为(0,0,0),位于下底面面心位置的 O 的坐标参数为$(\frac{1}{2},\frac{1}{2},0)$,在 KIO₃晶胞结构的另一种表示中,I 处于各顶角位置,设左下角顶角的 I 的坐标参数为(0,0,0),则 K 的坐标参数为
($\frac{1}{2}$,$\frac{1}{2}$,$\frac{1}{2}$)
。
答案:
(1)12 $\frac{214}{N_{A}·(a×10^{-7})^{3}}$
(2)($\frac{1}{2}$,$\frac{1}{2}$,$\frac{1}{2}$)
(1)12 $\frac{214}{N_{A}·(a×10^{-7})^{3}}$
(2)($\frac{1}{2}$,$\frac{1}{2}$,$\frac{1}{2}$)
11. 材料是人类文明进步的阶梯,第ⅢA、ⅣA、ⅤA 族元素是组成特殊材料的重要元素。请回答下列问题。
(1) 基态 Ge 的价层电子的轨道表示式为____;基态 As 核外电子占据的能量最高的能级的电子云形状为
(2) Si、P、S、Cl 的第一电离能由大到小的顺序为
(3) M 与 Ga 位于同周期,$M^{3+}的一种配合物组成为[M(NH_{3})_{5}(H_{2}O)]Cl_{3}$。
①下列有关 NH₃、H₂O 的说法正确的是
a. 分子空间结构相同
b. 中心原子杂化轨道类型相同
c. 键角大小相同
②1 mol$[M(NH_{3})_{5}(H_{2}O)]^{3+}$含
③配合物 T 与$[M(NH_{3})_{5}(H_{2}O)]Cl_{3}$组成元素相同,中心离子的配位数相同。1 mol T 溶于水,加入足量 AgNO₃溶液可生成 2 mol AgCl。则 T 的化学式为
(4) 磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图 4 - 8 所示,该晶胞中 B 与相邻的 P 构成
已知该晶体的密度为 ρ g·cm⁻³,设 Nₐ是阿伏加德罗常数的值。BP 晶胞中面心上 6 个 P 相连构成正八面体,该正八面体的棱长为
(1) 基态 Ge 的价层电子的轨道表示式为____;基态 As 核外电子占据的能量最高的能级的电子云形状为
哑铃形(或纺锤形)
。(2) Si、P、S、Cl 的第一电离能由大到小的顺序为
Cl>P>S>Si
。(3) M 与 Ga 位于同周期,$M^{3+}的一种配合物组成为[M(NH_{3})_{5}(H_{2}O)]Cl_{3}$。
①下列有关 NH₃、H₂O 的说法正确的是
b
(填字母)。a. 分子空间结构相同
b. 中心原子杂化轨道类型相同
c. 键角大小相同
②1 mol$[M(NH_{3})_{5}(H_{2}O)]^{3+}$含
23
mol σ键。③配合物 T 与$[M(NH_{3})_{5}(H_{2}O)]Cl_{3}$组成元素相同,中心离子的配位数相同。1 mol T 溶于水,加入足量 AgNO₃溶液可生成 2 mol AgCl。则 T 的化学式为
[M(NH₃)₅Cl]Cl₂·H₂O
。(4) 磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如图 4 - 8 所示,该晶胞中 B 与相邻的 P 构成
正四面体
(填“立方体”“正四面体”或“正八面体”)。已知该晶体的密度为 ρ g·cm⁻³,设 Nₐ是阿伏加德罗常数的值。BP 晶胞中面心上 6 个 P 相连构成正八面体,该正八面体的棱长为
$\frac{\sqrt{2}}{2}$×$\sqrt[3]{\frac{168}{\rho N_{A}}}$×10¹⁰
pm(列式即可)。
答案:
(1)哑铃形(或纺锤形)
(2)Cl>P>S>Si
(3)①sp³ ②23 ③[M(NH₃)₅Cl]Cl₂·H₂O
(4)正四面体 $\frac{\sqrt{2}}{2}$×$\sqrt[3]{\frac{168}{\rho N_{A}}}$×10¹⁰
(1)哑铃形(或纺锤形)
(2)Cl>P>S>Si
(3)①sp³ ②23 ③[M(NH₃)₅Cl]Cl₂·H₂O
(4)正四面体 $\frac{\sqrt{2}}{2}$×$\sqrt[3]{\frac{168}{\rho N_{A}}}$×10¹⁰
查看更多完整答案,请扫码查看


