2025年暑假生活北京师范大学出版社高二化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假生活北京师范大学出版社高二化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
5. 处于同一周期的A、B、C、D四种短周期元素,其气态原子获得一个电子所放出的能量:$A\gt B\gt C\gt D$。则下列说法正确的是(
A.非金属性:$A\lt B\lt C\lt D$
B.电负性:$A\lt B\lt C\lt D$
C.第一电离能:$A\lt B\lt C\lt D$
D.最高价氧化物对应水化物的酸性:$A\gt B\gt C\gt D$
D
)。A.非金属性:$A\lt B\lt C\lt D$
B.电负性:$A\lt B\lt C\lt D$
C.第一电离能:$A\lt B\lt C\lt D$
D.最高价氧化物对应水化物的酸性:$A\gt B\gt C\gt D$
答案:
D
6. 图2-4是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法错误的是(
A.电负性:$a\gt f$
B.第一电离能:$d\gt c$
C.简单气态氢化物的稳定性:$f\gt e$
D.a和b形成的化合物可能含有共价键
B
)。A.电负性:$a\gt f$
B.第一电离能:$d\gt c$
C.简单气态氢化物的稳定性:$f\gt e$
D.a和b形成的化合物可能含有共价键
答案:
B
7. 图2-5为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是(
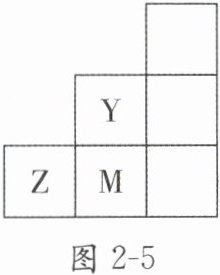
A.电负性:$Y\gt Z\gt M$
B.简单离子半径:$M\gt Z\gt Y$
C.$ZM_{2}$分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子的轨道表示式为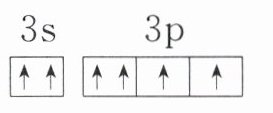
C
)。
A.电负性:$Y\gt Z\gt M$
B.简单离子半径:$M\gt Z\gt Y$
C.$ZM_{2}$分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子的轨道表示式为

答案:
C
8. 以下有关元素性质的说法不正确的是(
A.具有下列电子排布式的原子:①$1s^{2}2s^{2}2p^{6}3s^{2}3p^{2}$;②$1s^{2}2s^{2}2p^{3}$;③$1s^{2}2s^{2}2p^{2}$;④$1s^{2}2s^{2}2p^{6}3s^{2}3p^{4}$。原子半径最大的是①
B.具有下列价层电子排布式的原子:①$3s^{2}3p^{1}$;②$3s^{2}3p^{2}$;③$3s^{2}3p^{3}$;④$3s^{2}3p^{4}$。第一电离能最大的是③
C.①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl。元素的电负性随原子序数的增加而递增的是④
D.某元素X的逐级电离能(单位:$kJ\cdot mol^{ - 1}$)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时,最可能生成的阳离子是$X^{3 + }$
D
)。A.具有下列电子排布式的原子:①$1s^{2}2s^{2}2p^{6}3s^{2}3p^{2}$;②$1s^{2}2s^{2}2p^{3}$;③$1s^{2}2s^{2}2p^{2}$;④$1s^{2}2s^{2}2p^{6}3s^{2}3p^{4}$。原子半径最大的是①
B.具有下列价层电子排布式的原子:①$3s^{2}3p^{1}$;②$3s^{2}3p^{2}$;③$3s^{2}3p^{3}$;④$3s^{2}3p^{4}$。第一电离能最大的是③
C.①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl。元素的电负性随原子序数的增加而递增的是④
D.某元素X的逐级电离能(单位:$kJ\cdot mol^{ - 1}$)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时,最可能生成的阳离子是$X^{3 + }$
答案:
D
9. 现有五种前四周期元素,其结构信息见下表,回答下列问题。
|元素|结构信息|
|A|基态原子有6个原子轨道填充满电子,有3个未成对电子|
|B|M层电子数比L层电子数少2个|
|C|基态原子核外有17个不同运动状态的电子|
|D|基态原子的价层电子排布式为$3d^{x}4s^{2}$,在常见化合物中其最高正价为+7|
|E|基态原子的M层全充满,N层没有成对电子,只有1个未成对电子|
(1)A、B、C三种元素最高价氧化物对应的水化物的酸性由强到弱的顺序为____(用最高价氧化物对应的水化物的化学式表示)。
(2)D在元素周期表中的位置为____,其基态原子的价层电子排布式为____。
(3)写出基态B原子价层电子的轨道表示式:____。
(4)E位于元素周期表的____区,基态原子填有电子的轨道数为____。
|元素|结构信息|
|A|基态原子有6个原子轨道填充满电子,有3个未成对电子|
|B|M层电子数比L层电子数少2个|
|C|基态原子核外有17个不同运动状态的电子|
|D|基态原子的价层电子排布式为$3d^{x}4s^{2}$,在常见化合物中其最高正价为+7|
|E|基态原子的M层全充满,N层没有成对电子,只有1个未成对电子|
(1)A、B、C三种元素最高价氧化物对应的水化物的酸性由强到弱的顺序为____(用最高价氧化物对应的水化物的化学式表示)。
(2)D在元素周期表中的位置为____,其基态原子的价层电子排布式为____。
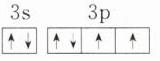
(3)写出基态B原子价层电子的轨道表示式:____。
(4)E位于元素周期表的____区,基态原子填有电子的轨道数为____。
答案:
(1)HClO₄>H₂SO₄>H₃PO₄
(2)第四周期第ⅦB族 3d⁵4s²
(3)
(4)ds 15
(1)HClO₄>H₂SO₄>H₃PO₄
(2)第四周期第ⅦB族 3d⁵4s²
(3)

(4)ds 15
查看更多完整答案,请扫码查看


