第78页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
21.(10分)(2025·扬州期末)金属的冶炼和利用大大促进了人类文明的进步。
Ⅰ.金属的性质
(1)铝具有很好的抗腐蚀性,因为铝在空气中能与氧气反应形成一层致密的氧化铝薄膜,反应的化学方程式为
(2)已知胆矾溶于水得到硫酸铜溶液,请用化学方程式解释“熬胆矾铁釜,久之亦化为铜”的原因:
Ⅱ.金属的冶炼
(3)工业上用赤铁矿$(Fe_2O_3)$炼铁,CO与$Fe_2O_3$反应的化学方程式为
Ⅲ.金属的腐蚀
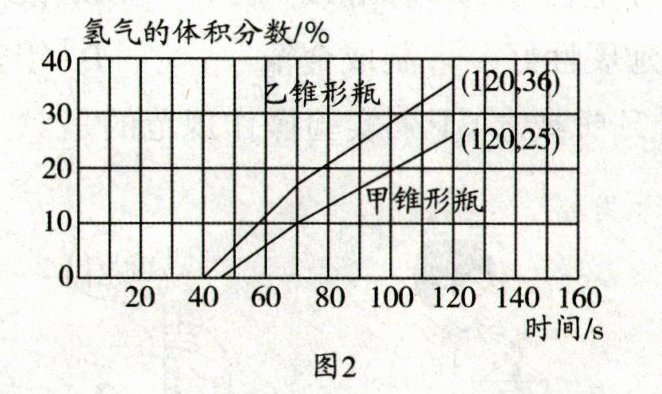
(4)实验小组通过下列实验探究影响钢铁腐蚀的因素,实验如图1、图2所示。
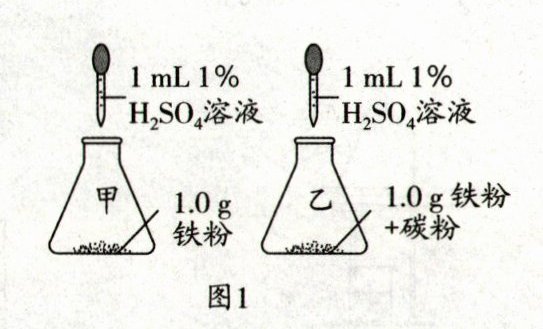
①铁在稀硫酸中发生腐蚀反应的化学方程式是
②从图2分析可知,实验中腐蚀速率较快的是
③通过本实验你认为提高钢铁的抗腐蚀能力的方法是
Ⅰ.金属的性质
(1)铝具有很好的抗腐蚀性,因为铝在空气中能与氧气反应形成一层致密的氧化铝薄膜,反应的化学方程式为
4Al+3O₂2Al₂O₃
。(2)已知胆矾溶于水得到硫酸铜溶液,请用化学方程式解释“熬胆矾铁釜,久之亦化为铜”的原因:
Fe+CuSO₄Cu+FeSO₄
。Ⅱ.金属的冶炼
(3)工业上用赤铁矿$(Fe_2O_3)$炼铁,CO与$Fe_2O_3$反应的化学方程式为
3CO+Fe₂O₃2Fe+3CO₂
。炼铁时,加入菱锰矿可制得冶炼锰钢的材料。锰钢用作高铁的钢轨,主要利用了锰钢的硬度大
性能。Ⅲ.金属的腐蚀
(4)实验小组通过下列实验探究影响钢铁腐蚀的因素,实验如图1、图2所示。


①铁在稀硫酸中发生腐蚀反应的化学方程式是
Fe+H₂SO₄FeSO₄+H₂↑
。②从图2分析可知,实验中腐蚀速率较快的是
乙
(填“甲”或“乙”)锥形瓶中的样品。③通过本实验你认为提高钢铁的抗腐蚀能力的方法是
降低钢铁中的含碳量
。
答案:
(1)4Al+3O₂2Al₂O₃
(2)Fe+CuSO₄Cu+FeSO₄
(3)3CO+Fe₂O₃2Fe+3CO₂ 硬度大
(4)①Fe+H₂SO₄FeSO₄+H₂↑ ②乙 ③降低钢铁中的含碳量
(1)4Al+3O₂2Al₂O₃
(2)Fe+CuSO₄Cu+FeSO₄
(3)3CO+Fe₂O₃2Fe+3CO₂ 硬度大
(4)①Fe+H₂SO₄FeSO₄+H₂↑ ②乙 ③降低钢铁中的含碳量
22.(10分)“三寸粉笔,三尺讲台系国运”这是对教师的礼赞。教师授课的粉笔主要成分为石灰石$(CaCO_3)$和石膏$(CaSO_4)。$如图,将32g制作好的粉笔末放于硬质玻璃管中高温煅烧使其充分反应,冷却后称量剩余固体的质量为23.2g。(已知$:CaSO_4$和杂质受热都不分解,也不与$CaCO_3$反应)
回答下列问题:
$(1)CaSO_4$中硫元素和氧元素的质量比为______
(2)反应生成二氧化碳的质量为______
(3)计算32g粉笔末中$CaCO_3$的质量分数(写出计算过程)。
(4)酒精灯的燃料为酒精,量取一定体积的酒精所需要的仪器是______
回答下列问题:
$(1)CaSO_4$中硫元素和氧元素的质量比为______
1:2
。(2)反应生成二氧化碳的质量为______
8.8
g。(3)计算32g粉笔末中$CaCO_3$的质量分数(写出计算过程)。
解:设该粉笔末中碳酸钙的质量分数为x。CaCO₃CaO+CO₂↑100 4432g·x 8.8g= x=62.5%答:该粉笔末中碳酸钙的质量分数为62.5%。
(4)酒精灯的燃料为酒精,量取一定体积的酒精所需要的仪器是______
量筒
和胶头滴管,若仰视读数,则量取酒精的实际体积______偏大
(填“偏大”“偏小”或“相等”)。
答案:
(1)1:2
(2)8.8
(3)解:设该粉笔末中碳酸钙的质量分数为x。CaCO₃CaO+CO₂↑100 4432g·x 8.8g= x=62.5%答:该粉笔末中碳酸钙的质量分数为62.5%。
(4)量筒 偏大
(1)1:2
(2)8.8
(3)解:设该粉笔末中碳酸钙的质量分数为x。CaCO₃CaO+CO₂↑100 4432g·x 8.8g= x=62.5%答:该粉笔末中碳酸钙的质量分数为62.5%。
(4)量筒 偏大
查看更多完整答案,请扫码查看


