第40页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
17. (5 分)利用化学方法可消除家居装修过程中产生的甲醛,其反应的微观示意图如下,回答下列问题:
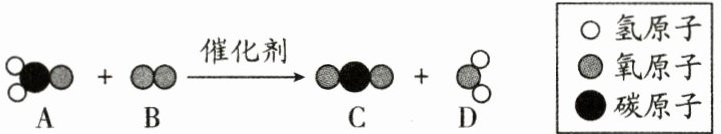
(1)甲醛的化学式为 $ CH_{2}O $,图中表示甲醛分子的是
(2)甲醛中碳元素与氢元素的质量比为
(3)该反应的化学方程式为

(1)甲醛的化学式为 $ CH_{2}O $,图中表示甲醛分子的是
A
(填字母)。(2)甲醛中碳元素与氢元素的质量比为
6∶1
。(3)该反应的化学方程式为
CH₂O+O₂$\frac{\underline{\;催化剂\;}}{\;}$CO₂+H₂O
。
答案:
(1)A
(2)6∶1
(3)CH₂O+O₂$\frac{\underline{\;催化剂\;}}{\;}$CO₂+H₂O解析:
(2)甲醛中碳元素与氢元素的质量比为12∶(1×2)=6∶1。
(1)A
(2)6∶1
(3)CH₂O+O₂$\frac{\underline{\;催化剂\;}}{\;}$CO₂+H₂O解析:
(2)甲醛中碳元素与氢元素的质量比为12∶(1×2)=6∶1。
18. (7 分)在质量守恒定律的实验探究活动中,某小组同学将一根用砂纸打磨干净的长镁条和一个陶土网一起放在托盘天平上称量,记录所称的质量为 $ m_{1} $。在陶土网上方将镁条点燃,观察到的现象是
镁条燃烧,发出耀眼的白光,放出热量,生成白色固体
。将镁条燃烧后的产物与陶土网一起放在托盘天平上称量,记录所称的质量为 $ m_{2} $,发现 $ m_{1} > m_{2} $,该反应遵循
(填“遵循”或“不遵循”)质量守恒定律。如果在燃着的镁条上方罩上烧杯,使生成物全部收集起来与陶土网一起放在托盘天平上称量,记录所称的质量为 $ m_{3} $,则 $ m_{1} $<
(填“>”“<”或“=”) $ m_{3} $,原因是空气中氧气参加反应,生成物氧化镁的质量大于镁条的质量
。
答案:
镁条燃烧,发出耀眼的白光,放出热量,生成白色固体 遵循 < 空气中氧气参加反应,生成物氧化镁的质量大于镁条的质量解析:镁在空气中燃烧发出耀眼的白光,放出热量,生成白色的固体。化学变化都遵循质量守恒定律,而m₁>m₂是由于镁在空气中燃烧时,部分生成物逸散到空气中。由于该反应有空气中的氧气参加了反应,而反应前没有称量到氧气的质量,故m₁<m₂。
19. (7 分)已知 A、B、C、D、E 是初中化学常见的五种物质。它们分别由 C、H、O 中的一种或几种元素组成,通常状况下 A、C 为气体,B 为黑色固体,D、E 为液体(“—”表示相连的两种物质能发生反应,“→”表示相连物质能向箭头所指一方转化,部分反应物、生成物及反应条件已省略)。请回答下列问题:
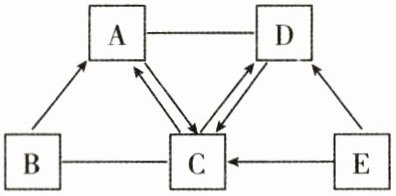
(1)B 生成 A 属于____
(2)C 物质的用途:____
(3)请写出 B 与 C 反应的化学方程式:____
(4)请写出 $ E \to C $ 反应的化学方程式:____

(1)B 生成 A 属于____
化合
(填基本反应类型)反应。(2)C 物质的用途:____
用于医疗急救
(答一点即可)。(3)请写出 B 与 C 反应的化学方程式:____
C+O₂$\frac{\underline{\;点燃\;}}{\;}$CO₂
。(4)请写出 $ E \to C $ 反应的化学方程式:____
2H₂O₂$\frac{\underline{\;MnO_2\;}}{\;}$O₂↑+2H₂O
。
答案:
(1)化合
(2)用于医疗急救
(3)C+O₂$\frac{\underline{\;点燃\;}}{\;}$CO₂
(4)2H₂O₂$\frac{\underline{\;MnO_2\;}}{\;}$O₂↑+2H₂O解析:A、B、C、D、E分别由C、H、O中的一种或几种元素组成,通常状况下D、E为液体,A、C为气体,D、E、C之间转化符合过氧化氢在二氧化锰的催化作用下分解生成水和氧气;A为气体,B为黑色固体,A、B、C之间转化关系符合二氧化碳通过光合作用生成氧气,含碳物质燃烧生成二氧化碳。
(1)B生成A的反应为木炭和氧气反应生成二氧化碳,反应符合"多变一"特点,属于化合反应。
(2)C是氧气,能支持呼吸,可用于医疗急救等。
(3)B与C的反应可以为碳在点燃条件下生成二氧化碳,反应的化学方程式为C+O₂$\frac{\underline{\;点燃\;}}{\;}$CO₂。
(4)E→C反应为过氧化氢在二氧化锰催化作用下生成氧气和水,化学方程式为2H₂O₂$\frac{\underline{\;MnO_2\;}}{\;}$O₂↑+2H₂O。
(1)化合
(2)用于医疗急救
(3)C+O₂$\frac{\underline{\;点燃\;}}{\;}$CO₂
(4)2H₂O₂$\frac{\underline{\;MnO_2\;}}{\;}$O₂↑+2H₂O解析:A、B、C、D、E分别由C、H、O中的一种或几种元素组成,通常状况下D、E为液体,A、C为气体,D、E、C之间转化符合过氧化氢在二氧化锰的催化作用下分解生成水和氧气;A为气体,B为黑色固体,A、B、C之间转化关系符合二氧化碳通过光合作用生成氧气,含碳物质燃烧生成二氧化碳。
(1)B生成A的反应为木炭和氧气反应生成二氧化碳,反应符合"多变一"特点,属于化合反应。
(2)C是氧气,能支持呼吸,可用于医疗急救等。
(3)B与C的反应可以为碳在点燃条件下生成二氧化碳,反应的化学方程式为C+O₂$\frac{\underline{\;点燃\;}}{\;}$CO₂。
(4)E→C反应为过氧化氢在二氧化锰催化作用下生成氧气和水,化学方程式为2H₂O₂$\frac{\underline{\;MnO_2\;}}{\;}$O₂↑+2H₂O。
20. (10 分)燃烧不仅可以帮助人们创造美好生活,同时也促进了工业的发展和人类文明的进步。某项目小组的同学以“家用燃料”为主题开展了项目化学习的探究之旅。
【项目一】燃烧是如何发生的
同学们用如图所示的装置进行实验,研究可燃物燃烧的条件。
已知:白磷的着火点为 $ 40^{\circ}C $,红磷的着火点为 $ 240^{\circ}C $;白磷燃烧的生成物有毒有害。
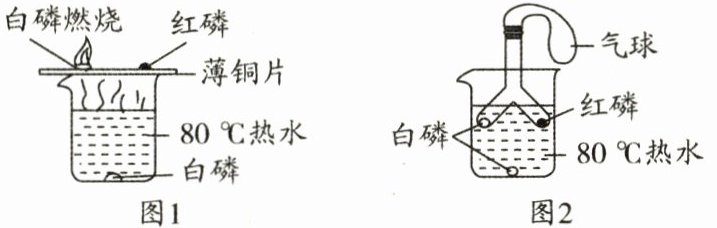
(1)图 1 中薄铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧需要的条件是
【项目二】家用燃料的合理使用
(一)燃烧燃料为了取暖
(2)同学们经过走访调查,了解到从前人们把煤制成蜂窝煤后燃烧会更加充分,请你从充分燃烧的角度解释这一现象:
(二)燃烧燃料为了照明
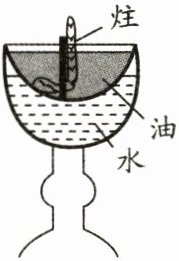
诗人陆游曾记载:“书灯惟瓷盏最省油,蜀中有夹瓷盏,一端作小窍,注清冷于其中,每夕一易之……可省油之半”。夹瓷盏是省油灯,用棉线做灯芯,上层盏盛油,下层盏内盛水。
(3)油燃烧时的能量转化形式是
【项目三】家用燃料的变迁和未来

同学们查阅资料,了解到家用燃料的更新历程如下:
(4)天然气和液化石油气中碳元素的质量分数分别约为 75%和 82.3%,通过该数据分析,用等质量的天然气和液化石油气作燃料,天然气更环保的原因是
(5)下列有关家用燃料更新的理由错误的是
A. 燃料使用更便捷
B. 固体燃料燃烧得更充分
C. 减少煤燃烧过程中产生的污染物
(6)通过研究家用燃料的更新历程,同学们预测未来燃料的发展方向是开发和利用清洁而又高效的能源。如氢能,氢气燃烧的化学方程式为
【项目一】燃烧是如何发生的
同学们用如图所示的装置进行实验,研究可燃物燃烧的条件。
已知:白磷的着火点为 $ 40^{\circ}C $,红磷的着火点为 $ 240^{\circ}C $;白磷燃烧的生成物有毒有害。

(1)图 1 中薄铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧需要的条件是
温度达到可燃物的着火点
;写出白磷燃烧的化学方程式:4P+5O₂$\frac{\underline{\;点燃\;}}{\;}$2P₂O₅
;利用图 1 实验证明可燃物燃烧的另一个条件,依据的现象是薄铜片上的白磷燃烧,而水中的白磷不燃烧
;与图 1 装置相比,利用图 2 装置进行实验的优点是更环保
。【项目二】家用燃料的合理使用
(一)燃烧燃料为了取暖
(2)同学们经过走访调查,了解到从前人们把煤制成蜂窝煤后燃烧会更加充分,请你从充分燃烧的角度解释这一现象:
增大了煤与氧气的接触面积
。(二)燃烧燃料为了照明

诗人陆游曾记载:“书灯惟瓷盏最省油,蜀中有夹瓷盏,一端作小窍,注清冷于其中,每夕一易之……可省油之半”。夹瓷盏是省油灯,用棉线做灯芯,上层盏盛油,下层盏内盛水。
(3)油燃烧时的能量转化形式是
化学
能转化为光能和热能,下层盏内盛水能达到省油的目的,原理是水吸热降温,减少油的挥发
。【项目三】家用燃料的变迁和未来

同学们查阅资料,了解到家用燃料的更新历程如下:
(4)天然气和液化石油气中碳元素的质量分数分别约为 75%和 82.3%,通过该数据分析,用等质量的天然气和液化石油气作燃料,天然气更环保的原因是
液化石油气中碳元素的含量比天然气高,燃烧等质量天然气和液化石油气,天然气排放的二氧化碳更少
。(5)下列有关家用燃料更新的理由错误的是
B
(填字母)。A. 燃料使用更便捷
B. 固体燃料燃烧得更充分
C. 减少煤燃烧过程中产生的污染物
(6)通过研究家用燃料的更新历程,同学们预测未来燃料的发展方向是开发和利用清洁而又高效的能源。如氢能,氢气燃烧的化学方程式为
2H₂+O₂$\frac{\underline{\;点燃\;}}{\;}$2H₂O
。
答案:
【项目一】
(1)温度达到可燃物的着火点 4P+5O₂$\frac{\underline{\;点燃\;}}{\;}$2P₂O₅ 薄铜片上的白磷燃烧,而水中的白磷不燃烧 更环保 【项目二】
(2)增大了煤与氧气的接触面积
(3)化学 水吸热降温,减少油的挥发
(4)液化石油气中碳元素的含量比天然气高,燃烧等质量天然气和液化石油气,天然气排放的二氧化碳更少
(5)B
(6)2H₂+O₂$\frac{\underline{\;点燃\;}}{\;}$2H₂O解析:
(1)图1中薄铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧需要的条件是温度达到可燃物的着火点;白磷在氧气中燃烧生成五氧化二磷,化学方程式为4P+5O₂$\frac{\underline{\;点燃\;}}{\;}$2P₂O₅;图1中薄铜片上的白磷与氧气接触且温度达到白磷的着火点,所以白磷燃烧;水中的白磷温度达到其着火点,但没有与氧气接触,所以白磷不燃烧,对比说明可燃物燃烧的另一个条件是与氧气接触;与图1装置相比,图2装置是在密闭环境中进行实验,避免了生成的五氧化二磷逸散到空气中造成的环境污染,优点是更环保。
(2)把煤制成蜂窝煤后燃烧会更加充分,是因为增大了煤与氧气的接触面积。
(3)油燃烧时的能量转化形式是化学能转化为光能和热能;下层盏内盛水能达到省灯油的目的,原理是水吸热降温,减少油的挥发。
(4)天然气和液化石油气中碳元素的质量分数分别约为75%和82.3%,用等质量的天然气和液化石油气作燃料,天然气更环保的原因是液化石油气中碳元素的含量比天然气高,燃烧等质量天然气和液化石油气,天然气排放的二氧化碳更少。
(5)燃料使用更便捷,与家用燃料更新有关,A不符合题意;相同条件下,气体燃料比固体燃料燃烧得更充分,B符合题意;减少煤燃烧过程中产生的污染物,与家用燃料更新有关,C不符合题意。故选B。
(6)氢气在氧气中燃烧生成水,化学方程式为2H₂+O₂$\frac{\underline{\;点燃\;}}{\;}$2H₂O。
(1)温度达到可燃物的着火点 4P+5O₂$\frac{\underline{\;点燃\;}}{\;}$2P₂O₅ 薄铜片上的白磷燃烧,而水中的白磷不燃烧 更环保 【项目二】
(2)增大了煤与氧气的接触面积
(3)化学 水吸热降温,减少油的挥发
(4)液化石油气中碳元素的含量比天然气高,燃烧等质量天然气和液化石油气,天然气排放的二氧化碳更少
(5)B
(6)2H₂+O₂$\frac{\underline{\;点燃\;}}{\;}$2H₂O解析:
(1)图1中薄铜片上的白磷燃烧而红磷不燃烧,说明可燃物燃烧需要的条件是温度达到可燃物的着火点;白磷在氧气中燃烧生成五氧化二磷,化学方程式为4P+5O₂$\frac{\underline{\;点燃\;}}{\;}$2P₂O₅;图1中薄铜片上的白磷与氧气接触且温度达到白磷的着火点,所以白磷燃烧;水中的白磷温度达到其着火点,但没有与氧气接触,所以白磷不燃烧,对比说明可燃物燃烧的另一个条件是与氧气接触;与图1装置相比,图2装置是在密闭环境中进行实验,避免了生成的五氧化二磷逸散到空气中造成的环境污染,优点是更环保。
(2)把煤制成蜂窝煤后燃烧会更加充分,是因为增大了煤与氧气的接触面积。
(3)油燃烧时的能量转化形式是化学能转化为光能和热能;下层盏内盛水能达到省灯油的目的,原理是水吸热降温,减少油的挥发。
(4)天然气和液化石油气中碳元素的质量分数分别约为75%和82.3%,用等质量的天然气和液化石油气作燃料,天然气更环保的原因是液化石油气中碳元素的含量比天然气高,燃烧等质量天然气和液化石油气,天然气排放的二氧化碳更少。
(5)燃料使用更便捷,与家用燃料更新有关,A不符合题意;相同条件下,气体燃料比固体燃料燃烧得更充分,B符合题意;减少煤燃烧过程中产生的污染物,与家用燃料更新有关,C不符合题意。故选B。
(6)氢气在氧气中燃烧生成水,化学方程式为2H₂+O₂$\frac{\underline{\;点燃\;}}{\;}$2H₂O。
查看更多完整答案,请扫码查看


