第55页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
7. (2024·泰州兴化质检)某课题组的同学通过数字化实验对白磷燃烧的温度变化及影响因素进行探究。将 5g 白磷加入试管中并将试管置于$60^{\circ }C$热水中,$t_{3}$时,推注$H_{2}O_{2}$溶液,实验装置及数据曲线如图所示。下列说法中,不正确的是 ( )
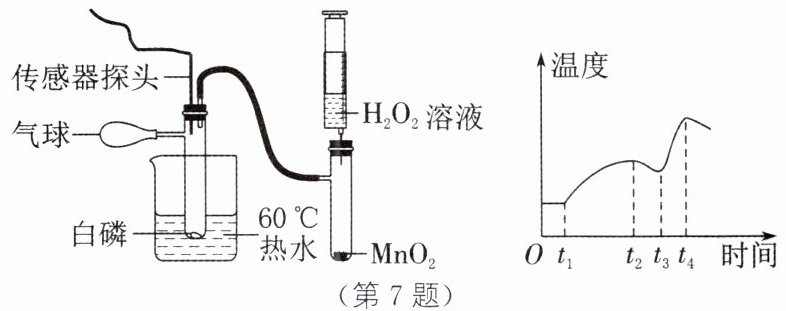
A.$t_{1}$时白磷开始燃烧
B.$t_{4}时温度大于t_{2}$说明氧气浓度越大,燃烧越剧烈
C.$t_{3}\sim t_{4}$对应温度升高说明过氧化氢分解放热
D.气球的作用是调节气压和防止生成的五氧化二磷污染空气

A.$t_{1}$时白磷开始燃烧
B.$t_{4}时温度大于t_{2}$说明氧气浓度越大,燃烧越剧烈
C.$t_{3}\sim t_{4}$对应温度升高说明过氧化氢分解放热
D.气球的作用是调节气压和防止生成的五氧化二磷污染空气
答案:
C 解析:t₁时温度升高,白磷开始燃烧,A选项正确;t₃时,推注H₂O₂溶液,H₂O₂在MnO₂的催化下分解生成氧气和水,t₄对应的温度高于t₂,说明氧气的浓度越大,燃烧越剧烈,放出的热量越多,B选项正确;t₃时,推注H₂O₂溶液,H₂O₂在MnO₂的催化下分解生成氧气和水,白磷与O₂接触,继续燃烧,放出大量热,故温度再次升高,C选项不正确;该实验中,白磷燃烧,放出热量,装置内气体受热膨胀,压强增大,故气球的作用是调节气压,防止压强过大,橡皮塞被冲出,白磷燃烧生成的五氧化二磷不能直接排放到空气中,会污染空气,所以气球可以收集五氧化二磷,防止污染空气,D选项正确。
8. 点燃不纯的可燃性气体可能会引发爆炸。如图所示为某同学改进的实验装置,请回答下列问题:

(1)如图甲所示为可燃性气体的洗气改进装置,检查它的气密性的方法是关闭止水夹,向导管 a 处 _,若 _,则装置气密性良好;若在导管 a 处通入可燃性气体,在导管 b 处连上尖嘴管并打开止水夹,点燃,即使气体不纯也不会发生爆炸,可见此装置的作用是 _。
(2)用图乙尖嘴管导出可燃性气体并点燃,也不会使管中气体爆炸,其原理是铜丝和水都可以 _。

(1)如图甲所示为可燃性气体的洗气改进装置,检查它的气密性的方法是关闭止水夹,向导管 a 处 _,若 _,则装置气密性良好;若在导管 a 处通入可燃性气体,在导管 b 处连上尖嘴管并打开止水夹,点燃,即使气体不纯也不会发生爆炸,可见此装置的作用是 _。
(2)用图乙尖嘴管导出可燃性气体并点燃,也不会使管中气体爆炸,其原理是铜丝和水都可以 _。
答案:
(1)通入气体 玻璃管内水面上升(或水从玻璃管中喷出) 作安全瓶(合理答案均可) (2)吸热,将温度降到气体的着火点以下 解析:(1)关闭止水夹,向导管a处通入气体,若装置气密性良好,则瓶内压强会变大,水会进入中间的玻璃管,因此通入气体,玻璃管内水面上升(或有水从玻璃管中喷出),即说明装置气密性良好;通入的气体即使不纯净,但由于火焰从b处进入瓶内就会熄灭,不会通过a处进入气体发生装置,因此该装置的作用是阻断燃烧,保护气体发生装置,是一个安全瓶。(2)铜丝和水都可以吸收热量,使温度降到气体的着火点以下,从而使火焰熄灭,保护气体发生装置。
9. ★(2024·清远质检)学校化学兴趣小组的同学欲探究物质燃烧的条件。
[查阅资料]白磷的着火点是$40^{\circ }C$,红磷的着火点是$240^{\circ }C$;$P_{2}O_{5}$能溶于水,有毒性。
[实验用品]药品:白磷、红磷、$80^{\circ }C$热水;仪器:漏斗、乳胶管、铁丝隔网等。

[实验装置]如图所示(夹持仪器已略去)。
[实验步骤]如表所示。
|实验步骤及操作|实验现象|
|Ⅰ.将一定量的白磷、红磷分别浸入$80^{\circ }C$热水中|白磷、红磷均不燃烧|
|Ⅱ.升高右侧漏斗至红磷露出水面| ▲ |
|Ⅲ. ▲ |白磷燃烧|

[讨论交流]
(1)实验步骤Ⅱ中的实验现象是 _,实验步骤Ⅲ中的操作是 _。
(2)本实验选择白磷与红磷作实验药品的原因:红磷和白磷都是 _,但红磷与白磷的 _不同。
(3)本实验中使用$80^{\circ }C$热水的作用是 _、 _。
(4)实验步骤Ⅰ中白磷不燃烧,Ⅲ中白磷燃烧,对比可得物质燃烧的条件是 _。
(5)步骤Ⅲ中反应的符号表达式为 _。
[拓展反思]
(6)本实验存在的不足之处是 _。
[查阅资料]白磷的着火点是$40^{\circ }C$,红磷的着火点是$240^{\circ }C$;$P_{2}O_{5}$能溶于水,有毒性。
[实验用品]药品:白磷、红磷、$80^{\circ }C$热水;仪器:漏斗、乳胶管、铁丝隔网等。

[实验装置]如图所示(夹持仪器已略去)。
[实验步骤]如表所示。
|实验步骤及操作|实验现象|
|Ⅰ.将一定量的白磷、红磷分别浸入$80^{\circ }C$热水中|白磷、红磷均不燃烧|
|Ⅱ.升高右侧漏斗至红磷露出水面| ▲ |
|Ⅲ. ▲ |白磷燃烧|

[讨论交流]
(1)实验步骤Ⅱ中的实验现象是 _,实验步骤Ⅲ中的操作是 _。
(2)本实验选择白磷与红磷作实验药品的原因:红磷和白磷都是 _,但红磷与白磷的 _不同。
(3)本实验中使用$80^{\circ }C$热水的作用是 _、 _。
(4)实验步骤Ⅰ中白磷不燃烧,Ⅲ中白磷燃烧,对比可得物质燃烧的条件是 _。
(5)步骤Ⅲ中反应的符号表达式为 _。
[拓展反思]
(6)本实验存在的不足之处是 _。
答案:
(1)红磷不燃烧 升高左侧漏斗至白磷露出水面 (2)可燃物 着火点 (3)提供热量 隔绝空气 (4)可燃物与空气接触 (5)${P + O_{2}->[点燃]P_{2}O_{5}}$ (6)没有处理反应生成的有毒物质 解析:(1)红磷的着火点为240°C,实验步骤Ⅱ中温度没有达到红磷的着火点,所以实验现象为红磷不燃烧。白磷的着火点是40°C,实验步骤Ⅲ中温度达到了白磷的着火点,实验现象为白磷燃烧,则白磷还需要与空气接触,故实验步骤Ⅲ操作为升高左侧漏斗至白磷露出水面。(2)本实验选择白磷与红磷作实验药品的原因:红磷和白磷都是可燃物,但红磷与白磷的着火点不同,便于探究燃烧的条件。(3)本实验中使用80°C热水的作用是提供热量以及隔绝氧气。(4)实验现象Ⅰ中白磷不燃烧,Ⅲ中白磷燃烧,区别在于白磷是否与空气接触,所以对比可得物质燃烧的条件之一是可燃物与空气接触。(5)实验步骤Ⅲ中是白磷在空气中燃烧生成五氧化二磷,反应的符号表达式为${P + O_{2}->[点燃]P_{2}O_{5}}$ (6)因为燃烧生成的五氧化二磷有毒,生成后会逸散到空气中,所以本实验的不足是没有处理反应生成的有毒物质。
查看更多完整答案,请扫码查看


