2025年新学案高中化学必修第二册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新学案高中化学必修第二册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第7页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
1.在常温下,Fe和Al遇浓硫酸和浓硝酸发生“钝化”,能否说明常温下浓$H_{2}SO_{4}$和浓$HNO_{3}$与Fe和Al都不反应?
答案:
不能。浓硫酸和浓硝酸具有强氧化性,常温下能将$Fe$、$Al$表面氧化生成致密的氧化膜,导致$Fe$、$Al$不能进一步与浓硫酸和浓硝酸反应,即金属发生了钝化。而钝化的过程就是浓硫酸和浓硝酸与$Fe$和$Al$反应的过程。
2.足量的铜与含2 mol $H_{2}SO_{4}$的浓硫酸反应,能否得到1 mol $SO_{2}$?足量的木炭与含2 mol $H_{2}SO_{4}$的浓硫酸反应,能否得到2 mol $SO_{2}$?
答案:
都不能。随着反应进行,硫酸浓度降低到一定程度后,与铜或木炭均不再发生反应。
3.浓硫酸具有强氧化性,稀硫酸不具有氧化性,对吗?
答案:
错。$H_{2}SO_{4}$中$ + 6$价的硫元素在化学反应中易得电子,故浓硫酸具有强氧化性。稀硫酸中存在$H_{2}SO_{4}=\!=\!=2H^{+}+SO_{4}^{2 - }$,$H^{+}$具有氧化性,能与活泼金属发生置换反应。故稀硫酸也具有氧化性,只是体现氧化性的是$H^{+}$。
4.浓硫酸具有强氧化性,能干燥$H_{2}$、CO、$SO_{2}$等还原性气体吗?
答案:
能。尽管$H_{2}$、$CO$、$SO_{2}$具有还原性,但均不与浓硫酸反应,故可用浓硫酸干燥。
5.浓硫酸能使蓝色胆矾变为白色,该过程体现了浓硫酸的脱水性还是吸水性?
答案:
体现了吸水性。浓硫酸的吸水性是指浓硫酸吸收水分子(如气体、液体中的水分子,吸收固体中的结晶水等)。
1.硫酸根离子实验探究
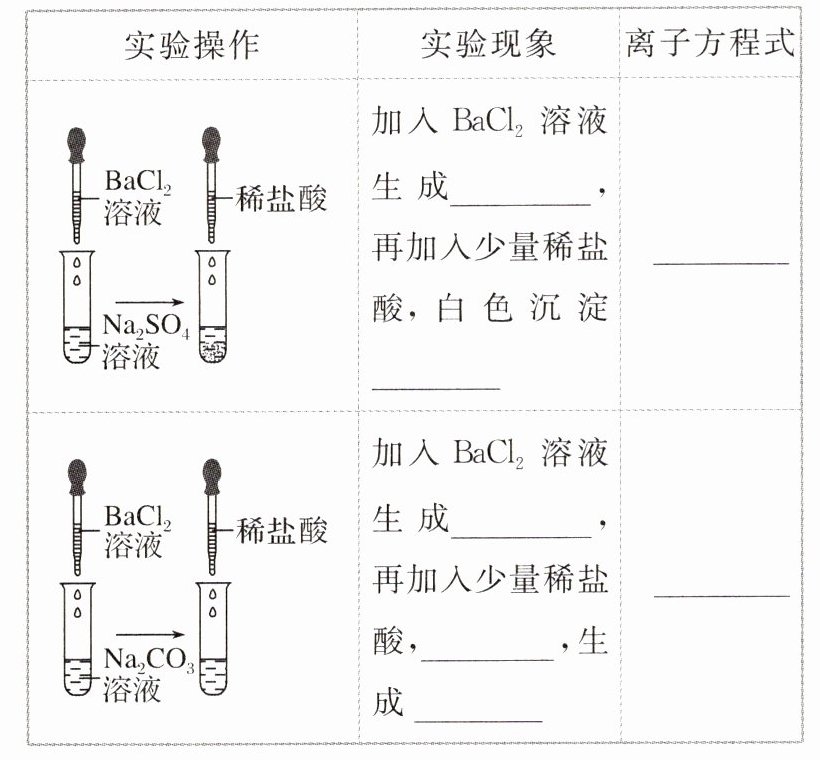

答案:
白色沉淀@@不溶解@@白色沉淀@@白色沉淀溶解@@无色无味气体
2.检验$SO_{4}^{2 - }$的正确操作方法
被检液$\xrightarrow{加足量盐酸酸化}$取清液$\xrightarrow{滴加BaCl_{2}溶液}$有无白色沉淀产生(判断有无$SO_{4}^{2 - }$)。
先加稀盐酸的目的是____________________。
被检液$\xrightarrow{加足量盐酸酸化}$取清液$\xrightarrow{滴加BaCl_{2}溶液}$有无白色沉淀产生(判断有无$SO_{4}^{2 - }$)。
先加稀盐酸的目的是____________________。
答案:
排除$CO_{3}^{2 - }$、$SO_{3}^{2 - }$、$Ag^{+}$的干扰
1.判断正误
(1)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀$HNO_{3}$,沉淀不溶解,则溶液中一定含有$SO_{4}^{2 - }$。 ( )
(2)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀盐酸,沉淀不溶解,则溶液中一定含有$SO_{4}^{2 - }$。 ( )
(3)为除去粗盐水中少量的$CO_{3}^{2 - }$,可向溶液中加入过量的$K_{2}CO_{3}$溶液,然后过滤。 ( )
(4)除去多种杂质时应考虑加入试剂的合理顺序。 ( )
(1)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀$HNO_{3}$,沉淀不溶解,则溶液中一定含有$SO_{4}^{2 - }$。 ( )
(2)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀盐酸,沉淀不溶解,则溶液中一定含有$SO_{4}^{2 - }$。 ( )
(3)为除去粗盐水中少量的$CO_{3}^{2 - }$,可向溶液中加入过量的$K_{2}CO_{3}$溶液,然后过滤。 ( )
(4)除去多种杂质时应考虑加入试剂的合理顺序。 ( )
答案:
×
@@×
@@×
@@√
@@×
@@×
@@√
2.某溶液中可能含有$SO_{4}^{2 - }$、$CO_{3}^{2 - }$、$Cl^{ - }$中的一种或几种,为确定该溶液的离子组成,现进行如下实验:
①取少量该溶液滴加硝酸钡溶液,产生白色沉淀;②滴加稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的无色气体,白色沉淀部分溶解;③取上层清液,继续滴加硝酸钡溶液至无沉淀时,再滴加硝酸银溶液,产生白色沉淀。根据上述实验,以下对原溶液的推测正确的是__________。
A.一定有$SO_{4}^{2 - }$
B.一定有$CO_{3}^{2 - }$
C.不能确定$Cl^{ - }$是否存在
D.不能确定$SO_{4}^{2 - }$是否存在
①取少量该溶液滴加硝酸钡溶液,产生白色沉淀;②滴加稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的无色气体,白色沉淀部分溶解;③取上层清液,继续滴加硝酸钡溶液至无沉淀时,再滴加硝酸银溶液,产生白色沉淀。根据上述实验,以下对原溶液的推测正确的是__________。
A.一定有$SO_{4}^{2 - }$
B.一定有$CO_{3}^{2 - }$
C.不能确定$Cl^{ - }$是否存在
D.不能确定$SO_{4}^{2 - }$是否存在
答案:
ABC
查看更多完整答案,请扫码查看


