2025年新学案高中化学必修第二册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新学案高中化学必修第二册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
(1)用途:
①重要的化工原料,可用于制__________、__________、炸药、染料、盐类等。
②用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等。
①重要的化工原料,可用于制__________、__________、炸药、染料、盐类等。
②用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等。
答案:
化肥@@农药
(2)硫酸的工业制法:
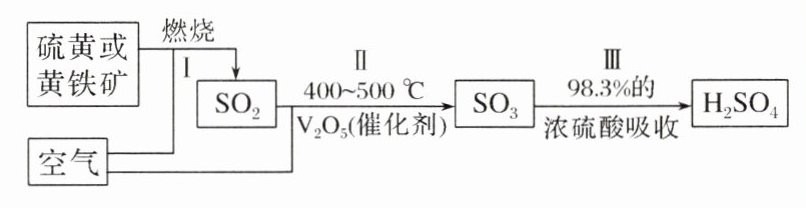
①写出以黄铁矿为原料制取硫酸各阶段的化学方程式:
Ⅰ.______________________________;
Ⅱ.______________________________;
Ⅲ.______________________________。
②工业上制取硫酸常用浓硫酸而不用水吸收$SO_{3}$,原因是______________________________。

①写出以黄铁矿为原料制取硫酸各阶段的化学方程式:
Ⅰ.______________________________;
Ⅱ.______________________________;
Ⅲ.______________________________。
②工业上制取硫酸常用浓硫酸而不用水吸收$SO_{3}$,原因是______________________________。
答案:
$4FeS_{2}+11O_{2}\stackrel{高温}{=\!=\!=}2Fe_{2}O_{3}+8SO_{2}$@@$2SO_{2}+O_{2}\underset{400~500^{\circ}C}{\overset{V_{2}O_{5}}{\rightleftharpoons}}2SO_{3}$@@$SO_{3}+H_{2}O=\!=\!=H_{2}SO_{4}$@@$SO_{3}$与水反应为放热反应,易产生酸雾,影响$SO_{3}$的吸收
2.硫酸的物理性质
(1)纯硫酸是无色、黏稠、_______挥发的油状液体,稀释时_______大量热。
(2)硫酸的密度大于水的密度,硫酸溶液中硫酸的质量分数越大,其密度越大;质量分数为98%的浓硫酸,密度为1.84 g/cm³。
(1)纯硫酸是无色、黏稠、_______挥发的油状液体,稀释时_______大量热。
(2)硫酸的密度大于水的密度,硫酸溶液中硫酸的质量分数越大,其密度越大;质量分数为98%的浓硫酸,密度为1.84 g/cm³。
答案:
难@@放出
【思考】 怎么稀释浓硫酸?
答案:
浓硫酸溶解时可放出大量的热;浓硫酸的稀释方法是将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃不断搅拌。
3.硫酸具有酸的共性


答案:
Fe + 2H^{+}=\!=\!=Fe^{2+}+H_{2}\uparrow@@MgO + 2H^{+}=\!=\!=Mg^{2+}+H_{2}O@@Mg(OH)_{2}+2H^{+}=\!=\!=Mg^{2+}+2H_{2}O@@CO_{3}^{2 - }+2H^{+}=\!=\!=CO_{2}\uparrow +H_{2}O@@红色
4.浓硫酸的特性
(1)吸水性:

(2)脱水性:
 |
|
(3)强氧化性:
实验探究:浓硫酸与铜的反应。
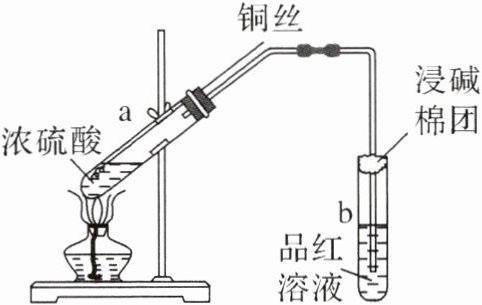

(1)吸水性:

(2)脱水性:
 |
|(3)强氧化性:
实验探究:浓硫酸与铜的反应。


答案:
蔗糖变黑,体积膨胀,变成疏松多孔的海绵状的炭,并释放出有刺激性气味的气体@@有气泡产生@@迅速褪色@@蓝@@$Cu + 2H_{2}SO_{4}(浓)\stackrel{\triangle}{=\!=\!=}CuSO_{4}+SO_{2}\uparrow +2H_{2}O$
查看更多完整答案,请扫码查看


