2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第67页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
14. (5分)我国科研团队开发出二氧化碳电催化转化制乙烯$(C_{2}H_{4})$的新技术,如图为其微观反应示意图(部分粒子未标出)。
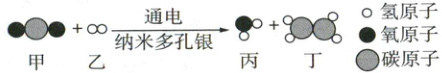
请回答下列问题:
(1) 从微观角度解释$CO_{2}$与$C_{2}H_{4}$化学性质不同的原因:_______。
(2) 乙的化学式为_______,该物质属于_______(填物质类别),该物质的一种用途是_______。
(3) 该反应的化学方程式为_______。

请回答下列问题:
(1) 从微观角度解释$CO_{2}$与$C_{2}H_{4}$化学性质不同的原因:_______。
(2) 乙的化学式为_______,该物质属于_______(填物质类别),该物质的一种用途是_______。
(3) 该反应的化学方程式为_______。
答案:
14
(1)分子构成不同
(2)H₂ 单质 作燃料(合理即可)
$(3)2CO₂ + 6H₂ \overset{通电}{=} C₂H₄ + 4H₂O $纳米多孔银
(1)分子构成不同
(2)H₂ 单质 作燃料(合理即可)
$(3)2CO₂ + 6H₂ \overset{通电}{=} C₂H₄ + 4H₂O $纳米多孔银
15. (5分)如图是工业上处理含$SO_{2}$的尾气和制备$CaSO_{4}$的工业流程图,$CaSO_{4}$是重要的化工原料,广泛用于建筑、医疗、环保等领域。
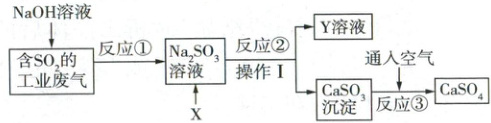
请回答下列问题:
(1) 反应①的化学方程式为
(2) 若$Y$溶液的溶质在流程中可循环利用,则反应②中加入的试剂$X$的化学式为
(3) 实验室进行操作Ⅰ时用到的玻璃仪器有玻璃棒、烧杯、
(4) 此流程能减少$SO_{2}$的排放,可缓解的环境问题是

请回答下列问题:
(1) 反应①的化学方程式为
2NaOH + SO₂ = Na₂SO₃ + H₂O
。(2) 若$Y$溶液的溶质在流程中可循环利用,则反应②中加入的试剂$X$的化学式为
Ca(OH)₂(或CaO)
。(3) 实验室进行操作Ⅰ时用到的玻璃仪器有玻璃棒、烧杯、
漏斗
,若得到的$Y$溶液浑浊,可能的原因是滤纸破损(或液面高于滤纸边缘、仪器不干净等,合理即可)
(写一点即可)。(4) 此流程能减少$SO_{2}$的排放,可缓解的环境问题是
酸雨
。
答案:
15
(1)2NaOH + SO₂ = Na₂SO₃ + H₂O
(2)Ca(OH)₂(或CaO)
(3)漏斗 滤纸破损(或液面高于滤纸边缘、仪器不干净等,合理即可)
(4)酸雨
(1)2NaOH + SO₂ = Na₂SO₃ + H₂O
(2)Ca(OH)₂(或CaO)
(3)漏斗 滤纸破损(或液面高于滤纸边缘、仪器不干净等,合理即可)
(4)酸雨
16. 新教材 铜与氧气反应前后质量的测定 (5分)根据如图所示装置进行实验,回答下列问题。
(1) 图1所示为制取并收集干燥的$CO_{2}$的装置。装置$B$的作用是
(2) 图2所示为加热铜粉验证质量守恒定律的实验装置。加热时发生反应的化学方程式为
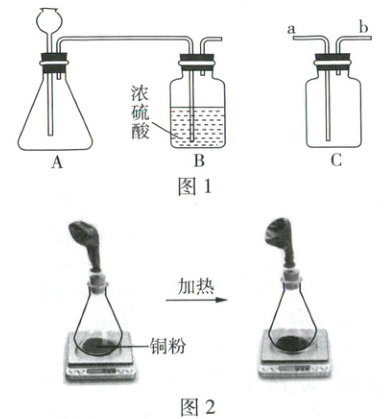
(1) 图1所示为制取并收集干燥的$CO_{2}$的装置。装置$B$的作用是
干燥CO₂(或干燥气体)
,用装置$C$收集$CO_{2}$时,气体应从导管口a
(填“$a$”或“$b$”)端通入。(2) 图2所示为加热铜粉验证质量守恒定律的实验装置。加热时发生反应的化学方程式为
2Cu + O₂ \overset{\triangle}{=} 2CuO
,装置中橡胶塞和气球的作用是形成密闭装置和调节瓶内气压
,若去掉气球,最终电子天平的示数会变大
(填“变大”“变小”或“不变”)。
答案:
16
(1)干燥CO₂(或干燥气体) a
$(2)2Cu + O₂ \overset{\triangle}{=} 2CuO $形成密闭装置和调节瓶内气压 变大
(1)干燥CO₂(或干燥气体) a
$(2)2Cu + O₂ \overset{\triangle}{=} 2CuO $形成密闭装置和调节瓶内气压 变大
17. 新教材 合理用药 (7分)$NaHCO_{3}$是治疗胃酸过多症的一种抗酸药。某兴趣小组在室温下,对$Na_{2}CO_{3}$是否适合作为抗酸药进行实验探究。
【查阅资料】①人体胃液(含有盐酸)的$pH$约为1.5,温度约为$37^{\circ}C$。
②抗酸药的标准之一:药物发生疗效时,胃液的$pH$保持在3~5最宜,$pH$过高会导致胃痛等不适症状。
(1) 小芳:$Na_{2}CO_{3}$适合作为抗酸药。其理由是
小松:$Na_{2}CO_{3}$不适合作为抗酸药。其原因可能是碱性较强。
【实验1】探究$NaHCO_{3}$与$Na_{2}CO_{3}$溶液碱性的强弱
(2) 小松用$pH$试纸依次测量等浓度的$Na_{2}CO_{3}$溶液和$NaHCO_{3}$溶液的$pH$,结果分别为11和8。$Na_{2}CO_{3}$溶液的碱性比$NaHCO_{3}$溶液
【实验2】探究$Na_{2}CO_{3}$作为抗酸药的适应性
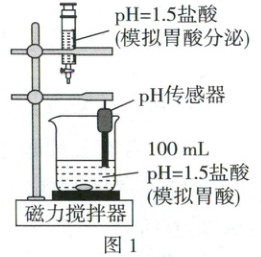
该小组利用图1装置,用自动注射器向烧杯中以1 mL/min的速度滴入$pH=1.5$的盐酸,再加入1.0 g $Na_{2}CO_{3}$固体,并持续搅拌。记录溶液$pH$随时间的变化曲线。
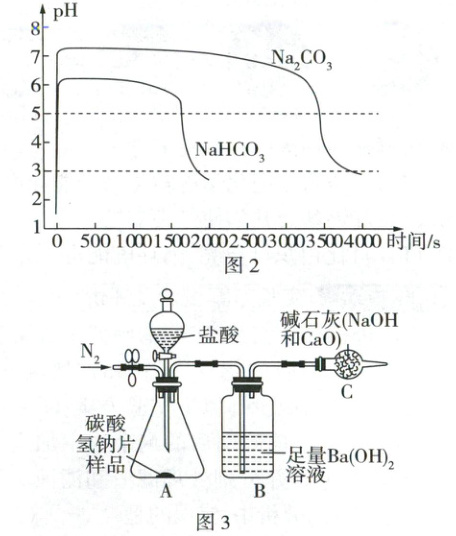
将上述实验中的$Na_{2}CO_{3}$换成等量的$NaHCO_{3}$,重复实验过程。所得两条曲线如图2所示。
(3) 由图2可知$Na_{2}CO_{3}$不适合作为抗酸药,原因是
(4) 从控制变量和对比实验的角度来看,“实验2”设计
【拓展实验】市售的碳酸氢钠片中含有淀粉、硬脂酸镁等辅料,小组同学设计图3所示装置测定市售的碳酸氢钠片中$NaHCO_{3}$的质量分数(碳酸氢钠片中辅料遇酸不产生气体),向装置$A$中缓慢滴加足量盐酸,充分反应后,通入一段时间$N_{2}$,将装置$B$中的$BaCO_{3}$沉淀过滤、洗涤、干燥、称量,计算得出实验结果。已知:装置$B$中相关反应的化学方程式为$CO_{2}+Ba(OH)_{2}=BaCO_{3}\downarrow +H_{2}O$。
(5) 当装置$A$中物质充分反应后,通入一段时间$N_{2}$,目的是
【查阅资料】①人体胃液(含有盐酸)的$pH$约为1.5,温度约为$37^{\circ}C$。
②抗酸药的标准之一:药物发生疗效时,胃液的$pH$保持在3~5最宜,$pH$过高会导致胃痛等不适症状。
(1) 小芳:$Na_{2}CO_{3}$适合作为抗酸药。其理由是
Na₂CO₃ + 2HCl = 2NaCl + H₂O + CO₂↑
(用化学方程式表示)。小松:$Na_{2}CO_{3}$不适合作为抗酸药。其原因可能是碱性较强。
【实验1】探究$NaHCO_{3}$与$Na_{2}CO_{3}$溶液碱性的强弱
(2) 小松用$pH$试纸依次测量等浓度的$Na_{2}CO_{3}$溶液和$NaHCO_{3}$溶液的$pH$,结果分别为11和8。$Na_{2}CO_{3}$溶液的碱性比$NaHCO_{3}$溶液
强
(填“强”或“弱”)。【实验2】探究$Na_{2}CO_{3}$作为抗酸药的适应性
该小组利用图1装置,用自动注射器向烧杯中以1 mL/min的速度滴入$pH=1.5$的盐酸,再加入1.0 g $Na_{2}CO_{3}$固体,并持续搅拌。记录溶液$pH$随时间的变化曲线。
将上述实验中的$Na_{2}CO_{3}$换成等量的$NaHCO_{3}$,重复实验过程。所得两条曲线如图2所示。
(3) 由图2可知$Na_{2}CO_{3}$不适合作为抗酸药,原因是
Na₂CO₃反应时造成胃液pH远大于5,且pH>5持续时间较长,会导致胃痛等不适症状,故Na₂CO₃不适合作为抗酸药。
。(4) 从控制变量和对比实验的角度来看,“实验2”设计
不严谨
(填“严谨”或“不严谨”),理由是没有模拟人体温度37℃进行对比实验
。【拓展实验】市售的碳酸氢钠片中含有淀粉、硬脂酸镁等辅料,小组同学设计图3所示装置测定市售的碳酸氢钠片中$NaHCO_{3}$的质量分数(碳酸氢钠片中辅料遇酸不产生气体),向装置$A$中缓慢滴加足量盐酸,充分反应后,通入一段时间$N_{2}$,将装置$B$中的$BaCO_{3}$沉淀过滤、洗涤、干燥、称量,计算得出实验结果。已知:装置$B$中相关反应的化学方程式为$CO_{2}+Ba(OH)_{2}=BaCO_{3}\downarrow +H_{2}O$。
(5) 当装置$A$中物质充分反应后,通入一段时间$N_{2}$,目的是
将反应生成的CO₂全部赶入装置B让其充分吸收
,装置$C$的作用是防止空气中的CO₂进入装置B,引起误差
。

答案:
17
(1)Na₂CO₃ + 2HCl = 2NaCl + H₂O + CO₂↑
(2)强
(3)Na₂CO₃反应时造成胃液pH远大于5,且pH>5持续时间较长,会导致胃痛等不适症状,故Na₂CO₃不适合作为抗酸药。
(4)不严谨 没有模拟人体温度37℃进行对比实验
(5)将反应生成的CO₂全部赶入装置B让其充分吸收 防止空气中的CO₂进入装置B,引起误差
(1)Na₂CO₃ + 2HCl = 2NaCl + H₂O + CO₂↑
(2)强
(3)Na₂CO₃反应时造成胃液pH远大于5,且pH>5持续时间较长,会导致胃痛等不适症状,故Na₂CO₃不适合作为抗酸药。
(4)不严谨 没有模拟人体温度37℃进行对比实验
(5)将反应生成的CO₂全部赶入装置B让其充分吸收 防止空气中的CO₂进入装置B,引起误差
查看更多完整答案,请扫码查看


