2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第51页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
14. (6分)我国科学家利用高效催化剂进行人工固氮,下图是该反应的微观示意图。
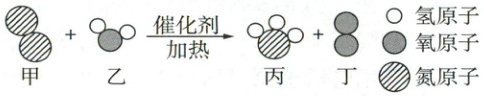
请回答下列问题:
(1)从微观角度分析,图中的反应遵守质量守恒定律的原因是
(2)甲在生活中常见的用途是
(3)该反应中化合价降低的元素是
(4)该反应的化学方程式为
(5)若有30g甲和54g乙混合发生上述反应,理论上生成丁的质量为

请回答下列问题:
(1)从微观角度分析,图中的反应遵守质量守恒定律的原因是
反应前后原子种类、数目、质量不变
。(2)甲在生活中常见的用途是
作保护气(合理即可)
。(3)该反应中化合价降低的元素是
N
(填元素符号)。(4)该反应的化学方程式为
$2N₂ + 6H₂O\stackrel{催化剂}{\underset{\triangle}{=\!=\!=}}4NH₃ + 3O₂$
,属于的基本反应类型是置换反应
。(5)若有30g甲和54g乙混合发生上述反应,理论上生成丁的质量为
48
g。
答案:
(1)反应前后原子种类、数目、质量不变
(2)作保护气(合理即可)
$(3)N (4)2N₂ + 6H₂O\stackrel{催化剂}{\underset{\triangle}{=\!=\!=}}4NH₃ + 3O₂ $置换反应
(5)48
【解题思路】甲是N₂,乙是H₂O,丙是NH₃,丁是O₂,反应的化学方程式及各元素的化合价和质量关系为

(1)反应前后原子种类、数目、质量不变
(2)作保护气(合理即可)
$(3)N (4)2N₂ + 6H₂O\stackrel{催化剂}{\underset{\triangle}{=\!=\!=}}4NH₃ + 3O₂ $置换反应
(5)48
【解题思路】甲是N₂,乙是H₂O,丙是NH₃,丁是O₂,反应的化学方程式及各元素的化合价和质量关系为

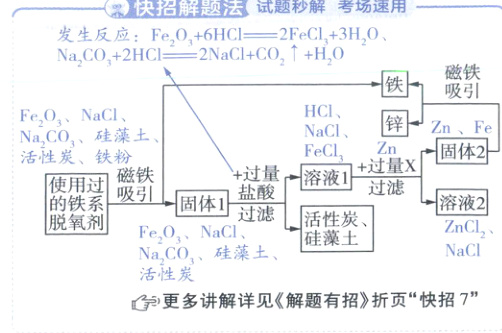
15. (5分)保护金属资源的有效途径之一是金属的回收利用。已知使用过的某铁系脱氧剂中含有氧化铁、氯化钠、碳酸钠、硅藻土、活性炭、铁粉。同学们设计了如图所示回收铁的流程。
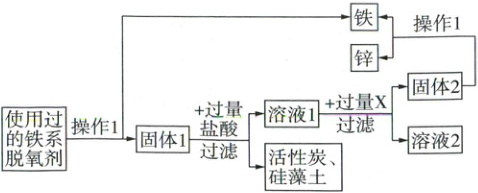
资料卡:(1)硅藻土不溶于水和酸;(2)FeCl₃溶液与Fe、Zn均能反应生成FeCl₂。
(1)操作1为
(2)加过量盐酸时,固体1中的氧化物发生反应的化学方程式为
(3)过滤时滤纸没有紧贴漏斗内壁,可能造成的后果是
(4)试剂X为

资料卡:(1)硅藻土不溶于水和酸;(2)FeCl₃溶液与Fe、Zn均能反应生成FeCl₂。
(1)操作1为
用磁铁吸引
。(2)加过量盐酸时,固体1中的氧化物发生反应的化学方程式为
Fe₂O₃ + 6HCl =\!=\!= 2FeCl₃ + 3H₂O
,溶液1的溶质为HCl、FeCl₃、NaCl
。(3)过滤时滤纸没有紧贴漏斗内壁,可能造成的后果是
过滤速度过慢
。(4)试剂X为
Zn
(写化学式)。
答案:
(1)用磁铁吸引
(2)Fe₂O₃ + 6HCl =\!=\!= 2FeCl₃ + 3H₂O HCl、FeCl₃、NaCl
(3)过滤速度过慢
(4)Zn
(1)用磁铁吸引
(2)Fe₂O₃ + 6HCl =\!=\!= 2FeCl₃ + 3H₂O HCl、FeCl₃、NaCl
(3)过滤速度过慢
(4)Zn

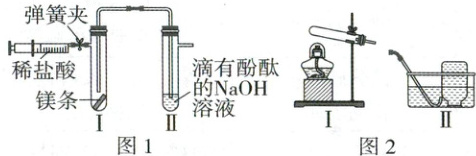
16. (5分)根据下图所示的实验回答下列问题。
(1)图1是证明氢氧化钠与稀盐酸发生中和反应的实验。打开弹簧夹,将足量稀盐酸一次性推入试管Ⅰ中,关闭弹簧夹(保持导管口在液面以下),试管Ⅰ中观察到的现象是
(2)图2是实验室用高锰酸钾制取并收集氧气的装置。选择Ⅰ作为该反应的发生装置,依据是
(1)图1是证明氢氧化钠与稀盐酸发生中和反应的实验。打开弹簧夹,将足量稀盐酸一次性推入试管Ⅰ中,关闭弹簧夹(保持导管口在液面以下),试管Ⅰ中观察到的现象是
有气泡产生
;一段时间后有液体从试管Ⅰ中流入试管Ⅱ中,试管Ⅱ中的溶液由红色变为无色且无沉淀产生
,由此说明氢氧化钠全部被稀盐酸消耗了。(2)图2是实验室用高锰酸钾制取并收集氧气的装置。选择Ⅰ作为该反应的发生装置,依据是
反应物是固体且反应条件为加热
。为了防止粉末状试剂进入导管,还需要进行的改进是试管口放一团棉花
;Ⅱ中当观察到导管口有连续均匀的气泡冒出
时开始收集气体。
答案:
(1)有气泡产生 无沉淀产生
(2)反应物是固体且反应条件为加热 试管口放一团棉花
导管口有连续均匀的气泡冒出
【解题思路】
(1)进入试管Ⅱ中的溶液中一定含有盐酸和氯化镁,盐酸与氢氧化钠优先反应,且盐酸将氢氧化钠全部消耗,说明没有发生氯化镁和氢氧化钠的反应,所以可观察到无白色沉淀产生。
(1)有气泡产生 无沉淀产生
(2)反应物是固体且反应条件为加热 试管口放一团棉花
导管口有连续均匀的气泡冒出
【解题思路】
(1)进入试管Ⅱ中的溶液中一定含有盐酸和氯化镁,盐酸与氢氧化钠优先反应,且盐酸将氢氧化钠全部消耗,说明没有发生氯化镁和氢氧化钠的反应,所以可观察到无白色沉淀产生。
17. (7分)端午节的传统美食——碱水粽子,是在糯米中加入适量的碱水,用老黄箬叶裹扎。煮熟后糯米变成浅黄色,可蘸白糖吃,清香可口。某兴趣小组围绕碱水粽子展开探究。
探究一 碱水粽子富含的营养物质
小组同学观察到碱水粽子主要原料为糯米、红豆等,含有蛋白质、糖类、维生素、矿物质等多种营养物质,其中可以供能的营养物质是_______。
探究二 碱水的成分
【查阅资料】
①传统碱水由草木灰浸泡过滤制得。
②草木灰的主要成分为钾盐,可能含有碳酸钾、硫酸钾和氯化钾中的一种或几种。
③AgCl和BaSO₄都是既不溶于水,也不溶于酸的白色沉淀。
【提出问题】“碱水”的主要成分是什么?
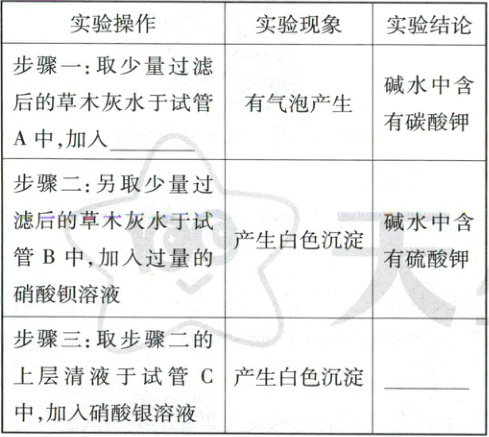
【实验】
【结论】“碱水”的主要成分是碳酸钾、硫酸钾和氯化钾。
【反思与交流】
(1)晓强对步骤二的结论产生怀疑,理由是_______(用化学方程式解释),同学们提出不需要进行步骤一实验,只需向步骤二的白色沉淀中加入稀盐酸,若观察到_______,即可证明碱水中同时含有碳酸钾和硫酸钾。
(2)现代生活中制作碱水粽子时常用碳酸钠代替草木灰水,碳酸钠俗称_______。(写出一种即可)
探究三 警惕“返青粽叶”的危害
不法商贩将粽叶经硫酸铜浸泡后得到“返青粽叶”,人们长期食用有害健康。向粽叶浸泡后得到的溶液中加入_______可检验某粽叶是否经硫酸铜处理。
探究一 碱水粽子富含的营养物质
小组同学观察到碱水粽子主要原料为糯米、红豆等,含有蛋白质、糖类、维生素、矿物质等多种营养物质,其中可以供能的营养物质是_______。
探究二 碱水的成分
【查阅资料】
①传统碱水由草木灰浸泡过滤制得。
②草木灰的主要成分为钾盐,可能含有碳酸钾、硫酸钾和氯化钾中的一种或几种。
③AgCl和BaSO₄都是既不溶于水,也不溶于酸的白色沉淀。
【提出问题】“碱水”的主要成分是什么?
【实验】
【结论】“碱水”的主要成分是碳酸钾、硫酸钾和氯化钾。
【反思与交流】
(1)晓强对步骤二的结论产生怀疑,理由是_______(用化学方程式解释),同学们提出不需要进行步骤一实验,只需向步骤二的白色沉淀中加入稀盐酸,若观察到_______,即可证明碱水中同时含有碳酸钾和硫酸钾。
(2)现代生活中制作碱水粽子时常用碳酸钠代替草木灰水,碳酸钠俗称_______。(写出一种即可)
探究三 警惕“返青粽叶”的危害
不法商贩将粽叶经硫酸铜浸泡后得到“返青粽叶”,人们长期食用有害健康。向粽叶浸泡后得到的溶液中加入_______可检验某粽叶是否经硫酸铜处理。

答案:
探究一:糖类和蛋白质
探究二:稀盐酸(合理即可) 碱水中含有氯化钾
【反思与交流】
(1) $Ba(NO_{3})_{2} + K_{2}CO_{3} = BaCO_{3}\downarrow + 2KNO_{3}$ 沉淀部分溶解,有气泡产生
(2) 纯碱(或苏打)
探究三:铁钉(合理即可)
探究二:稀盐酸(合理即可) 碱水中含有氯化钾
【反思与交流】
(1) $Ba(NO_{3})_{2} + K_{2}CO_{3} = BaCO_{3}\downarrow + 2KNO_{3}$ 沉淀部分溶解,有气泡产生
(2) 纯碱(或苏打)
探究三:铁钉(合理即可)
查看更多完整答案,请扫码查看


