2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第26页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
9. 通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图。下列说法正确的是(

A.物质乙、丙、丁都由分子构成
B.物质乙中氢、氮元素的质量比为3:1
C.反应中物质乙和丙的质量比为2:1
D.参加反应的乙和生成的丁中氢元素质量不一定相等
A
)
A.物质乙、丙、丁都由分子构成
B.物质乙中氢、氮元素的质量比为3:1
C.反应中物质乙和丙的质量比为2:1
D.参加反应的乙和生成的丁中氢元素质量不一定相等
答案:
9 A 快招解题法 试题秒解 考场速用
第1步:写出各物质的化学式。
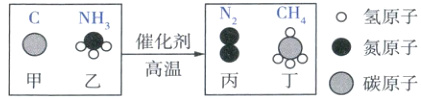
第2步:写出反应的化学方程式,注意配平。
3C + 4NH₃$\xlongequal[高温]{催化剂}$2N₂ + 3CH₄
第3步:结合化学方程式,分析选项。
A(√)NH₃、N₂、CH₄都由分子构成。
B(×)乙中氢、氮元素的质量比为3:14(注意区分原子个数比与元素质量比)。
C(×)反应中物质乙和丙的质量比为(4×17):28 = 17:7。
D(×)根据质量守恒定律,化学反应前后元素种类和质量不变,甲、丙中均不含氢元素,则参加反应的乙和生成的丁中氢元素质量一定相等。
更多讲解详见《解题有招》折页“快招3”
名师讲方法
思维导引
配平化学方程式的一般思路
配平C + NH₃——N₂ + CH₄
①找出组成最复杂物质的化学式→可以选择CH₄
②使找出的化学式的化学计量数为“1”→C + NH₃——N₂ + 1CH₄
③配平其他物质的化学式→1C + 4/3NH₃——2/3N₂ + 1CH₄
④通分,将分数化为整数并将“——”变“══”→3C + 4NH₃ ══ 2N₂ + 3CH₄
配平后注意检查,标注反应条件及生成物状态符号。
9 A 快招解题法 试题秒解 考场速用
第1步:写出各物质的化学式。

第2步:写出反应的化学方程式,注意配平。
3C + 4NH₃$\xlongequal[高温]{催化剂}$2N₂ + 3CH₄
第3步:结合化学方程式,分析选项。
A(√)NH₃、N₂、CH₄都由分子构成。
B(×)乙中氢、氮元素的质量比为3:14(注意区分原子个数比与元素质量比)。
C(×)反应中物质乙和丙的质量比为(4×17):28 = 17:7。
D(×)根据质量守恒定律,化学反应前后元素种类和质量不变,甲、丙中均不含氢元素,则参加反应的乙和生成的丁中氢元素质量一定相等。
更多讲解详见《解题有招》折页“快招3”
名师讲方法
思维导引
配平化学方程式的一般思路
配平C + NH₃——N₂ + CH₄
①找出组成最复杂物质的化学式→可以选择CH₄
②使找出的化学式的化学计量数为“1”→C + NH₃——N₂ + 1CH₄
③配平其他物质的化学式→1C + 4/3NH₃——2/3N₂ + 1CH₄
④通分,将分数化为整数并将“——”变“══”→3C + 4NH₃ ══ 2N₂ + 3CH₄
配平后注意检查,标注反应条件及生成物状态符号。
10. 下图所示图像中,不能正确反映对应关系的是(

A.高温煅烧石灰石
B.加热含空气的密闭容器中的铜粉
C.向一定量的稀盐酸中滴加氢氧化钠溶液
D.向一定量硫酸和硫酸铜混合溶液中滴加氢氧化钠溶液
B
)
A.高温煅烧石灰石
B.加热含空气的密闭容器中的铜粉
C.向一定量的稀盐酸中滴加氢氧化钠溶液
D.向一定量硫酸和硫酸铜混合溶液中滴加氢氧化钠溶液
答案:
10 B 快招解题法 试题秒解 考场速用
A(√)高温煅烧石灰石,发生反应CaCO₃$\xlongequal{高温}$CaO + CO₂↑,随着反应的进行,二氧化碳逸出,剩余固体的质量逐渐减小,但钙元素的质量不变,则固体中钙元素的质量分数逐渐增大,至完全反应,不再发生改变。
B(×)加热含空气的密闭容器中的铜粉,发生反应2Cu + O₂$\xlongequal{\triangle}$2CuO,随着反应的进行,固体的质量逐渐增大,至氧气完全反应,不再发生改变,正确图像如图所示。
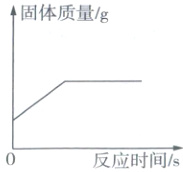
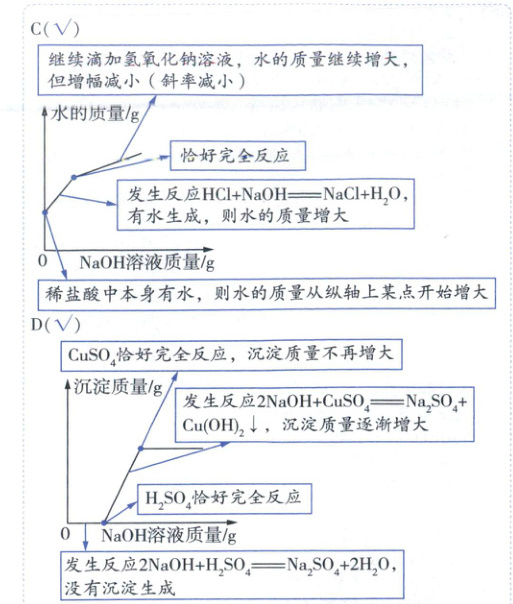
10 B 快招解题法 试题秒解 考场速用
A(√)高温煅烧石灰石,发生反应CaCO₃$\xlongequal{高温}$CaO + CO₂↑,随着反应的进行,二氧化碳逸出,剩余固体的质量逐渐减小,但钙元素的质量不变,则固体中钙元素的质量分数逐渐增大,至完全反应,不再发生改变。
B(×)加热含空气的密闭容器中的铜粉,发生反应2Cu + O₂$\xlongequal{\triangle}$2CuO,随着反应的进行,固体的质量逐渐增大,至氧气完全反应,不再发生改变,正确图像如图所示。


11. (4分)诗人陆游的笔记中记载“书灯勿用铜盏,惟瓷盏最省油,蜀中有夹瓷盏……可省油之半”“一端作小窍(孔),注清冷水于其中,每夕一易(更换)之”。夹瓷盏被称为省油灯,其结构如图所示,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水。
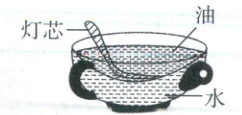
(1)陆游笔记中提到的“用棉绳做炷”中,“棉绳”的材质属于
(2)“书灯勿用铜盛”是因为铜具有良好的
(3)如图所示夹瓷盏省油的原理:油燃烧放热,上层盏内的油温升高,利于灯芯吸附灯油燃烧照明;下层盏内的水起到
(4)“注清冷水于其中,每夕一易(更换)之”。下列对“盏中水减少”的微观解释正确的是
a. 水分子受热分解
b. 水分子不断运动,盏中水分子数目减少
c. 水分子间的间隔变大,水由液态变气态

(1)陆游笔记中提到的“用棉绳做炷”中,“棉绳”的材质属于
天然高分子材料
(填“金属材料”“合成材料”或“天然高分子材料”)。(2)“书灯勿用铜盛”是因为铜具有良好的
导热
性,易造成油的挥发。(3)如图所示夹瓷盏省油的原理:油燃烧放热,上层盏内的油温升高,利于灯芯吸附灯油燃烧照明;下层盏内的水起到
吸热(合理即可)
作用,可减少油的挥发,以达到省油的目的。(4)“注清冷水于其中,每夕一易(更换)之”。下列对“盏中水减少”的微观解释正确的是
bc
(填字母)。a. 水分子受热分解
b. 水分子不断运动,盏中水分子数目减少
c. 水分子间的间隔变大,水由液态变气态
答案:
11
(1)天然高分子材料
(2)导热
(3)吸热(合理即可)
(4)bc
【解题思路】
(4)A(×)盏中水减少,是因为水受热变成水蒸气,没有分解。
B(√)盏中水减少,是因为水分子在不断运动,盏中的部分水分子运动到空气中,使盏中水分子数目减少。
C(√)盏中水减少,是因为水受热变成水蒸气,水分子间的间隔变大,水由液态变气态。
(1)天然高分子材料
(2)导热
(3)吸热(合理即可)
(4)bc
【解题思路】
(4)A(×)盏中水减少,是因为水受热变成水蒸气,没有分解。
B(√)盏中水减少,是因为水分子在不断运动,盏中的部分水分子运动到空气中,使盏中水分子数目减少。
C(√)盏中水减少,是因为水受热变成水蒸气,水分子间的间隔变大,水由液态变气态。
12. (4分)如图是实验室制取气体的常用装置。请根据要求回答问题。

(1)仪器①的名称为
(2)实验室制取氧气,若发生装置选用A,则选用的试剂为
(3)实验室用大理石和稀盐酸反应制取CO₂,应选用的发生装置是
(4)实验室制取CO₂和O₂均不能选用的收集装置是

(1)仪器①的名称为
水槽
。(2)实验室制取氧气,若发生装置选用A,则选用的试剂为
KMnO₄
。(3)实验室用大理石和稀盐酸反应制取CO₂,应选用的发生装置是
B
(填字母)。(4)实验室制取CO₂和O₂均不能选用的收集装置是
D
(填字母)。
答案:
12
(1)水槽
(2)KMnO₄
(3)B
(4)D
【解题思路】
(4)O₂:不易溶于水→排水法
O₂:密度比空气大且不与空气中成分反应→向上排空气法
CO₂:密度比空气大且不与空气中成分反应→向上排空气法收集
名师敲重点
归纳总结
实验室常见发生装置和收集装置的选择
(1)实验室制取气体的装置包括发生装置和收集装置,发生装置的选择依据是反应条件和反应物的状态;收集装置的选择依据是气体的密度、在水中的溶解性、是否与空气中成分反应,常用的有排水法、向上排空气法、向下排空气法。
(2)常见的发生装置

12
(1)水槽
(2)KMnO₄
(3)B
(4)D
【解题思路】
(4)O₂:不易溶于水→排水法
O₂:密度比空气大且不与空气中成分反应→向上排空气法
CO₂:密度比空气大且不与空气中成分反应→向上排空气法收集
名师敲重点
归纳总结
实验室常见发生装置和收集装置的选择
(1)实验室制取气体的装置包括发生装置和收集装置,发生装置的选择依据是反应条件和反应物的状态;收集装置的选择依据是气体的密度、在水中的溶解性、是否与空气中成分反应,常用的有排水法、向上排空气法、向下排空气法。
(2)常见的发生装置

13. (5分)海水中氯化钠的质量分数大约在3.5%左右,人类从海水中提取并提纯氯化钠用于生活和生产。海水晒盐的大致过程如图所示。请回答下列问题。

(1)科学家依据溶液的
(2)海水晒盐利用了氯化钠的溶解度随温度变化的规律是
(3)图中,实现母液和粗盐分离的操作是
(4)下列对图示海水晒盐的过程中,各成分的分析正确的是
A. 海水由储水池引入蒸发池,海水中氯化钠的质量不变
B. 结晶池结晶过程中,溶液中氯化钠的质量不变
C. 析出晶体后的母液是氯化钠的不饱和溶液

(1)科学家依据溶液的
均一
(填“均一”或“稳定”)性,通过测定海水样品中氯化钠的质量占比,得出海水中氯化钠的质量分数。若海水中氯化钠的质量分数为3.5%,则每吨海水理论上可提取氯化钠35
kg。(2)海水晒盐利用了氯化钠的溶解度随温度变化的规律是
氯化钠溶解度受温度影响变化不大(合理即可)
。(3)图中,实现母液和粗盐分离的操作是
过滤
。(4)下列对图示海水晒盐的过程中,各成分的分析正确的是
A
(填字母)。A. 海水由储水池引入蒸发池,海水中氯化钠的质量不变
B. 结晶池结晶过程中,溶液中氯化钠的质量不变
C. 析出晶体后的母液是氯化钠的不饱和溶液
答案:
13
(1)均一 35
(2)氯化钠溶解度受温度影响变化不大(合理即可)
(3)过滤
(4)A
【解题思路】
(1)1吨 = 1000kg,海水中氯化钠质量分数为3.5%,则每吨海水中氯化钠的质量为1000kg×3.5% = 35kg。
(4)A(√)海水由储水池引入蒸发池,只是位置改变,没有发生化学变化,海水中氯化钠的质量不变。
B(×)结晶池结晶过程中,氯化钠不断结晶析出,溶液中氯化钠的质量减小。
C(√)析出晶体,说明氯化钠不能继续溶解,则母液是氯化钠的饱和溶液。
(1)均一 35
(2)氯化钠溶解度受温度影响变化不大(合理即可)
(3)过滤
(4)A
【解题思路】
(1)1吨 = 1000kg,海水中氯化钠质量分数为3.5%,则每吨海水中氯化钠的质量为1000kg×3.5% = 35kg。
(4)A(√)海水由储水池引入蒸发池,只是位置改变,没有发生化学变化,海水中氯化钠的质量不变。
B(×)结晶池结晶过程中,氯化钠不断结晶析出,溶液中氯化钠的质量减小。
C(√)析出晶体,说明氯化钠不能继续溶解,则母液是氯化钠的饱和溶液。
查看更多完整答案,请扫码查看


