2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第18页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
9. 物质的检验、鉴别和除杂是科学探究的重要组成部分。下列实验方案设计正确的是(
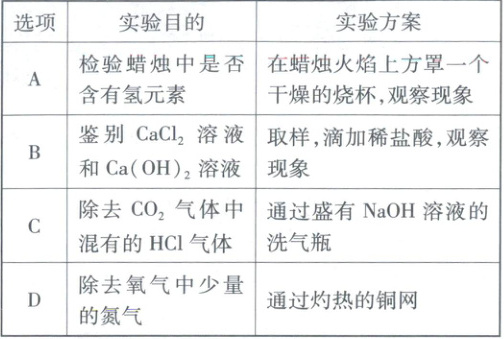
A
)
答案:
9 A A(√)在蜡烛火焰上方罩一个干燥的烧杯,烧杯内壁出现水雾,说明蜡烛燃烧生成了水,水是由氢元素和氧元素组成的,反应物氧气中只含有氧元素,则蜡烛中一定含有氢元素。
B(×)$\mathrm{CaCl_2 + HCl}$,不反应,无明显现象
$\mathrm{Ca(OH)_2 + 2HCl \xlongequal{} CaCl_2 + 2H_2O}$,能反应,但无明显现象
同时除去原物质
C(×)$\mathrm{CO_2 + 2NaOH \xlongequal{} Na_2CO_3 + H_2O}$和杂质,故
$\mathrm{HCl + NaOH \xlongequal{} NaCl + H_2O}$
D(×)氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,除去原物质,不符合除杂原则。
B(×)$\mathrm{CaCl_2 + HCl}$,不反应,无明显现象
$\mathrm{Ca(OH)_2 + 2HCl \xlongequal{} CaCl_2 + 2H_2O}$,能反应,但无明显现象
同时除去原物质
C(×)$\mathrm{CO_2 + 2NaOH \xlongequal{} Na_2CO_3 + H_2O}$和杂质,故
$\mathrm{HCl + NaOH \xlongequal{} NaCl + H_2O}$
D(×)氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,除去原物质,不符合除杂原则。
10. 新考法 实验分析与图像相结合 分析兴趣小组同学用图1所示装置完成加热高锰酸钾并收集一瓶氧气的任务,集气瓶内液面的高度随加热时间的变化如图2所示,其中$P$点时将集气瓶从水槽中取出。下列说法正确的是(
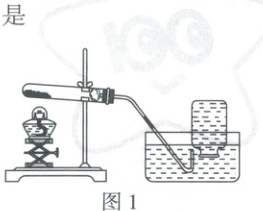
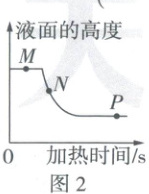
A.$M$点:导管口有气泡冒出,表示可以开始收集
B.$N$点:将试管内固体经溶解、过滤、蒸发,可得到二氧化锰
C.$P$点:试管中可能含有三种固体
D.$M \to N$固体减少的质量等于集气瓶内减少的水的质量
C
)

A.$M$点:导管口有气泡冒出,表示可以开始收集
B.$N$点:将试管内固体经溶解、过滤、蒸发,可得到二氧化锰
C.$P$点:试管中可能含有三种固体
D.$M \to N$固体减少的质量等于集气瓶内减少的水的质量
答案:
10 C 名师教审题
结合图像分析如下:
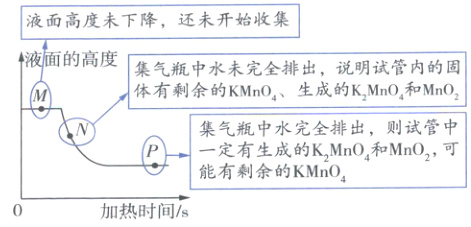
A(×)刚开始冒出的气泡可能是试管或导管中的空气,或空气和氧气的混合物,应等有连续均匀的气泡冒出时,再开始收集。
B(×)N点时,试管内的$\mathrm{KMnO_4}$和$\mathrm{K_2MnO_4}$易溶于水,$\mathrm{MnO_2}$不溶于水,溶解、过滤、蒸发得到$\mathrm{KMnO_4}$和$\mathrm{K_2MnO_4}$的混合物,要想得到$\mathrm{MnO_2}$,应对滤渣进行洗涤、干燥。
C(√)P点时,试管中一定有生成的$\mathrm{K_2MnO_4}$和$\mathrm{MnO_2}$,可能有剩余的$\mathrm{KMnO_4}$。
D(×)由M→N,集气瓶中排出水的质量大于生成氧气的质量(氧气的密度比水小得多),固体减少的质量即生成氧气的质量小于集气瓶内减少的水的质量。
名师碎碎念 解答此题时,应注意图2的纵轴代表的是集气瓶内液面的高度,而非以往的试管内固体的质量,则分析实验过程时应注意,当曲线不再下降时,不代表试管中的固体已经完全反应,有可能会有剩余。
10 C 名师教审题
结合图像分析如下:

A(×)刚开始冒出的气泡可能是试管或导管中的空气,或空气和氧气的混合物,应等有连续均匀的气泡冒出时,再开始收集。
B(×)N点时,试管内的$\mathrm{KMnO_4}$和$\mathrm{K_2MnO_4}$易溶于水,$\mathrm{MnO_2}$不溶于水,溶解、过滤、蒸发得到$\mathrm{KMnO_4}$和$\mathrm{K_2MnO_4}$的混合物,要想得到$\mathrm{MnO_2}$,应对滤渣进行洗涤、干燥。
C(√)P点时,试管中一定有生成的$\mathrm{K_2MnO_4}$和$\mathrm{MnO_2}$,可能有剩余的$\mathrm{KMnO_4}$。
D(×)由M→N,集气瓶中排出水的质量大于生成氧气的质量(氧气的密度比水小得多),固体减少的质量即生成氧气的质量小于集气瓶内减少的水的质量。
名师碎碎念 解答此题时,应注意图2的纵轴代表的是集气瓶内液面的高度,而非以往的试管内固体的质量,则分析实验过程时应注意,当曲线不再下降时,不代表试管中的固体已经完全反应,有可能会有剩余。
11. 新教材 跨学科实践 (4分)石家庄公交车使用的能源经历了如图所示的变迁,对环保和可持续发展产生了深远影响。
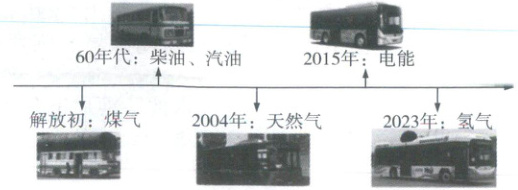
(1)60年代的燃油汽车使用柴油、汽油等作为燃料。柴油、汽油是
(2)为了满足使用电能、氢能等能源的汽车轻量化的需求,在车身结构中广泛使用到了铝合金,铝合金与铝相比其硬度更
(3)电动汽车普遍采用锂电池来提供动力,其中${LiCoO_{2}}$是常见的正极材料。${LiCoO_{2}}$中锂(${Li}$)的化合价为$+1$,则钴(${Co}$)的化合价为
(4)氢能源汽车以氢气为燃料,与化石燃料相比,氢能的优点是

(1)60年代的燃油汽车使用柴油、汽油等作为燃料。柴油、汽油是
石油
综合利用的产物。(2)为了满足使用电能、氢能等能源的汽车轻量化的需求,在车身结构中广泛使用到了铝合金,铝合金与铝相比其硬度更
大
(填“大”或“小”)。(3)电动汽车普遍采用锂电池来提供动力,其中${LiCoO_{2}}$是常见的正极材料。${LiCoO_{2}}$中锂(${Li}$)的化合价为$+1$,则钴(${Co}$)的化合价为
+3
。(4)氢能源汽车以氢气为燃料,与化石燃料相比,氢能的优点是
无污染(合理即可)
(写出一条即可)。
答案:
11
(1)石油
(2)大
(3)+3
(4)无污染(合理即可)
【解题思路】
(1)石油是一种复杂的混合物,通过分馏等综合利用方式,可以根据各成分沸点不同,从中分离出汽油、柴油等多种产品。
(2)合金的硬度比组成它的纯金属的硬度大。
(3)$\mathrm{LiCoO_2}$中锂(Li)的化合价为 +1,氧的化合价为 -2,设钴的化合价为x,根据化合物中各元素正、负化合价代数和为0,可得( +1)+x+( -2)×2 = 0,解得x = +3。
(1)石油
(2)大
(3)+3
(4)无污染(合理即可)
【解题思路】
(1)石油是一种复杂的混合物,通过分馏等综合利用方式,可以根据各成分沸点不同,从中分离出汽油、柴油等多种产品。
(2)合金的硬度比组成它的纯金属的硬度大。
(3)$\mathrm{LiCoO_2}$中锂(Li)的化合价为 +1,氧的化合价为 -2,设钴的化合价为x,根据化合物中各元素正、负化合价代数和为0,可得( +1)+x+( -2)×2 = 0,解得x = +3。
12. (3分)我国传统文化博大精深,蕴含了丰富的化学知识。
(1)《梦溪笔谈》中记载薯莨汁可用于染色,薯莨汁中含有丰富的单宁酸(${C_{76}H_{52}O_{46}}$),单宁酸属于
(2)松烟墨在我国书法和绘画中有着悠久的历史,“烟”是由松木的不完全燃烧而形成的,这里“烟”的主要成分是
(3)非遗民俗表演“打铁花”,是将铁水抛洒向空中,形成“火树银花落,万点星辰开”的绚丽场景。铁花在飞溅过程中形成黑色固体,其化学方程式为
(1)《梦溪笔谈》中记载薯莨汁可用于染色,薯莨汁中含有丰富的单宁酸(${C_{76}H_{52}O_{46}}$),单宁酸属于
有机
(填“有机”或“无机”)化合物。(2)松烟墨在我国书法和绘画中有着悠久的历史,“烟”是由松木的不完全燃烧而形成的,这里“烟”的主要成分是
碳
(填物质名称)。(3)非遗民俗表演“打铁花”,是将铁水抛洒向空中,形成“火树银花落,万点星辰开”的绚丽场景。铁花在飞溅过程中形成黑色固体,其化学方程式为
$\mathrm{3Fe + 2O_2 \xlongequal{点燃} Fe_3O_4}$
。
答案:
12
(1)有机
(2)碳
(3)$\mathrm{3Fe + 2O_2 \xlongequal{点燃} Fe_3O_4}$
(1)有机
(2)碳
(3)$\mathrm{3Fe + 2O_2 \xlongequal{点燃} Fe_3O_4}$
13. (5分)《天工开物·作咸》中记载“候潮一过,明日天晴,半日晒出盐霜,疾趋扫起煎炼”。“盐霜”的主要成分是氯化钠固体,如图1所示为氯化钠的溶解度曲线,回答下列问题:
(1)$20\ ^{\circ}C$时,饱和氯化钠溶液中溶质的质量分数是
(2)氯化钠以离子的形式分散在水中形成溶液,其溶液中的阳离子是
(3)“半日晒出盐霜”中,“晒”与实验室中
(4)在$40\ ^{\circ}C$时,恒温蒸发一定质量的氯化钠溶液模拟海水晒盐的过程,溶液中溶质的质量与蒸发水的质量关系如图2所示。该实验所用氯化钠溶液是
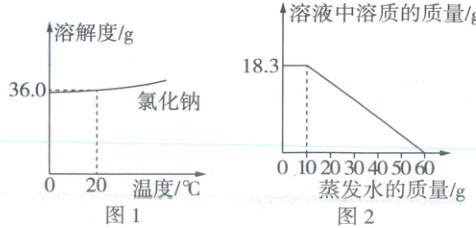
(1)$20\ ^{\circ}C$时,饱和氯化钠溶液中溶质的质量分数是
26.5%
(结果保留一位小数)。(2)氯化钠以离子的形式分散在水中形成溶液,其溶液中的阳离子是
$\mathrm{Na^+}$
(填离子符号)。(3)“半日晒出盐霜”中,“晒”与实验室中
蒸发
(填操作名称)的原理相同。(4)在$40\ ^{\circ}C$时,恒温蒸发一定质量的氯化钠溶液模拟海水晒盐的过程,溶液中溶质的质量与蒸发水的质量关系如图2所示。该实验所用氯化钠溶液是
不饱和
(填“饱和”或“不饱和”)溶液;$40\ ^{\circ}C$时,氯化钠的溶解度为36.6
$g$。
答案:
13
(1)26.5%
(2)$\mathrm{Na^+}$
(3)蒸发
(4)不饱和 36.6
【解题思路】
(1)20℃时,饱和NaCl溶液中溶质的质量分数是$\frac{36.0g}{36.0g + 100g}×100\% ≈ 26.5\%$。
(2)NaCl是由$\mathrm{Na^+}$和$\mathrm{Cl^-}$构成的,则其溶液中的阳离子是$\mathrm{Na^+}$。
(3)“半日晒出盐霜”中,“晒”时温度升高,水分子获得能量,运动加快,水分子间的间隔变大,逸散到空气中,与实验室中蒸发的原理相同。
(4)一开始蒸发水,溶液中溶质的质量不变,说明原来的NaCl溶液是不饱和溶液,由图示可知,蒸发50g水,析出18.3g的NaCl,即该温度下,50g水中最多溶解18.3gNaCl,则在该温度下,100g水中最多溶解36.6g,所以40℃时,氯化钠的溶解度为36.6g。
(1)26.5%
(2)$\mathrm{Na^+}$
(3)蒸发
(4)不饱和 36.6
【解题思路】
(1)20℃时,饱和NaCl溶液中溶质的质量分数是$\frac{36.0g}{36.0g + 100g}×100\% ≈ 26.5\%$。
(2)NaCl是由$\mathrm{Na^+}$和$\mathrm{Cl^-}$构成的,则其溶液中的阳离子是$\mathrm{Na^+}$。
(3)“半日晒出盐霜”中,“晒”时温度升高,水分子获得能量,运动加快,水分子间的间隔变大,逸散到空气中,与实验室中蒸发的原理相同。
(4)一开始蒸发水,溶液中溶质的质量不变,说明原来的NaCl溶液是不饱和溶液,由图示可知,蒸发50g水,析出18.3g的NaCl,即该温度下,50g水中最多溶解18.3gNaCl,则在该温度下,100g水中最多溶解36.6g,所以40℃时,氯化钠的溶解度为36.6g。
查看更多完整答案,请扫码查看


