2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第35页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
14. (5 分)传统乙醇制氢工艺化学反应原理为 C₂H₅OH + 3H₂O $\xlongequal[高温]{催化剂}$ 2CO₂ + 6H₂。2025 年 2 月《科学》杂志刊发了北京大学马丁团队研发的制氢技术成果,他们创造性使用铂 - 铱双金属催化剂,使乙醇与水在 260℃下反应,生成醋酸(CH₃COOH)和氢气。其微观示意图如图所示:
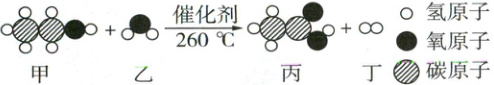
(1) 该变化前后发生改变的微观粒子是
(2) 氢气被人们称为最清洁的燃料,原因是
(3) 反应过程中乙、丁分子的个数比为
(4) 该反应使用铂 - 铱双金属催化剂,以下有关此催化剂的说法正确的是
A. 降低了反应所需温度
B. 使生成氢气的质量增加
C. 反应后质量会减少
(5) 对比两种工艺,马丁团队技术的核心优势是

(1) 该变化前后发生改变的微观粒子是
分子
_(填“分子”或“原子”)。(2) 氢气被人们称为最清洁的燃料,原因是
2H₂+O₂点燃2H₂O
_ (用化学方程式表示)。(3) 反应过程中乙、丁分子的个数比为
1:2
_ 。(4) 该反应使用铂 - 铱双金属催化剂,以下有关此催化剂的说法正确的是
A
_ (填字母)。A. 降低了反应所需温度
B. 使生成氢气的质量增加
C. 反应后质量会减少
(5) 对比两种工艺,马丁团队技术的核心优势是
没有生成二氧化碳(合理即可)
_ ,助力碳中和目标的实现。
答案:
14
(1)分子
(2)2H₂+O₂点燃2H₂O
(3)1:2
(4)A
(5)没有生成二氧化碳(合理即可)
【解题思路】
(1)化学反应的实质是分子破裂、原子重新组合。在这个反应中,反应前是乙醇分子和水分子,反应后是醋酸分子和氢气分子,分子发生了改变,而原子的种类和数目不变。
(3)由微观示意图可知,甲是C₂H₅OH,乙是H₂O,丙是CH₃COOH,丁是H₂,该反应的化学方程式为C₂H₅OH+H₂O铂-铱双金属催化剂260℃CH₃COOH+2H₂↑,所以乙(H₂O)、丁(H₂)分子的个数比为1:2。
(4)催化剂能改变化学反应速率,但不会影响生成物的质量,且其质量和化学性质在反应前后不发生改变(此为结论,要牢记)。
(5)传统工艺生成二氧化碳,会增加碳排放,而马丁团队技术的反应产物中没有二氧化碳,核心优势是没有生成二氧化碳,助力碳中和目标的实现。
(1)分子
(2)2H₂+O₂点燃2H₂O
(3)1:2
(4)A
(5)没有生成二氧化碳(合理即可)
【解题思路】
(1)化学反应的实质是分子破裂、原子重新组合。在这个反应中,反应前是乙醇分子和水分子,反应后是醋酸分子和氢气分子,分子发生了改变,而原子的种类和数目不变。
(3)由微观示意图可知,甲是C₂H₅OH,乙是H₂O,丙是CH₃COOH,丁是H₂,该反应的化学方程式为C₂H₅OH+H₂O铂-铱双金属催化剂260℃CH₃COOH+2H₂↑,所以乙(H₂O)、丁(H₂)分子的个数比为1:2。
(4)催化剂能改变化学反应速率,但不会影响生成物的质量,且其质量和化学性质在反应前后不发生改变(此为结论,要牢记)。
(5)传统工艺生成二氧化碳,会增加碳排放,而马丁团队技术的反应产物中没有二氧化碳,核心优势是没有生成二氧化碳,助力碳中和目标的实现。
15. (5 分)废旧手机回收处理作为“朝阳产业”拥有很大的发展潜力。小南设计了如图所示流程,从废旧手机的部件中回收银和铜。
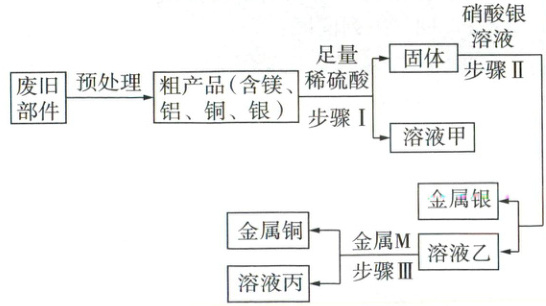
(1) 步骤Ⅰ ~ Ⅲ中涉及了共同的操作,实验室进行该操作时用到的玻璃仪器有烧杯、玻璃棒和
(2) 步骤Ⅰ中加入足量稀硫酸的目的是
(3) 溶液甲中一定含有的溶质为
(4) 步骤Ⅲ中,发生反应的化学方程式可能为
(5) 该工艺流程的价值在于

(1) 步骤Ⅰ ~ Ⅲ中涉及了共同的操作,实验室进行该操作时用到的玻璃仪器有烧杯、玻璃棒和
漏斗
_ 。(2) 步骤Ⅰ中加入足量稀硫酸的目的是
使粗产品中的镁、铝完全反应
_。(3) 溶液甲中一定含有的溶质为
MgSO₄、Al₂(SO₄)₃
_ (填化学式)。(4) 步骤Ⅲ中,发生反应的化学方程式可能为
Cu(NO₃)₂+Fe=Fe(NO₃)₂+Cu(答案不唯一,合理即可)
_ (写一个)。(5) 该工艺流程的价值在于
节约金属资源,减少环境污染(合理即可)
_ 。
答案:
15
(1)漏斗
(2)使粗产品中的镁、铝完全反应
(3)MgSO₄、Al₂(SO₄)₃
(4)Cu(NO₃)₂+Fe=Fe(NO₃)₂+Cu(答案不唯一,合理即可)
(5)节约金属资源,减少环境污染(合理即可)
◇快招解题法 试题秒解 考场速用
结合流程图分析如下:
发生反应:Mg+H₂SO₄=MgSO₄+H₂↑、2Al+3H₂SO₄=Al₂(SO₄)₃+3H₂↑、Cu、Ag在金属活动性顺序中位于氢后,不与稀硫酸反应

(1)由图可知,操作I~Ⅲ都是将固体和液体分离的操作,这种操作是过滤,过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)由图可知,粗产品中含有镁、铝等杂质,加入足量稀硫酸的目的是使粗产品中的镁、铝完全反应。
(3)若M是铁,发生的反应为Cu(NO₃)₂+Fe=Fe(NO₃)₂+Cu;若M是锌,发生的反应为Cu(NO₃)₂+Zn=Zn(NO₃)₂+Cu;若M是Al,发生的反应为2Al+3Cu(NO₃)₂=2Al(NO₃)₃+3Cu。
⇨更多讲解详见《解题有招》折页“快招7”
15
(1)漏斗
(2)使粗产品中的镁、铝完全反应
(3)MgSO₄、Al₂(SO₄)₃
(4)Cu(NO₃)₂+Fe=Fe(NO₃)₂+Cu(答案不唯一,合理即可)
(5)节约金属资源,减少环境污染(合理即可)
◇快招解题法 试题秒解 考场速用
结合流程图分析如下:
发生反应:Mg+H₂SO₄=MgSO₄+H₂↑、2Al+3H₂SO₄=Al₂(SO₄)₃+3H₂↑、Cu、Ag在金属活动性顺序中位于氢后,不与稀硫酸反应

(1)由图可知,操作I~Ⅲ都是将固体和液体分离的操作,这种操作是过滤,过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)由图可知,粗产品中含有镁、铝等杂质,加入足量稀硫酸的目的是使粗产品中的镁、铝完全反应。
(3)若M是铁,发生的反应为Cu(NO₃)₂+Fe=Fe(NO₃)₂+Cu;若M是锌,发生的反应为Cu(NO₃)₂+Zn=Zn(NO₃)₂+Cu;若M是Al,发生的反应为2Al+3Cu(NO₃)₂=2Al(NO₃)₃+3Cu。
⇨更多讲解详见《解题有招》折页“快招7”
16. (5 分)根据图 1、图 2 所示装置进行实验,回答下列问题。
(1) 图 1 是用钢丝棉验证铁生锈条件的装置。一段时间后,观察到 a 处锈迹斑斑,b 处无明显现象,c 处出现少量锈迹。还可观察到 U 形管左侧液面
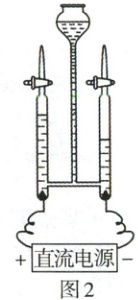
(2) 图 2 为电解水的实验装置。实验时向水中加入氢氧化钠,其目的是
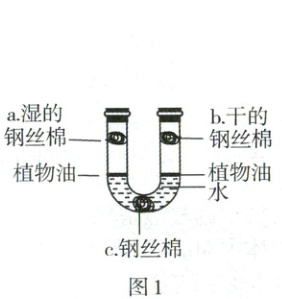
(1) 图 1 是用钢丝棉验证铁生锈条件的装置。一段时间后,观察到 a 处锈迹斑斑,b 处无明显现象,c 处出现少量锈迹。还可观察到 U 形管左侧液面
高于
_ (填“高于”或“低于”)右侧。为了避免在 c 处出现锈迹,改进的实验方案是改用经煮沸并迅速冷却的蒸馏水进行实验
_。(2) 图 2 为电解水的实验装置。实验时向水中加入氢氧化钠,其目的是
增强水的导电性
_。通过电解水和氢气燃烧实验都能得出水的组成。两种推理方法不同:一种方法是通过发生分解
_(填“化合”或“分解”)反应,由分析生成物的组成确定反应物的组成;另一种方法是通过发生化合
_ (填“化合”或“分解”)反应,由分析反应物的组成确定生成物的组成。

答案:
16
(1)高于 改用经煮沸并迅速冷却的蒸馏水进行实验
(2)增强水的导电性 分解 化合
【解题思路】
(1)a处铁与氧气和水接触,生锈,b处铁只与氧气接触,不生锈,a中铁生锈消耗了氧气,装置内气体减少,压强减小,可观察到U形管左侧液面高于右侧,水中含有溶解氧,故c处出现少量锈迹,为了避免在c处出现锈迹,改进的实验方案是改用经煮沸并迅速冷却的蒸馏水进行实验。
(2)电解水:2H₂O通电2H₂↑+O₂↑;一变多,分解反应;
氢气燃烧:2H₂+O₂点燃2H₂O,多变一,化合反应。
(1)高于 改用经煮沸并迅速冷却的蒸馏水进行实验
(2)增强水的导电性 分解 化合
【解题思路】
(1)a处铁与氧气和水接触,生锈,b处铁只与氧气接触,不生锈,a中铁生锈消耗了氧气,装置内气体减少,压强减小,可观察到U形管左侧液面高于右侧,水中含有溶解氧,故c处出现少量锈迹,为了避免在c处出现锈迹,改进的实验方案是改用经煮沸并迅速冷却的蒸馏水进行实验。
(2)电解水:2H₂O通电2H₂↑+O₂↑;一变多,分解反应;
氢气燃烧:2H₂+O₂点燃2H₂O,多变一,化合反应。
17. 新课标 项目式学习 (7 分)我市一些县区采用了“渔光互补”的发展模式,化学实践小组的同学在老师的指导下展开了项目式学习活动。
任务一:了解渔光互补模式
如图 1 所示在水上架设光伏板发电,下方水域进行水产养殖。
(1) 光伏发电过程是将光能转化为
任务二:检测鱼塘水质
同学们来到“××渔光互补示范园”,据养殖人员介绍,水产养殖过程中需保证合适的水温、溶氧量和酸碱度。
【实验 1】(2) 同学们用
(3) 小组同学认为水中溶有鱼呼吸产生的 CO₂,pH 应该减小,但从清晨到中午,鱼塘水的 pH 却逐渐增大,原因可能与水中藻类的
任务三:如何养护鱼塘水质
老师告诉大家:①鱼塘底部塘泥中的有机物分解易使水质酸性增强;②该鱼塘养殖鱼虾,需定期为鱼虾补充钙质。
【讨论交流】(4) 有同学提出向鱼塘中直接投放生石灰,既可以调节鱼塘水的 pH 又可以为鱼虾补充钙质,大家一致反对,请说明反对的理由:
养殖人员介绍:定量向鱼塘投放过氧化钙(如图 2 所示),水中会持续缓慢产生气泡。
探究Ⅰ:产生的气体是否为氧气?
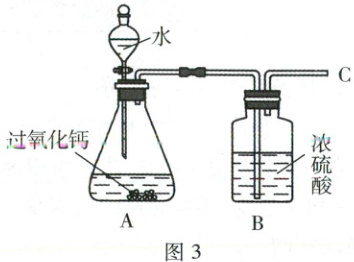
【实验 2】取适量过氧化钙样品和水,按图 3 所示进行实验。
(5) A 中产生气泡缓慢,有同学提议在 C 处放一燃着的小木条,观察到
探究Ⅱ:反应后溶液中溶质是什么?
【作出猜想】小组同学经过分析后认为,反应后溶液中溶质是氢氧化钙。
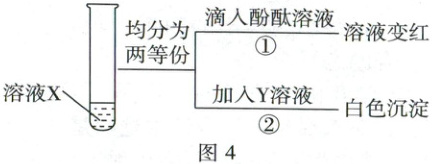
【实验 3】取装置 A 中反应后溶液 X,按图 4 所示方案进行实验,验证了他们的猜想是正确的。
(6) Y 为常见试剂,步骤②中反应的化学方程式为
【拓展交流】
(7) 水上光伏发电设施长期处于潮湿且可能带有盐分(海水环境)的特殊环境中,金属部件、电气设备易受影响。请结合已有知识经验写出一条该设施需要定期检修、维护的项目:


任务一:了解渔光互补模式
如图 1 所示在水上架设光伏板发电,下方水域进行水产养殖。
(1) 光伏发电过程是将光能转化为
电
_ 能。任务二:检测鱼塘水质
同学们来到“××渔光互补示范园”,据养殖人员介绍,水产养殖过程中需保证合适的水温、溶氧量和酸碱度。
【实验 1】(2) 同学们用
pH试纸(或pH计)
_ 测定了不同时段鱼塘水的 pH。(3) 小组同学认为水中溶有鱼呼吸产生的 CO₂,pH 应该减小,但从清晨到中午,鱼塘水的 pH 却逐渐增大,原因可能与水中藻类的
光合
_ 作用有关。任务三:如何养护鱼塘水质
老师告诉大家:①鱼塘底部塘泥中的有机物分解易使水质酸性增强;②该鱼塘养殖鱼虾,需定期为鱼虾补充钙质。
【讨论交流】(4) 有同学提出向鱼塘中直接投放生石灰,既可以调节鱼塘水的 pH 又可以为鱼虾补充钙质,大家一致反对,请说明反对的理由:
生石灰与水反应放出大量热,会伤害鱼虾
_ 。养殖人员介绍:定量向鱼塘投放过氧化钙(如图 2 所示),水中会持续缓慢产生气泡。
探究Ⅰ:产生的气体是否为氧气?
【实验 2】取适量过氧化钙样品和水,按图 3 所示进行实验。
(5) A 中产生气泡缓慢,有同学提议在 C 处放一燃着的小木条,观察到
木条燃烧更旺
_,说明生成的气体是氧气。探究Ⅱ:反应后溶液中溶质是什么?
【作出猜想】小组同学经过分析后认为,反应后溶液中溶质是氢氧化钙。
【实验 3】取装置 A 中反应后溶液 X,按图 4 所示方案进行实验,验证了他们的猜想是正确的。
(6) Y 为常见试剂,步骤②中反应的化学方程式为
Ca(OH)₂+Na₂CO₃=CaCO₃↓+2NaOH[或Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH]
_ 。【拓展交流】
(7) 水上光伏发电设施长期处于潮湿且可能带有盐分(海水环境)的特殊环境中,金属部件、电气设备易受影响。请结合已有知识经验写出一条该设施需要定期检修、维护的项目:
检查金属部分是否锈蚀(或涂防锈漆等进行防锈处理或检查电气设备是否漏电,更换老化绝缘材料等,合理即可)
_。



答案:
17
(1)电
(2)pH试纸(或pH计)
(3)光合
(4)生石灰与水反应放出大量热,会伤害鱼虾
(5)木条燃烧更旺
(6)Ca(OH)₂+Na₂CO₃=CaCO₃↓+2NaOH[或Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH]
(7)检查金属部分是否锈蚀(或涂防锈漆等进行防锈处理或检查电气设备是否漏电,更换老化绝缘材料等,合理即可)
【解题思路】
(3)从清晨到中午,随着光照增强,水中藻类进行光合作用,消耗CO₂,使溶液酸性减弱,pH增大。
(4)生石灰是氧化钙的俗称,氧化钙与水反应生成氢氧化钙,该反应发生时放出大量的热,会对鱼虾造成伤害。
(5)氧气具有助燃性,能使燃着的小木条燃烧更旺盛。则在C处放一燃着的小木条,若观察到木条燃烧更旺,则说明生成的气体是氧气。
(6)由【作出猜想】中“反应后溶液中溶质是氢氧化钙”可知加入的Y是一种碳酸盐溶液,如碳酸钠、碳酸钾等。
(1)电
(2)pH试纸(或pH计)
(3)光合
(4)生石灰与水反应放出大量热,会伤害鱼虾
(5)木条燃烧更旺
(6)Ca(OH)₂+Na₂CO₃=CaCO₃↓+2NaOH[或Ca(OH)₂+K₂CO₃=CaCO₃↓+2KOH]
(7)检查金属部分是否锈蚀(或涂防锈漆等进行防锈处理或检查电气设备是否漏电,更换老化绝缘材料等,合理即可)
【解题思路】
(3)从清晨到中午,随着光照增强,水中藻类进行光合作用,消耗CO₂,使溶液酸性减弱,pH增大。
(4)生石灰是氧化钙的俗称,氧化钙与水反应生成氢氧化钙,该反应发生时放出大量的热,会对鱼虾造成伤害。
(5)氧气具有助燃性,能使燃着的小木条燃烧更旺盛。则在C处放一燃着的小木条,若观察到木条燃烧更旺,则说明生成的气体是氧气。
(6)由【作出猜想】中“反应后溶液中溶质是氢氧化钙”可知加入的Y是一种碳酸盐溶液,如碳酸钠、碳酸钾等。
查看更多完整答案,请扫码查看


