2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第19页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
14. (6分)在北京大学马丁教授团队的“零碳排放制氢技术”中,涉及到乙醇和水分子的重整反应,其微观示意图如图所示:

氢原子 氧原子 碳原子
(1)丙分子中 和 两种原子的个数比为
(2)该反应的化学方程式为
(3)该反应创新性地使用了铂 - 铱双金属催化剂,降低了反应条件的难度。以下有关此催化剂的说法正确的是
A. 加快了反应速率
B. 降低了反应所需温度
C. 反应后质量会减少
D. 使生成氢气的质量增加
(4)“零碳排放制氢技术”助力碳中和目标的实现。该技术可减少${CO_{2}}$的排放,从而能够缓解的环境问题是

氢原子 氧原子 碳原子
(1)丙分子中 和 两种原子的个数比为
1:2
(填最简整数比)。(2)该反应的化学方程式为
$\mathrm{C_2H_5OH + H_2O \xlongequal{催化剂} CH_3COOH + 2H_2↑}$
;参加反应的甲和乙的质量比为23:9
(填最简整数比)。(3)该反应创新性地使用了铂 - 铱双金属催化剂,降低了反应条件的难度。以下有关此催化剂的说法正确的是
AB
。A. 加快了反应速率
B. 降低了反应所需温度
C. 反应后质量会减少
D. 使生成氢气的质量增加
(4)“零碳排放制氢技术”助力碳中和目标的实现。该技术可减少${CO_{2}}$的排放,从而能够缓解的环境问题是
温室效应
,请写出一种生活中缓解该环境问题的做法:少开私家车,尽量乘坐公交车出行(合理即可)
。
答案:
14
(1)1:2
(2)$\mathrm{C_2H_5OH + H_2O \xlongequal{催化剂} CH_3COOH + 2H_2↑}$ 23:9
(3)AB
(4)温室效应 少开私家车,尽量乘坐公交车出行(合理即可)
【解题思路】
(1)由分子的模型图可知,丙分子中 和○两种原子的个数比为 2:4 = 1:2。
(2)由反应的微观示意图可知,该反应的化学方程式为$\mathrm{C_2H_5OH + H_2O \xlongequal{催化剂} CH_3COOH + 2H_2↑}$,则参加反应的甲和乙的质量比为 46:18 = 23:9。
(3)催化剂只能改变反应速率,不能改变生成物的质量,其质量和化学性质在反应前后均不发生改变,物理性质可能发生改变。
(4)生活中缓解该环境问题的做法有很多,如随手关灯、植树造林、少开私家车,尽量乘坐公交车出行等。
(1)1:2
(2)$\mathrm{C_2H_5OH + H_2O \xlongequal{催化剂} CH_3COOH + 2H_2↑}$ 23:9
(3)AB
(4)温室效应 少开私家车,尽量乘坐公交车出行(合理即可)
【解题思路】
(1)由分子的模型图可知,丙分子中 和○两种原子的个数比为 2:4 = 1:2。
(2)由反应的微观示意图可知,该反应的化学方程式为$\mathrm{C_2H_5OH + H_2O \xlongequal{催化剂} CH_3COOH + 2H_2↑}$,则参加反应的甲和乙的质量比为 46:18 = 23:9。
(3)催化剂只能改变反应速率,不能改变生成物的质量,其质量和化学性质在反应前后均不发生改变,物理性质可能发生改变。
(4)生活中缓解该环境问题的做法有很多,如随手关灯、植树造林、少开私家车,尽量乘坐公交车出行等。
15. (5分)铁红(${Fe_{2}O_{3}}$)可用于制备红色颜料。某兴趣小组进行了从“暖宝宝”的废渣中提取${Fe_{2}O_{3}}$的实验,具体操作过程如图所示。已知:暖宝宝的废渣中含有${Fe}$、${Fe_{2}O_{3}}$、${NaCl}$、活性炭和蛭石等,蛭石不溶于水也不参与流程中的任一反应。

请回答下列问题:
(1)步骤①中分离出铁粉的方法为
(2)步骤②中加入过量稀${H_{2}SO_{4}}$的目的为
(3)步骤③中生成${Fe(OH)_{3}}$的化学方程式为

请回答下列问题:
(1)步骤①中分离出铁粉的方法为
用磁铁吸引
。(2)步骤②中加入过量稀${H_{2}SO_{4}}$的目的为
使氧化铁充分反应
,滤液$a$中溶质为$\mathrm{Fe_2(SO_4)_3、NaCl、H_2SO_4}$(或硫酸铁、稀硫酸、氯化钠)
。(3)步骤③中生成${Fe(OH)_{3}}$的化学方程式为
$\mathrm{Fe_2(SO_4)_3 + 6NaOH \xlongequal{} 2Fe(OH)_3↓ + 3Na_2SO_4}$
。制备${Fe_{2}O_{3}}$时发生的反应为${2Fe(OH)_{3} \xlongequal{\Delta} Fe_{2}O_{3} + 3X}$,物质$X$的化学式为$\mathrm{H_2O}$
。
答案:
15
(1)用磁铁吸引
(2)使氧化铁充分反应 $\mathrm{Fe_2(SO_4)_3、NaCl、H_2SO_4}$(或硫酸铁、稀硫酸、氯化钠)
(3)$\mathrm{Fe_2(SO_4)_3 + 6NaOH \xlongequal{} 2Fe(OH)_3↓ + 3Na_2SO_4}$ $\mathrm{H_2O}$
【解题思路】结合流程图分析如下:
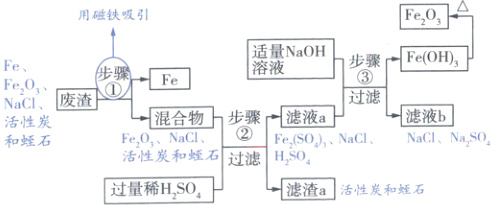
(1)因为铁是磁性材料,所以步骤①中可用磁铁吸引分离出铁。
(2)步骤②中加入过量稀硫酸,是为了使氧化铁和稀硫酸充分反应。氧化铁和稀硫酸反应生成硫酸铁和水。由于稀硫酸过量,所以滤液a中溶质为硫酸铁和稀硫酸。
(3)步骤③中加入适量NaOH溶液,NaOH会与滤液a中的$\mathrm{Fe_2(SO_4)_3}$反应生成$\mathrm{Fe(OH)_3}$沉淀和$\mathrm{Na_2SO_4}$,化学方程式为$\mathrm{Fe_2(SO_4)_3 + 6NaOH \xlongequal{} 2Fe(OH)_3↓ + 3Na_2SO_4}$,根据反应前后原子的种类和数目不变,可得X的化学式为$\mathrm{H_2O}$。
15
(1)用磁铁吸引
(2)使氧化铁充分反应 $\mathrm{Fe_2(SO_4)_3、NaCl、H_2SO_4}$(或硫酸铁、稀硫酸、氯化钠)
(3)$\mathrm{Fe_2(SO_4)_3 + 6NaOH \xlongequal{} 2Fe(OH)_3↓ + 3Na_2SO_4}$ $\mathrm{H_2O}$
【解题思路】结合流程图分析如下:

(1)因为铁是磁性材料,所以步骤①中可用磁铁吸引分离出铁。
(2)步骤②中加入过量稀硫酸,是为了使氧化铁和稀硫酸充分反应。氧化铁和稀硫酸反应生成硫酸铁和水。由于稀硫酸过量,所以滤液a中溶质为硫酸铁和稀硫酸。
(3)步骤③中加入适量NaOH溶液,NaOH会与滤液a中的$\mathrm{Fe_2(SO_4)_3}$反应生成$\mathrm{Fe(OH)_3}$沉淀和$\mathrm{Na_2SO_4}$,化学方程式为$\mathrm{Fe_2(SO_4)_3 + 6NaOH \xlongequal{} 2Fe(OH)_3↓ + 3Na_2SO_4}$,根据反应前后原子的种类和数目不变,可得X的化学式为$\mathrm{H_2O}$。
16. 新考法 教材实验创新 (5分)根据如图所示的实验回答问题。
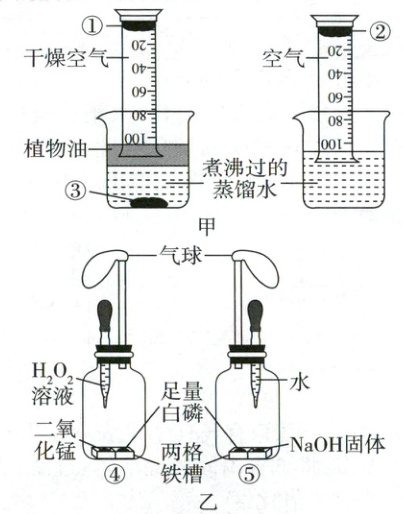
(1)甲是探究铁生锈条件的实验。图中①、②、③处均为光亮的铁丝绒。对比
(2)乙是探究热量变化的实验。将两装置中胶头滴管内的液体滴入铁槽中后,④、⑤中的白磷都发生燃烧,说明④中的反应

(1)甲是探究铁生锈条件的实验。图中①、②、③处均为光亮的铁丝绒。对比
②③
(填序号)的现象,可得铁生锈的条件之一为与氧气接触。植物油的作用为隔绝氧气,防止空气中的氧气进入水中干扰实验
。(2)乙是探究热量变化的实验。将两装置中胶头滴管内的液体滴入铁槽中后,④、⑤中的白磷都发生燃烧,说明④中的反应
放热
(填“吸收”或“放出”)热量;④中白磷燃烧更剧烈,说明燃烧的剧烈程度与氧气的浓度
有关。对比⑤装置滴入液体前后的现象,可得出可燃物燃烧的条件之一为温度达到其着火点
。
答案:
16
(1)②③ 隔绝氧气,防止空气中的氧气进入水中干扰实验
(2)放热 氧气的浓度 温度达到其着火点
【解题思路】
(1)①中的铁丝绒只与氧气接触,不生锈,③中铁丝绒只与水接触,不生锈,②中铁丝绒与氧气和水同时接触,生锈,对比②③中的现象,说明铁生锈的条件之一是与氧气接触。
(2)④中是过氧化氢在二氧化锰的催化作用下分解,⑤中是氢氧化钠固体溶于水,④、⑤中的白磷都发生燃烧,说明④中的反应放热,使温度达到了白磷的着火点。⑤中滴入水后,NaOH固体溶于水放热,白磷燃烧,改变的是⑤中的温度,则说明可燃物燃烧需要温度达到其着火点。
(1)②③ 隔绝氧气,防止空气中的氧气进入水中干扰实验
(2)放热 氧气的浓度 温度达到其着火点
【解题思路】
(1)①中的铁丝绒只与氧气接触,不生锈,③中铁丝绒只与水接触,不生锈,②中铁丝绒与氧气和水同时接触,生锈,对比②③中的现象,说明铁生锈的条件之一是与氧气接触。
(2)④中是过氧化氢在二氧化锰的催化作用下分解,⑤中是氢氧化钠固体溶于水,④、⑤中的白磷都发生燃烧,说明④中的反应放热,使温度达到了白磷的着火点。⑤中滴入水后,NaOH固体溶于水放热,白磷燃烧,改变的是⑤中的温度,则说明可燃物燃烧需要温度达到其着火点。
查看更多完整答案,请扫码查看


