2026年金考卷中考45套汇编化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年金考卷中考45套汇编化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第31页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
14. 新情境 科技成果 (6 分)我国自主研发了全球首艘氨燃料动力集装箱船,将开启全球航运零排放的氨燃料时代。氨气(NH₃)在氧气中燃烧的微观示意图如图所示。
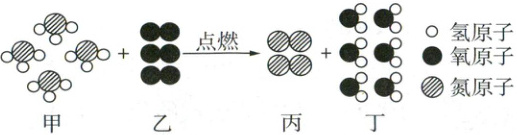
请回答下列问题:
(1)保持丁的化学性质的微观粒子是
(2)该反应前后没有发生改变的是
a. 原子种类
b. 分子数目
c. 原子数目
(3)请写出上述反应的化学方程式:
(4)若消耗了 17g 甲和 24g 乙,则生成了 14g 丙和
(5)氨燃料被认为是清洁燃料的原因是

请回答下列问题:
(1)保持丁的化学性质的微观粒子是
水分子
(填微观粒子名称)。(2)该反应前后没有发生改变的是
ac
(填字母)。a. 原子种类
b. 分子数目
c. 原子数目
(3)请写出上述反应的化学方程式:
$4NH₃+3O₂\overset{点燃}{=}2N₂+6H₂O$
,该反应属于置换
反应(填基本反应类型)。(4)若消耗了 17g 甲和 24g 乙,则生成了 14g 丙和
27
g 丁。(5)氨燃料被认为是清洁燃料的原因是
氨气燃烧生成氮气和水,不污染空气(合理即可)
。
答案:
14
(1)水分子
(2)ac
(3)$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$ 置换
(4)27
(5)氨气燃烧生成氮气和水,不污染空气(合理即可)
[解题思路]依据微观反应示意图写出反应的化学方程式:$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$。
(1)丁为水,水是由水分子构成的,则保持丁的化学性质的微观粒子是水分子(由分子构成的物质,分子是保持其化学性质的最小粒子)。
(2)化学反应前后原子种类和数目一定不变,分子数目可能改变,依据化学方程式可知,4个氨分子和3个氧分子在点燃条件下反应生成2个氮分子和6个水分子,反应前后分子数目改变。
(3)根据化学方程式$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,符合置换反应“单换单”的特征,属于置换反应。
(4)根据质量守恒定律,参加反应的各物质的质量和等于生成的各物质质量和,若消耗了17g甲和24g乙,生成了14g丙,则生成丁的质量为$17g + 24g - 14g = 27g$。
(1)水分子
(2)ac
(3)$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$ 置换
(4)27
(5)氨气燃烧生成氮气和水,不污染空气(合理即可)
[解题思路]依据微观反应示意图写出反应的化学方程式:$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$。
(1)丁为水,水是由水分子构成的,则保持丁的化学性质的微观粒子是水分子(由分子构成的物质,分子是保持其化学性质的最小粒子)。
(2)化学反应前后原子种类和数目一定不变,分子数目可能改变,依据化学方程式可知,4个氨分子和3个氧分子在点燃条件下反应生成2个氮分子和6个水分子,反应前后分子数目改变。
(3)根据化学方程式$4NH_{3}+3O_{2}\overset{点燃}{=}2N_{2}+6H_{2}O$,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物,符合置换反应“单换单”的特征,属于置换反应。
(4)根据质量守恒定律,参加反应的各物质的质量和等于生成的各物质质量和,若消耗了17g甲和24g乙,生成了14g丙,则生成丁的质量为$17g + 24g - 14g = 27g$。
15. (5 分)为减缓全球变暖速度,我国承诺在 2060 年实现“碳中和”,其中碳捕集是实现“碳中和”的措施之一,新兴碳捕集技术的工艺流程如图所示。
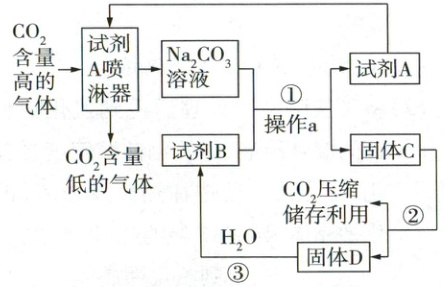
请回答下列问题:
(1)“碳中和”的碳是指
(2)操作 a 中会用到玻璃棒,其作用是
(3)试剂 A 在捕集 CO₂ 过程中,采用喷淋的方式,其目的是
(4)反应③中的能量变化为

请回答下列问题:
(1)“碳中和”的碳是指
二氧化碳(或CO₂)
。(2)操作 a 中会用到玻璃棒,其作用是
引流
。(3)试剂 A 在捕集 CO₂ 过程中,采用喷淋的方式,其目的是
增大反应物间的接触面积
。(4)反应③中的能量变化为
放热
(填“吸热”或“放热”)。反应①的化学方程式为Ca(OH)₂+Na₂CO₃=CaCO₃↓+2NaOH
。
答案:
15
(1)二氧化碳(或$CO_{2}$)
(2)引流
(3)增大反应物间的接触面积
(4)放热 $Ca(OH)_{2}+Na_{2}CO_{3}=CaCO_{3}↓+2NaOH$
[解题思路]结合流程图分析如下:

15
(1)二氧化碳(或$CO_{2}$)
(2)引流
(3)增大反应物间的接触面积
(4)放热 $Ca(OH)_{2}+Na_{2}CO_{3}=CaCO_{3}↓+2NaOH$
[解题思路]结合流程图分析如下:

16. (5 分)根据如图所示装置进行实验,回答下列问题。
(1)图 1 为小组同学设计的探究可燃物燃烧条件的装置(已知:白磷的着火点为 40℃)。图中 X 是
(2)图 2 为小组同学探究铁、铜、银的活动性顺序的装置。甲同学提出通过图中的实验不能判断三种金属的活动性顺序,理由是

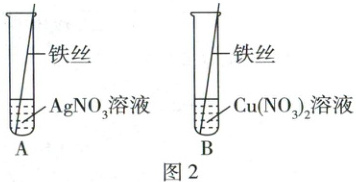
(1)图 1 为小组同学设计的探究可燃物燃烧条件的装置(已知:白磷的着火点为 40℃)。图中 X 是
冷水(或温度低于40℃的水)
,观察到 Y 形管左管中白磷燃烧,烧杯中白磷不燃烧的现象,说明可燃物燃烧的条件之一是与氧气(或空气)接触
。实验后气球比实验前变得更瘪,原因是白磷燃烧,消耗氧气,装置内气体压强变小(合理即可)
。(2)图 2 为小组同学探究铁、铜、银的活动性顺序的装置。甲同学提出通过图中的实验不能判断三种金属的活动性顺序,理由是
没有比较铜和银的活动性顺序
;要想达到实验目的,需要补充的实验操作是将洁净的铜丝放入硝酸银溶液中(合理即可)
。

答案:
16
(1)冷水(或温度低于40℃的水) 与氧气(或空气)接触 白磷燃烧,消耗氧气,装置内气体压强变小(合理即可)
(2)没有比较铜和银的活动性顺序 将洁净的铜丝放入硝酸银溶液中(合理即可)
[解题思路]
(1)可燃物燃烧需满足两个条件:温度达到可燃物的着火点、与氧气(或空气)接触。
温度达到可燃物的着火点 与氧气(或空气)接触
Y形管左侧白磷 √ √
Y形管右侧白磷 × √
烧杯中白磷 √ ×
表格中“√”代表满足条件,“×”代表不满足条件。
由Y形管左侧白磷和烧杯中白磷的现象对比可得出,可燃物燃烧的条件之一是与氧气(或空气)接触;若探究可燃物燃烧的另一条件,结合控制变量法,应对比Y形管左右两侧白磷的现象,左侧温度达到白磷的着火点,应设置右侧温度不达到白磷的着火点。
(2)试管A:铁丝表面有银白色物质析出,溶液由无色变为浅绿色,说明金属活动性:$Fe>Ag$;试管B:铁丝表面有红色物质析出,溶液由蓝色变为浅绿色,说明金属活动性:$Fe>Cu$;不能比较Ag和Cu的活动性强弱。为比较Ag和Cu的活动性强弱,可将银丝插入铜的盐溶液中或将铜丝插入硝酸银溶液中,观察现象。
名师讲方法 验证金属活动性顺序的方法 思维导引 验证两种金属活动性顺序 两种金属均在氢前或氢后 方法:金属与金属盐溶液反应 一种金属在氢前,另一种金属在氢后 方法一:金属与稀酸反应 方法二:金属与金属盐溶液反应 验证三种金属的活动性顺序 方法一:“两盐夹一金”(金属活动性最强和最弱的金属的盐溶液分别与金属活动性居中的金属的单质反应) 方法二:“两金夹一盐”(金属活动性最强和最弱的两种金属的单质分别与金属活动性居中的金属的盐溶液反应)

16
(1)冷水(或温度低于40℃的水) 与氧气(或空气)接触 白磷燃烧,消耗氧气,装置内气体压强变小(合理即可)
(2)没有比较铜和银的活动性顺序 将洁净的铜丝放入硝酸银溶液中(合理即可)
[解题思路]
(1)可燃物燃烧需满足两个条件:温度达到可燃物的着火点、与氧气(或空气)接触。
温度达到可燃物的着火点 与氧气(或空气)接触
Y形管左侧白磷 √ √
Y形管右侧白磷 × √
烧杯中白磷 √ ×
表格中“√”代表满足条件,“×”代表不满足条件。
由Y形管左侧白磷和烧杯中白磷的现象对比可得出,可燃物燃烧的条件之一是与氧气(或空气)接触;若探究可燃物燃烧的另一条件,结合控制变量法,应对比Y形管左右两侧白磷的现象,左侧温度达到白磷的着火点,应设置右侧温度不达到白磷的着火点。
(2)试管A:铁丝表面有银白色物质析出,溶液由无色变为浅绿色,说明金属活动性:$Fe>Ag$;试管B:铁丝表面有红色物质析出,溶液由蓝色变为浅绿色,说明金属活动性:$Fe>Cu$;不能比较Ag和Cu的活动性强弱。为比较Ag和Cu的活动性强弱,可将银丝插入铜的盐溶液中或将铜丝插入硝酸银溶液中,观察现象。
名师讲方法 验证金属活动性顺序的方法 思维导引 验证两种金属活动性顺序 两种金属均在氢前或氢后 方法:金属与金属盐溶液反应 一种金属在氢前,另一种金属在氢后 方法一:金属与稀酸反应 方法二:金属与金属盐溶液反应 验证三种金属的活动性顺序 方法一:“两盐夹一金”(金属活动性最强和最弱的金属的盐溶液分别与金属活动性居中的金属的单质反应) 方法二:“两金夹一盐”(金属活动性最强和最弱的两种金属的单质分别与金属活动性居中的金属的盐溶液反应)

17. (7 分)生活中洁厕液用于清洗厕所中的水垢、尿垢(含有碳酸钙等物质)。小丰同学在用洁厕液清洗马桶时,发现有气泡产生。这一现象引起他浓厚的探究兴趣,洁厕液的主要成分是什么?产生的气体又是什么?
探究Ⅰ 洁厕液成分的探究
【作出猜想】
通过实验室制取二氧化碳的反应原理,同学们猜想洁厕液的主要成分是酸。
【实验 1】
第一小组同学利用 pH 试纸测定洁厕液的 pH,结果 pH
【实验 2】
第二小组同学向盛有生锈铁钉的试管中加入洁厕液,一段时间后观察到铁锈逐渐消失,从而得出了洁厕液中含有酸的结论,他们作出判断的依据是
【分析讨论】
(1)小唐同学提出,向氢氧化钠溶液中直接加入洁厕液,也能证明洁厕液中含有酸的结论。但遭到了同学们的一致反对,同学们反对的原因是
(2)小明同学认为还可以用铁粉或石灰石,通过产生气泡的现象,证明洁厕液中含有酸的结论。老师对同学们勇于探索的态度给予肯定和表扬,并提示使用洁厕液清洁马桶时产生的气体只有一种。
探究Ⅱ 产生气体的探究
【提出问题】
清洗马桶时,产生的气体是什么呢?
【作出猜想】
小组同学结合水垢、尿垢和洁厕液成分,作出如下猜想:
猜想一:氢气; 猜想二:
【设计方案】
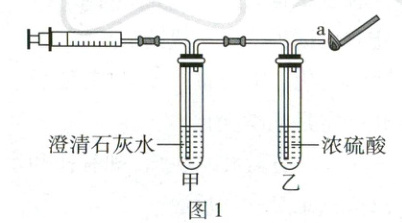
将收集到的气体通入如图 1 所示装置,观察到试管甲中
【学以致用】
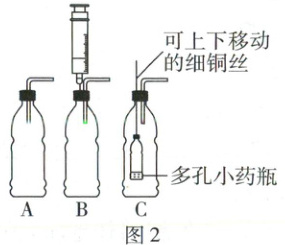
小丰同学发现,洁厕液也能与厨房中的纯碱粉末发生反应,而且反应非常剧烈。为了能够控制反应速率,他应该选择图 2 中的
【反思拓展】
(1)对物质进行检验需要利用物质的性质,并依据明显现象作出判断。
(2)使用洁厕液时应注意
探究Ⅰ 洁厕液成分的探究
【作出猜想】
通过实验室制取二氧化碳的反应原理,同学们猜想洁厕液的主要成分是酸。
【实验 1】
第一小组同学利用 pH 试纸测定洁厕液的 pH,结果 pH
<
7(填“>”“<”或“=”),初步判断洁厕液呈酸性。【实验 2】
第二小组同学向盛有生锈铁钉的试管中加入洁厕液,一段时间后观察到铁锈逐渐消失,从而得出了洁厕液中含有酸的结论,他们作出判断的依据是
Fe₂O₃+6HCl=2FeCl₃+3H₂O[或Fe₂O₃+3H₂SO₄=Fe₂(SO₄)₃+3H₂O]
(用化学方程式表示,写一个即可)。【分析讨论】
(1)小唐同学提出,向氢氧化钠溶液中直接加入洁厕液,也能证明洁厕液中含有酸的结论。但遭到了同学们的一致反对,同学们反对的原因是
氢氧化钠与稀酸反应没有明显现象(合理即可)
。(2)小明同学认为还可以用铁粉或石灰石,通过产生气泡的现象,证明洁厕液中含有酸的结论。老师对同学们勇于探索的态度给予肯定和表扬,并提示使用洁厕液清洁马桶时产生的气体只有一种。
探究Ⅱ 产生气体的探究
【提出问题】
清洗马桶时,产生的气体是什么呢?
【作出猜想】
小组同学结合水垢、尿垢和洁厕液成分,作出如下猜想:
猜想一:氢气; 猜想二:
二氧化碳(或CO₂)
。【设计方案】
将收集到的气体通入如图 1 所示装置,观察到试管甲中
澄清石灰水变浑浊
(填写实验
现象),将燃着的木条放在 a 管口处,a 管口无淡蓝色火焰产生,证明猜想二正确。【学以致用】
小丰同学发现,洁厕液也能与厨房中的纯碱粉末发生反应,而且反应非常剧烈。为了能够控制反应速率,他应该选择图 2 中的
B
(填字母)装置进行实验。【反思拓展】
(1)对物质进行检验需要利用物质的性质,并依据明显现象作出判断。
(2)使用洁厕液时应注意
不能接触金属制品或大理石(或使用时要戴口罩和手套或使用时要注意开窗通风,合理即可)
(写一条即可)。

答案:
17[实验1]< [实验2]$Fe_{2}O_{3}+6HCl=2FeCl_{3}+3H_{2}O$[或$Fe_{2}O_{3}+3H_{2}SO_{4}=Fe_{2}(SO_{4})_{3}+3H_{2}O$]
[分析讨论]氢氧化钠与稀酸反应没有明显现象(合理即可)
[作出猜想]二氧化碳(或$CO_{2}$)
[设计方案]澄清石灰水变浑浊
[学以致用]B
[反思拓展]不能接触金属制品或大理石(或使用时要戴口罩和手套或使用时要注意开窗通风,合理即可)
[解题思路][实验1]洁厕液呈酸性,则其$pH<7$(酸性溶液的$pH<7$,中性溶液的$pH = 7$,碱性溶液的$pH>7$)。
[实验2]铁锈的主要成分是$Fe_{2}O_{3}$,$Fe_{2}O_{3}$能与酸反应。
[作出猜想]水垢、尿垢含有碳酸钙等物质,碳酸钙和酸反应可生成$CO_{2}$,则猜想二为$CO_{2}$。
[设计方案]根据实验结论“证明猜想二正确”,可知产生的气体为$CO_{2}$,$CO_{2}$能使澄清石灰水变浑浊;将燃着的木条放在a管口处,a管口处无淡蓝色火焰产生(该气体不是氢气,因为氢气具有可燃性,燃烧产生淡蓝色火焰)。
[学以致用]B装置可通过注射器控制液体的滴加速率,从而控制反应速率。
[分析讨论]氢氧化钠与稀酸反应没有明显现象(合理即可)
[作出猜想]二氧化碳(或$CO_{2}$)
[设计方案]澄清石灰水变浑浊
[学以致用]B
[反思拓展]不能接触金属制品或大理石(或使用时要戴口罩和手套或使用时要注意开窗通风,合理即可)
[解题思路][实验1]洁厕液呈酸性,则其$pH<7$(酸性溶液的$pH<7$,中性溶液的$pH = 7$,碱性溶液的$pH>7$)。
[实验2]铁锈的主要成分是$Fe_{2}O_{3}$,$Fe_{2}O_{3}$能与酸反应。
[作出猜想]水垢、尿垢含有碳酸钙等物质,碳酸钙和酸反应可生成$CO_{2}$,则猜想二为$CO_{2}$。
[设计方案]根据实验结论“证明猜想二正确”,可知产生的气体为$CO_{2}$,$CO_{2}$能使澄清石灰水变浑浊;将燃着的木条放在a管口处,a管口处无淡蓝色火焰产生(该气体不是氢气,因为氢气具有可燃性,燃烧产生淡蓝色火焰)。
[学以致用]B装置可通过注射器控制液体的滴加速率,从而控制反应速率。
查看更多完整答案,请扫码查看


