第98页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
3. 在实验室,将$5.5g$氯酸钾和$2.5g$二氧化锰放在试管里加热,反应后称得剩余物质的质量为$7.2g$,那么剩余物质是( )
A.$MnO_{2}$和$KClO_{3}$
B.$KClO_{3}$
C.$KCl$和$KClO_{3}$
D.$MnO_{2}$、$KClO_{3}$和$KCl$
A.$MnO_{2}$和$KClO_{3}$
B.$KClO_{3}$
C.$KCl$和$KClO_{3}$
D.$MnO_{2}$、$KClO_{3}$和$KCl$
答案:
D
4. 镁在氧气与氮气的混合气体中燃烧不仅生成氧化镁,还有少量的镁与氮气化合生成氮化镁($Mg_{3}N_{2}$)。由此推知:$8g$镁在氧气与氮气的混合气体中完全燃烧,所得产物的质量可能是( )
A.$13.3g$
B.$12g$
C.$11.1g$
D.无法确定
A.$13.3g$
B.$12g$
C.$11.1g$
D.无法确定
答案:
B
5. [2024·湖南]老师和同学们在开展“基于特定需求设计和制作简易供氧器”的跨学科实践活动中,选取过氧化氢溶液和二氧化锰,利用供氧器制取氧气。回答下列问题:
(1)根据反应的化学方程式分析,过氧化氢的质量反应后比反应前________。
(2)现需要制得$3.2g$氧气,至少需要多少克溶质质量分数为$5\%$的过氧化氢溶液。(请写出计算过程)
(1)根据反应的化学方程式分析,过氧化氢的质量反应后比反应前________。
(2)现需要制得$3.2g$氧气,至少需要多少克溶质质量分数为$5\%$的过氧化氢溶液。(请写出计算过程)
答案:
5.
(1)减少
(2)解:设至少需要过氧化氢的质量为x。 2H₂O₂\stackrel{MnO₂}{=\!=\!=}2H₂O+O₂↑ 68 32 x 3.2g $\frac{68}{32}=\frac{x}{3.2g}$ x=6.8g 则至少需要溶质质量分数为5%的过氧化氢溶 液的质量为6.8g÷5%=136g。 答:至少需要136g溶质质量分数为5%的过氧 化氢溶液。
(1)减少
(2)解:设至少需要过氧化氢的质量为x。 2H₂O₂\stackrel{MnO₂}{=\!=\!=}2H₂O+O₂↑ 68 32 x 3.2g $\frac{68}{32}=\frac{x}{3.2g}$ x=6.8g 则至少需要溶质质量分数为5%的过氧化氢溶 液的质量为6.8g÷5%=136g。 答:至少需要136g溶质质量分数为5%的过氧 化氢溶液。
6. [2024·绥化节选]某毕业班同学去制纯碱的化工厂实习时,对该厂生产的纯碱产生了兴趣,于是取$10.7g$纯碱样品(含有少量的氯化钠)进行如下探究,完成以下问题。(已知:碳酸钠俗称纯碱,$Na_{2}CO_{3}+2HCl=2NaCl+H_{2}O+CO_{2}\uparrow$,酚酞在碳酸钠溶液中显红色)
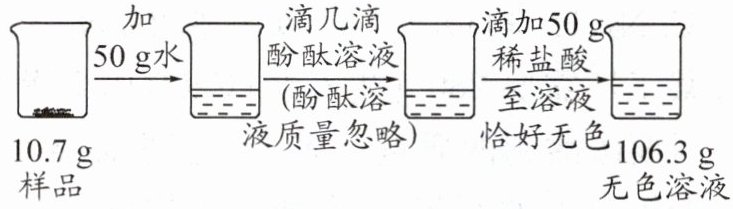
(1)该样品中碳酸钠的纯度是__________。(结果精确到$0.1\%$)
(2)将反应后的溶液恒温蒸发$6.3g$水,计算所得溶液中氯化钠的质量分数。

(1)该样品中碳酸钠的纯度是__________。(结果精确到$0.1\%$)
(2)将反应后的溶液恒温蒸发$6.3g$水,计算所得溶液中氯化钠的质量分数。
答案:
6.
(1)99.1%
(2)解:设纯碱样品中碳酸钠的质量为x,生成 NaCl的质量为y。 Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 106 117 44 x y 4.4g $\frac{106}{44}=\frac{x}{4.4g}$ x=10.6g $\frac{117}{44}=\frac{y}{4.4g}$ y=11.7g
(1)样品中碳酸钠的纯度: $\frac{10.6g}{10.7g}×100\%≈99.1\%$
(2)氯化钠的质量分数: $\frac{10.7g-10.6g+11.7g}{106.3g-6.3g}×100\%=11.8\%$ 答:所得溶液中氯化钠的质量分数是11.8%。
(1)99.1%
(2)解:设纯碱样品中碳酸钠的质量为x,生成 NaCl的质量为y。 Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 106 117 44 x y 4.4g $\frac{106}{44}=\frac{x}{4.4g}$ x=10.6g $\frac{117}{44}=\frac{y}{4.4g}$ y=11.7g
(1)样品中碳酸钠的纯度: $\frac{10.6g}{10.7g}×100\%≈99.1\%$
(2)氯化钠的质量分数: $\frac{10.7g-10.6g+11.7g}{106.3g-6.3g}×100\%=11.8\%$ 答:所得溶液中氯化钠的质量分数是11.8%。
7. (科学思维)[2024·镇江]已知:$2NaHCO_{3}\xlongequal{\triangle}Na_{2}CO_{3}+CO_{2}\uparrow +H_{2}O$,将$16.8gNaHCO_{3}$固体加热一段时间后,剩余固体质量为$13.7g$(已知:$NaHCO_{3}+HCl=NaCl+H_{2}O+CO_{2}\uparrow$,$Na_{2}CO_{3}+2HCl=2NaCl+H_{2}O+CO_{2}\uparrow$)。下列说法正确的是( )
A.原固体加热生成$3.1gCO_{2}$
B.加热后,固体中钠元素的质量分数减小
C.剩余固体中$NaHCO_{3}$和$Na_{2}CO_{3}$的质量比为$42:53$
D.将$13.7g$剩余固体溶于足量盐酸后,碳酸钠和碳酸氢钠都转化为$NaCl$,得$11.7gNaCl$
A.原固体加热生成$3.1gCO_{2}$
B.加热后,固体中钠元素的质量分数减小
C.剩余固体中$NaHCO_{3}$和$Na_{2}CO_{3}$的质量比为$42:53$
D.将$13.7g$剩余固体溶于足量盐酸后,碳酸钠和碳酸氢钠都转化为$NaCl$,得$11.7gNaCl$
答案:
D
查看更多完整答案,请扫码查看


