第97页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
2. $H_{2}$、$O_{2}$和$N_{2}$组成的混合气体$20g$,经点燃充分反应后生成$18g$水,剩余的气体不可能是( )
A.$N_{2}$和$H_{2}$
B.$N_{2}$和$O_{2}$
C.$N_{2}$、$H_{2}$和$O_{2}$
D.只有$2gN_{2}$
A.$N_{2}$和$H_{2}$
B.$N_{2}$和$O_{2}$
C.$N_{2}$、$H_{2}$和$O_{2}$
D.只有$2gN_{2}$
答案:
C
3. 某工厂需要$280g$生石灰($CaO$)作干燥剂,需要碳酸钙的质量是多少?至少需要含碳酸钙$80\%$的石灰石(杂质不参加反应)的质量是多少?(已知:$CaCO_{3}$在高温下分解生成$CaO$和$CO_{2}$)
答案:
3.解:设需要碳酸钙的质量为x。 CaCO₃$\stackrel{高温}{=\!=\!=}$CaO+CO₂↑ 100 56 x 280g $\frac{100}{56}=\frac{x}{280g}$ x=500g 需要含碳酸钙80%的石灰石的质量为500g÷ 80%=625g 答:需要碳酸钙的质量为500g,至少需要含碳酸 钙80%的石灰石的质量为625g。
1. [2024·淄博]硅化镁($Mg_{2}Si$)在能源器件、激光和半导体制造等领域具有重要应用价值,可通过石英砂(主要成分为$SiO_{2}$,杂质不含硅元素)和金属镁反应制得,反应的化学方程式为$SiO_{2}+4Mg\xlongequal{高温}Mg_{2}Si+2X$。
(1)化学方程式中$X$为__________(填化学式)。
(2)用$12.5kg$石英砂与足量镁充分反应得到$15.2kg$硅化镁,计算石英砂中$SiO_{2}$的质量分数。(写出计算过程)
(1)化学方程式中$X$为__________(填化学式)。
(2)用$12.5kg$石英砂与足量镁充分反应得到$15.2kg$硅化镁,计算石英砂中$SiO_{2}$的质量分数。(写出计算过程)
答案:
(1)MgO
(2)石英砂中SiO₂的质量分数为96%。
(1)MgO
(2)石英砂中SiO₂的质量分数为96%。
2. [2024·菏泽]超市卖的纯碱(碳酸钠的俗称)产品中,往往含有少量的$NaCl$。化学兴趣小组的同学要通过实验来测定某品牌纯碱样品中$Na_{2}CO_{3}$的质量分数。取$12g$纯碱样品放入烧杯中,加水完全溶解,逐滴加入一定溶质质量分数的$CaCl_{2}$溶液。产生沉淀的质量与加入$CaCl_{2}$溶液的质量关系如图所示。(已知:$Na_{2}CO_{3}+CaCl_{2}=CaCO_{3}\downarrow +2NaCl$)
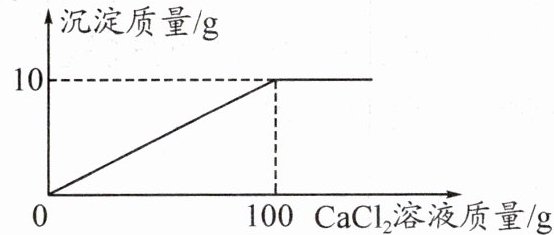
(1)完全反应后,生成沉淀的质量为_____g。
(2)计算纯碱样品中$Na_{2}CO_{3}$的质量分数。(结果精确到$0.1\%$)

(1)完全反应后,生成沉淀的质量为_____g。
(2)计算纯碱样品中$Na_{2}CO_{3}$的质量分数。(结果精确到$0.1\%$)
答案:
2.
(1)10
(2)解:设该纯碱样品中碳酸钠的质量为x。 Na₂CO₃+CaCl₂=CaCO₃↓+2NaCl 106 100 x 10g $\frac{106}{100}=\frac{x}{10g}$ x=10.6g 纯碱样品中Na₂CO₃的质量分数: $\frac{10.6g}{12g}×100\%≈88.3\%$ 答:纯碱样品中Na₂CO₃的质量分数为88.3%。
(1)10
(2)解:设该纯碱样品中碳酸钠的质量为x。 Na₂CO₃+CaCl₂=CaCO₃↓+2NaCl 106 100 x 10g $\frac{106}{100}=\frac{x}{10g}$ x=10.6g 纯碱样品中Na₂CO₃的质量分数: $\frac{10.6g}{12g}×100\%≈88.3\%$ 答:纯碱样品中Na₂CO₃的质量分数为88.3%。
查看更多完整答案,请扫码查看


