第71页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 质量守恒定律
内容:参加化学反应的各物质的
理解
一定不变
宏观:反应物和生成物的
微观:原子
一定改变
宏观:物质的种类一定改变
微观:分子的
可能改变:元素的
- 化学方程式
概念:用化学式表示化学反应的式子
意义
“质”:化学反应的反应物、生成物和反应条件
“量”
宏观:表示反应物、生成物之间的
微观:表示反应物、生成物之间的微粒
书写
原则:以客观事实为基础,遵守
步骤
写:写出反应物、生成物的化学式,注明化学反应的条件
配:配平化学方程式,把短线改为等号,注明生成物的状态
查:一查化学式是否正确;二查化学方程式是否配平;三查生成物状态是否标注、标注是否恰当;四查反应条件是否标明
根据化学方程式计算步骤:①根据题意,设未知量;②写出有关化学方程式;③写出相关物质的化学计量数与相对分子质量的乘积及质量;④列出比例式,求解;⑤简明地写出答案
内容:参加化学反应的各物质的
质量总和等于
,反应后生成的各物质的质量总和
理解
一定不变
宏观:反应物和生成物的
质量总和
不变,元素种类
不变,元素质量不变微观:原子
种类
不变,原子数目
不变,原子质量
不变(用于解释质量守恒的内在原因)一定改变
宏观:物质的种类一定改变
微观:分子的
种类
一定改变可能改变:元素的
化合价
可能改变,分子的数目
可能改变- 化学方程式
概念:用化学式表示化学反应的式子
意义
“质”:化学反应的反应物、生成物和反应条件
“量”
宏观:表示反应物、生成物之间的
质量比
微观:表示反应物、生成物之间的微粒
个数比
书写
原则:以客观事实为基础,遵守
质量守恒定律
步骤
写:写出反应物、生成物的化学式,注明化学反应的条件
配:配平化学方程式,把短线改为等号,注明生成物的状态
查:一查化学式是否正确;二查化学方程式是否配平;三查生成物状态是否标注、标注是否恰当;四查反应条件是否标明
根据化学方程式计算步骤:①根据题意,设未知量;②写出有关化学方程式;③写出相关物质的化学计量数与相对分子质量的乘积及质量;④列出比例式,求解;⑤简明地写出答案
答案:
质量总和等于 质量总和 质量总和 种类 种类 数目 质量 种类 化合价 数目 质量比 个数比 质量守恒定律
1.(2023年宜昌市改编)下列现象不能用质量守恒定律解释的是(
A.石蜡熔化前后,其质量不变
B.高锰酸钾受热分解后,剩余固体的质量比原反应物的质量小
C.木柴在空气中燃烧后化为灰烬,灰烬的质量比木柴的质量小
D.铜丝在空气中加热,生成物的质量比原来铜丝的质量大
A
)A.石蜡熔化前后,其质量不变
B.高锰酸钾受热分解后,剩余固体的质量比原反应物的质量小
C.木柴在空气中燃烧后化为灰烬,灰烬的质量比木柴的质量小
D.铜丝在空气中加热,生成物的质量比原来铜丝的质量大
答案:
A
2.(2023年泸州市)老师组织同学们对质量守恒定律进行了实验探究。回答相关问题:
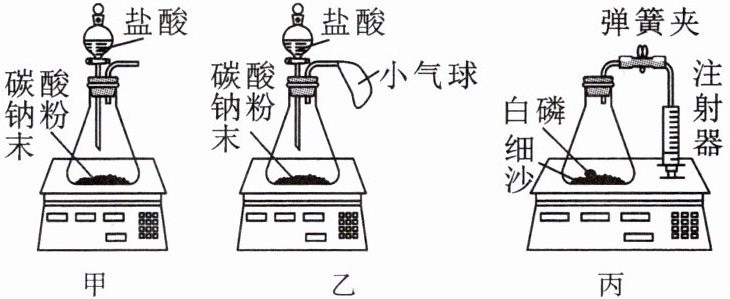
(1)第1组设计甲图的实验方案,用电子秤称量,读取加入盐酸前后的质量。反应的化学方程式为
(2)第2小组设计了乙图方案,以解决第1小组遇到的问题。但有同学认为会产生误差,他的理由是气球膨胀后不可忽略
(3)第3小组善于创新,设计了丙图方案,既达成本实验目的,还可以测定空气中氧气的含量。
①连接好装置后,打开弹簧夹,推或拉注射器活塞,松开手后活塞回到原位,说明气密性
②关闭弹簧夹,记录注射器初始读数,强光引燃白磷,冷却后打开弹簧夹。为保证锥形瓶内氧气完全反应,实验应采取的措施是

(1)第1组设计甲图的实验方案,用电子秤称量,读取加入盐酸前后的质量。反应的化学方程式为
Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
,比较读数发现反应前后的质量并不相等,其原因是反应生成CO₂逸出装置
。(2)第2小组设计了乙图方案,以解决第1小组遇到的问题。但有同学认为会产生误差,他的理由是气球膨胀后不可忽略
浮力
的影响。老师肯定了该同学勇于质疑、精益求精的科学精神。(3)第3小组善于创新,设计了丙图方案,既达成本实验目的,还可以测定空气中氧气的含量。
①连接好装置后,打开弹簧夹,推或拉注射器活塞,松开手后活塞回到原位,说明气密性
好
(选填“好”或“不好”)。②关闭弹簧夹,记录注射器初始读数,强光引燃白磷,冷却后打开弹簧夹。为保证锥形瓶内氧气完全反应,实验应采取的措施是
白磷足量
(任答1点);实验中需要测定的数据是锥形瓶(含导管)的容积、反应前后注射器的体积
。
答案:
(1)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 反应生成CO₂逸出装置
(2)浮力
(3)①好 ②白磷足量 反应前后注射器的体积
(1)Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑ 反应生成CO₂逸出装置
(2)浮力
(3)①好 ②白磷足量 反应前后注射器的体积
查看更多完整答案,请扫码查看


