2024年优加学案课时通九年级化学全一册鲁教版54制
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2024年优加学案课时通九年级化学全一册鲁教版54制 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第50页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
16. 现有一包白色固体,可能由碳酸钠、碳酸氢钠、氯化钠中的一种或多种物质组成。取10 g固体加入100 g溶质质量分数为7.3%的稀盐酸中,充分反应后,经测定溶液质量增加了5.6 g。下列说法正确的是( )
A. 白色固体可能是纯净物
B. 白色固体中一定有碳酸氢钠
C. 将溶液蒸干,得到氯化钠固体的质量一定为11.7 g
D. 向溶液中滴加硝酸银溶液,产生白色沉淀,该现象说明固体中一定有氯化钠
A. 白色固体可能是纯净物
B. 白色固体中一定有碳酸氢钠
C. 将溶液蒸干,得到氯化钠固体的质量一定为11.7 g
D. 向溶液中滴加硝酸银溶液,产生白色沉淀,该现象说明固体中一定有氯化钠
答案:
答案:B
解析:由题意可知,10g固体加入100g溶质质量分数为7.3%的稀盐酸中,充分反应后,经测定溶液质量增加了5.6g,说明生成二氧化碳的质量为10g - 5.6g = 4.4g。若白色固体全部是碳酸钠,设生成4.4g二氧化碳所需碳酸钠的质量为x,生成氯化钠的质量为a。
$\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$
106 117 44
x a 4.4g
$\frac{106}{44}=\frac{x}{4.4\ g}$ $x = 10.6\ g>10\ g$
$\frac{117}{44}=\frac{a}{4.4\ g}$ $a = 11.7\ g$
若白色固体全部是碳酸氢钠,设生成4.4g二氧化碳所需碳酸氢钠的质量为y,生成氯化钠的质量为b。
$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$
84 58.5 44
y b 4.4g
$\frac{84}{44}=\frac{y}{4.4\ g}$ $y = 8.4\ g<10\ g$
$\frac{58.5}{44}=\frac{b}{4.4\ g}$ $b = 5.85\ g$
若白色固体全部是氯化钠,无二氧化碳生成,则溶液质量增加10g。由此可知,原白色固体中一定有碳酸氢钠,可能含有碳酸钠、氯化钠中的一种或两种。由以上分析可知,A不正确,B正确;若白色固体全部是碳酸钠,则生成的氯化钠质量为11.7g,该白色固体不全是碳酸钠,所以将溶液蒸干,得到氯化钠固体的质量一定小于11.7g,C不正确;碳酸氢钠与盐酸反应生成了氯化钠,则向溶液中滴加硝酸银溶液,也会产生白色沉淀,则该现象不能说明固体中一定含有氯化钠,D不正确。
解析:由题意可知,10g固体加入100g溶质质量分数为7.3%的稀盐酸中,充分反应后,经测定溶液质量增加了5.6g,说明生成二氧化碳的质量为10g - 5.6g = 4.4g。若白色固体全部是碳酸钠,设生成4.4g二氧化碳所需碳酸钠的质量为x,生成氯化钠的质量为a。
$\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$
106 117 44
x a 4.4g
$\frac{106}{44}=\frac{x}{4.4\ g}$ $x = 10.6\ g>10\ g$
$\frac{117}{44}=\frac{a}{4.4\ g}$ $a = 11.7\ g$
若白色固体全部是碳酸氢钠,设生成4.4g二氧化碳所需碳酸氢钠的质量为y,生成氯化钠的质量为b。
$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$
84 58.5 44
y b 4.4g
$\frac{84}{44}=\frac{y}{4.4\ g}$ $y = 8.4\ g<10\ g$
$\frac{58.5}{44}=\frac{b}{4.4\ g}$ $b = 5.85\ g$
若白色固体全部是氯化钠,无二氧化碳生成,则溶液质量增加10g。由此可知,原白色固体中一定有碳酸氢钠,可能含有碳酸钠、氯化钠中的一种或两种。由以上分析可知,A不正确,B正确;若白色固体全部是碳酸钠,则生成的氯化钠质量为11.7g,该白色固体不全是碳酸钠,所以将溶液蒸干,得到氯化钠固体的质量一定小于11.7g,C不正确;碳酸氢钠与盐酸反应生成了氯化钠,则向溶液中滴加硝酸银溶液,也会产生白色沉淀,则该现象不能说明固体中一定含有氯化钠,D不正确。
17. (科学探究与实践)明明同学发现妈妈蒸馒头时常用到发酵粉或碱面。查阅标签得知:发酵粉的主要成分是碳酸氢钠和有机酸,碱面的主要成分是碳酸钠。他和小组同学一起展开了一系列的探究活动:
[实验一]碳酸氢钠和碳酸钠都为白色粉末状固体。分别取两种固体少量于试管中,加水振荡至充分溶解,得到无色溶液。
[实验二](1)在白色点滴板里进行如图甲所示实验,观察到溶液都变成______色。
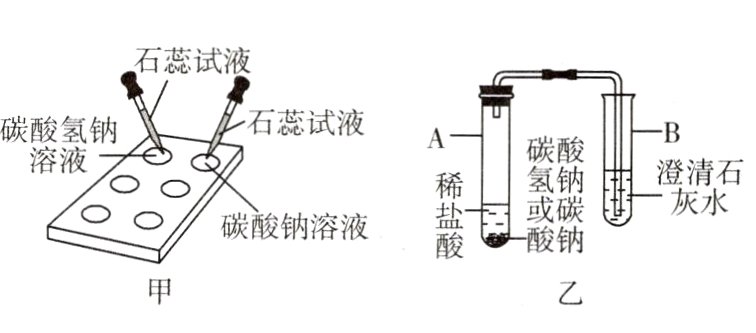
(2)如图乙所示,分别取适量碳酸氢钠和碳酸钠粉末于试管中,滴加稀盐酸。观察到试管A中都__________,试管B中澄清石灰水都变浑浊。写出试管A中反应的化学方程式:____________________(任写一个)。
[总结]以上实验说明,碳酸氢钠和碳酸钠溶液都呈______性,都能与稀盐酸反应生成二氧化碳气体。所以发酵粉或碱面能用来蒸馒头,是因为____________________。
芳芳提出猜想:蒸馒头时温度比较高,会不会是受热后它们都分解了呢?
[实验三]芳芳和小组同学一起设计方案,实验装置如图所示,请完成实验报告。
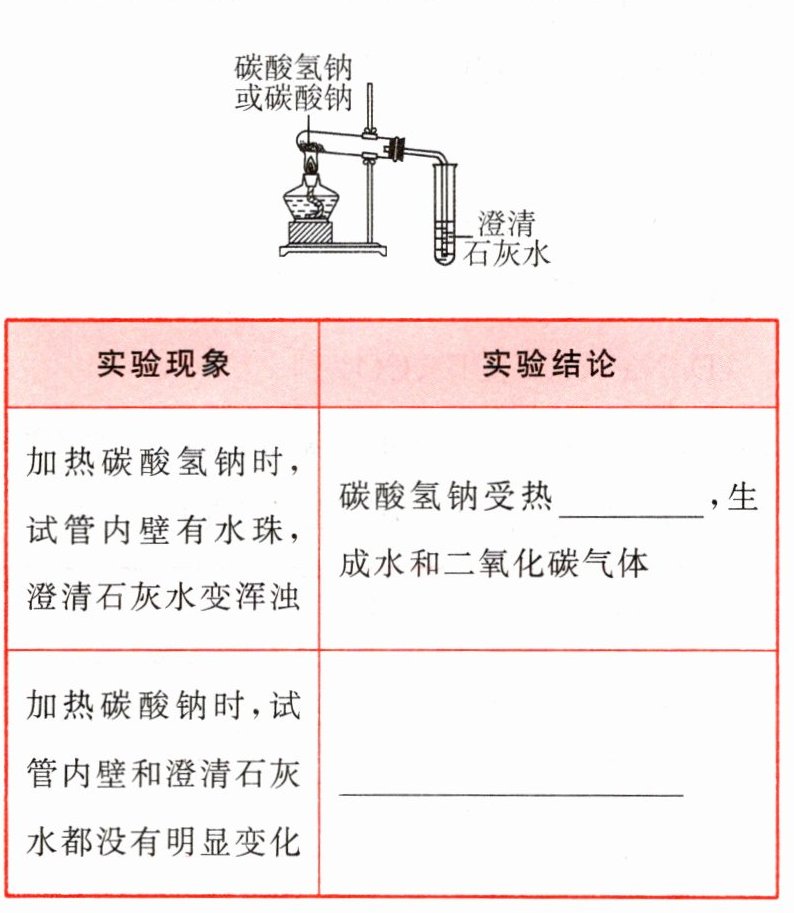
[结论]由此可知,芳芳的猜想______(填“正确”或“不正确”)。
[实验一]碳酸氢钠和碳酸钠都为白色粉末状固体。分别取两种固体少量于试管中,加水振荡至充分溶解,得到无色溶液。
[实验二](1)在白色点滴板里进行如图甲所示实验,观察到溶液都变成______色。

(2)如图乙所示,分别取适量碳酸氢钠和碳酸钠粉末于试管中,滴加稀盐酸。观察到试管A中都__________,试管B中澄清石灰水都变浑浊。写出试管A中反应的化学方程式:____________________(任写一个)。
[总结]以上实验说明,碳酸氢钠和碳酸钠溶液都呈______性,都能与稀盐酸反应生成二氧化碳气体。所以发酵粉或碱面能用来蒸馒头,是因为____________________。
芳芳提出猜想:蒸馒头时温度比较高,会不会是受热后它们都分解了呢?
[实验三]芳芳和小组同学一起设计方案,实验装置如图所示,请完成实验报告。

[结论]由此可知,芳芳的猜想______(填“正确”或“不正确”)。
答案:
答案:[实验二]
(1)蓝
(2)产生气泡 $\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$(或$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$)
[总结]碱 碳酸氢钠、碳酸钠都能中和发面中产生的酸,并生成二氧化碳气体,使馒头膨松
[实验三]分解 碳酸钠受热不分解
[结论]不正确
解析:[实验二]
(1)碳酸氢钠和碳酸钠溶液都显碱性,能使紫色石蕊试液变蓝。
(2)碳酸氢钠和碳酸钠都能与稀盐酸反应产生二氧化碳气体,所以观察到试管A中都产生气泡;反应的化学方程式可以是$\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$或$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$。
[总结]碳酸氢钠和碳酸钠溶液都呈碱性,都能与稀盐酸反应生成二氧化碳气体。发酵粉或碱面能用来蒸馒头,是因为碳酸氢钠、碳酸钠都能中和发面中产生的酸,并生成二氧化碳气体,使馒头膨松。
[实验三]加热碳酸氢钠时,试管内壁有水珠,澄清石灰水变浑浊,说明碳酸氢钠受热分解,生成水和二氧化碳气体;加热碳酸钠时,试管内壁和澄清石灰水都没有明显变化,说明碳酸钠受热不分解。
[结论]由实验可知,只有碳酸氢钠受热分解,碳酸钠受热不分解,所以芳芳的猜想不正确。
(1)蓝
(2)产生气泡 $\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$(或$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$)
[总结]碱 碳酸氢钠、碳酸钠都能中和发面中产生的酸,并生成二氧化碳气体,使馒头膨松
[实验三]分解 碳酸钠受热不分解
[结论]不正确
解析:[实验二]
(1)碳酸氢钠和碳酸钠溶液都显碱性,能使紫色石蕊试液变蓝。
(2)碳酸氢钠和碳酸钠都能与稀盐酸反应产生二氧化碳气体,所以观察到试管A中都产生气泡;反应的化学方程式可以是$\mathrm{Na}_{2}\mathrm{CO}_{3}+2\mathrm{HCl}\xlongequal{\;\;}2\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$或$\mathrm{NaHCO}_{3}+\mathrm{HCl}\xlongequal{\;\;}\mathrm{NaCl}+\mathrm{H}_{2}\mathrm{O}+\mathrm{CO}_{2}\uparrow$。
[总结]碳酸氢钠和碳酸钠溶液都呈碱性,都能与稀盐酸反应生成二氧化碳气体。发酵粉或碱面能用来蒸馒头,是因为碳酸氢钠、碳酸钠都能中和发面中产生的酸,并生成二氧化碳气体,使馒头膨松。
[实验三]加热碳酸氢钠时,试管内壁有水珠,澄清石灰水变浑浊,说明碳酸氢钠受热分解,生成水和二氧化碳气体;加热碳酸钠时,试管内壁和澄清石灰水都没有明显变化,说明碳酸钠受热不分解。
[结论]由实验可知,只有碳酸氢钠受热分解,碳酸钠受热不分解,所以芳芳的猜想不正确。
查看更多完整答案,请扫码查看


