第62页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
13. 将露置在空气中已部分变质的 $NaOH$ 样品,溶于水配成溶液,向其中滴加过量的稀盐酸。随着加入盐酸体积的变化,下列示意图能正确反映其中变化的是(
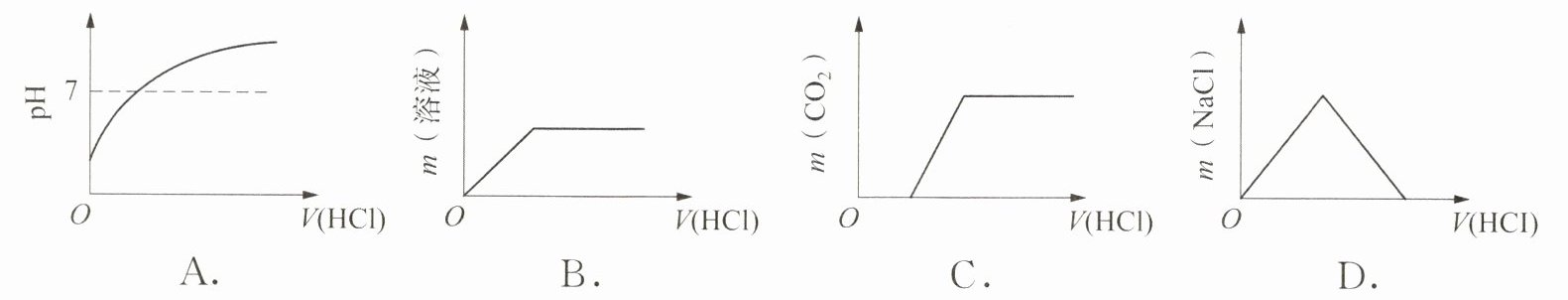
A.
B.
C.
D.
C
)
A.
B.
C.
D.
答案:
13.C
14. 相同质量的①$Na_2CO_3$、②$CaCO_3$、③$MgCO_3$、④$NaHCO_3$,分别加入足量的稀盐酸,产生 $CO_2$ 的质量(
A.相同
B.①最少
C.②最多
D.③最多
B
)A.相同
B.①最少
C.②最多
D.③最多
答案:
14.B [解析]题干中的四种物质均可与稀盐酸反应产生$CO_2$,当生成$44g$ $CO_2$时,需要$Na_2CO_3$、$CaCO_3$、$MgCO_3$、$NaHCO_3$的质量分别为$106g$、$100g$、$84g$、$84g$。所以等质量的四种物质,与足量的稀盐酸反应,产生$CO_2$最少的是$Na_2CO_3$,而$MgCO_3$和$NaHCO_3$产生的$CO_2$量一样多。
15. 下列各组物质中,含有相同酸根的是(
A.$HCl$、$HClO_3$
B.$Na_2SO_4$、$Na_2SO_3$
C.$Ca(NO_3)_2$、$KNO_3$
D.$KMnO_4$、$K_2MnO_4$
C
)A.$HCl$、$HClO_3$
B.$Na_2SO_4$、$Na_2SO_3$
C.$Ca(NO_3)_2$、$KNO_3$
D.$KMnO_4$、$K_2MnO_4$
答案:
15.C [解析]A.$HCl$、$HClO_3$的酸根分别是盐酸根和氯酸根。B.$Na_2SO_4$、$Na_2SO_3$的酸根分别是硫酸根和亚硫酸根。C.$Ca(NO_3)_2$、$KNO_3$的酸根都是硝酸根。D.$KMnO_4$、$K_2MnO_4$的酸根分别为高锰酸根和锰酸根。故选项C正确。
16. 以化合价为纵坐标,以物质类别为横坐标绘制的图像叫“价类二维图”。如图所示为铁元素的“价类二维图”。下列说法中正确的是(
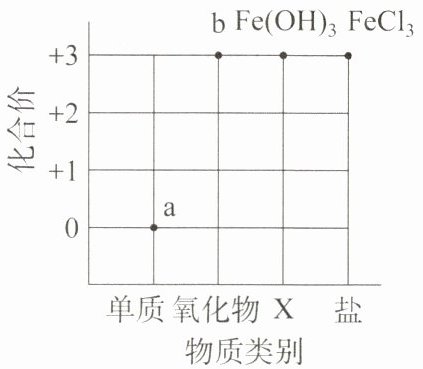
A.X 是碱
B.物质 a 可与稀盐酸反应生成 $FeCl_3$
C.物质 b 可与稀盐酸反应生成 $FeCl_2$
D.$FeCl_3$ 溶液可与 $NaOH$ 溶液反应生成 $Fe(OH)_3$
AD
)
A.X 是碱
B.物质 a 可与稀盐酸反应生成 $FeCl_3$
C.物质 b 可与稀盐酸反应生成 $FeCl_2$
D.$FeCl_3$ 溶液可与 $NaOH$ 溶液反应生成 $Fe(OH)_3$
答案:
16.AD
17. 某固体废弃物中,可能含有 $BaCl_2$、$Na_2SO_4$、$NaOH$、$CaCO_3$、$MgCl_2$ 中的一种或几种,为确定其组成,取样,进行如下实验。下列对该样品的分析正确的是(

A.可能含 $Na_2SO_4$
B.可能含 $CaCO_3$
C.一定不含 $MgCl_2$
D.一定含 $BaCl_2$
D
)
A.可能含 $Na_2SO_4$
B.可能含 $CaCO_3$
C.一定不含 $MgCl_2$
D.一定含 $BaCl_2$
答案:
17.D [解析]①滤渣中能和稀盐酸反应产生气体的只有$CaCO_3$,气体是$CO_2$。生成$0.44g$ $CO_2$需要$1g$ $CaCO_3$,现在滤渣有$1.4g$说明还有其他溶于酸的沉淀,即$Mg(OH)_2$。因此固体中一定有$NaOH$、$CaCO_3$、$MgCl_2$。②滤液中通入$CO_2$产生的白色沉淀,只能是$CO_2$先和$NaOH$反应生成$Na_2CO_3$,$Na_2CO_3$再与$BaCl_2$反应生成的$BaCO_3$。③因为滤渣全部溶于稀盐酸,所以滤渣中不会有$BaSO_4$。由②的分析得知样品中一定有$BaCl_2$,就一定没有$Na_2SO_4$。故选项D正确。
18. 中和反应是一类重要的化学反应。
(1)小组同学将氢氧化钠溶液和稀盐酸混合反应,实验装置如右图,采用无色酚酞试液做酸碱指示剂,用传感器分别测定溶液 pH、溶液温度的变化情况(见下页表)。写出该中和反应的化学方程式:
(2)混合前,烧杯内的是
(3)当滴加液体体积为______mL 时,酸碱中和反应恰好完成。根据表格数据可判断:中和反应是______(填“吸热”或“放热”)的反应,理由是:_。
(4)当滴加液体体积为 6 mL 时,烧杯中的溶质(除酚酞以外)有
(5)有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因:________________________,请设计实验证明你的结论:_。
(6)现有两杯质量相同、溶质质量分数相同的 $NaOH$ 溶液和 $KOH$ 溶液,在 $NaOH$ 溶液中加入 x g 盐酸恰好中和;在 $KOH$ 溶液中加入 y g 上述盐酸也能恰好中和,则 x

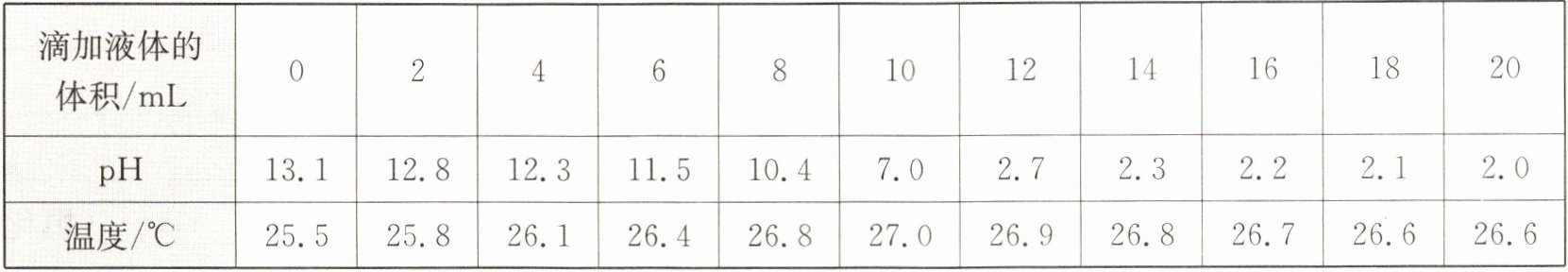
(1)小组同学将氢氧化钠溶液和稀盐酸混合反应,实验装置如右图,采用无色酚酞试液做酸碱指示剂,用传感器分别测定溶液 pH、溶液温度的变化情况(见下页表)。写出该中和反应的化学方程式:
NaOH + HCl = NaCl + H_2O
。(2)混合前,烧杯内的是
NaOH
溶液,判断的依据是一开始溶液的pH>7,呈碱性
。(3)当滴加液体体积为______mL 时,酸碱中和反应恰好完成。根据表格数据可判断:中和反应是______(填“吸热”或“放热”)的反应,理由是:_。
(4)当滴加液体体积为 6 mL 时,烧杯中的溶质(除酚酞以外)有
NaOH、NaCl
(填化学式)。(5)有同学发现在实验过程中,开始时没有气泡,持续滴加液体后,观察到有气泡产生,请分析可能的原因:________________________,请设计实验证明你的结论:_。
(6)现有两杯质量相同、溶质质量分数相同的 $NaOH$ 溶液和 $KOH$ 溶液,在 $NaOH$ 溶液中加入 x g 盐酸恰好中和;在 $KOH$ 溶液中加入 y g 上述盐酸也能恰好中和,则 x
>
(填“>”“<”或“=”)y。

答案:
18.
(1)$NaOH + HCl = NaCl + H_2O$
(2)$NaOH$一开始溶液的$pH>7$,呈碱性
(3)10放热 反应开始后,温度不断升高;反应结束,温度不再升高
(4)$NaOH$、$NaCl$
(5)氢氧化钠部分变质产生碳酸钠 取烧杯中液体加入氯化钙溶液,若产生白色沉淀,则说明氢氧化钠中含碳酸钠(也可使用氯化钡溶液、氢氧化钡等溶液,不可用稀盐酸)
(6)>
(1)$NaOH + HCl = NaCl + H_2O$
(2)$NaOH$一开始溶液的$pH>7$,呈碱性
(3)10放热 反应开始后,温度不断升高;反应结束,温度不再升高
(4)$NaOH$、$NaCl$
(5)氢氧化钠部分变质产生碳酸钠 取烧杯中液体加入氯化钙溶液,若产生白色沉淀,则说明氢氧化钠中含碳酸钠(也可使用氯化钡溶液、氢氧化钡等溶液,不可用稀盐酸)
(6)>
查看更多完整答案,请扫码查看


