第44页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
12. 下列关于复分解反应的说法中正确的是 (
A.反应物为酸和碱
B.都伴随有明显的现象
C.生成物为盐和水
D.反应前后元素的化合价不变
D
)A.反应物为酸和碱
B.都伴随有明显的现象
C.生成物为盐和水
D.反应前后元素的化合价不变
答案:
12.D
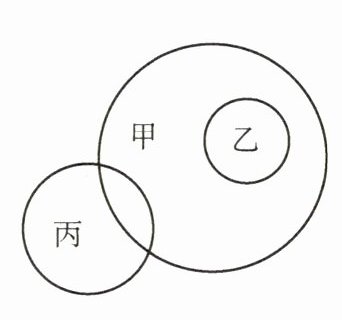
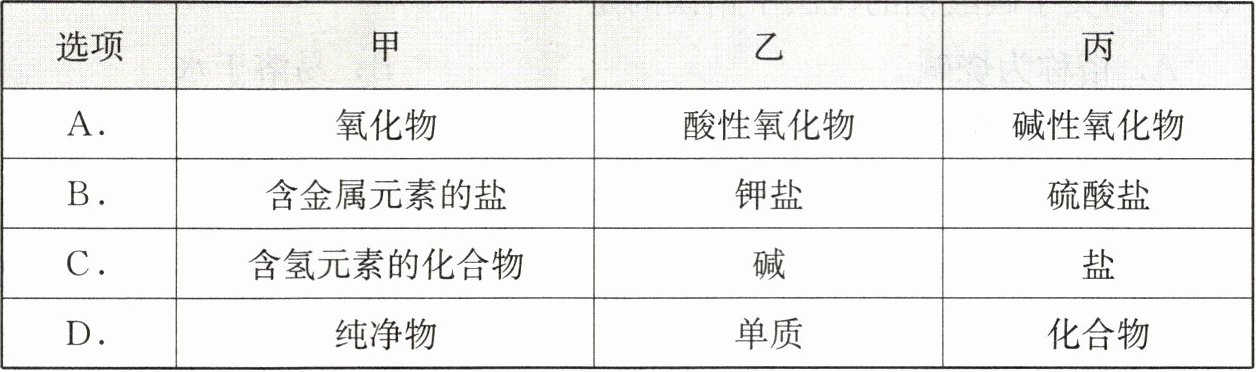
13. 如图表示甲、乙、丙三类物质的相互关系,甲包含全部乙、部分丙和其他物质。下表中符合图示关系的是 (
C
)

答案:
13.C [解析]酸性氧化物和碱性氧化物都属于氧化物,因此甲包含乙和丙,所以选项A错误。钾盐属于含金属元素的盐,因此甲包含乙。但硫酸盐中有硫酸钾,它也属于钾盐,乙和丙应该有重合,所以选项B错误。碱一定含有氢元素,因此甲包含乙。有NH₄Cl、NaHCO₃等含有氢元素的盐,也有NaCl、CuSO₄等不含氢元素的盐,所以甲和丙有部分重合。碱和盐属于两类物质,无重合,因此选项C正确。单质和化合物都属于纯净物,所以甲应该包含乙和丙,所以选项D错误。
二、简答题
$NH_{4}Cl + X\downarrow$},请回答以下问题。
(1) 氯化铵属于
(2) {NaCl}中的正离子为
(3) 本反应涉及
$NH_{4}Cl + X\downarrow$},请回答以下问题。
(1) 氯化铵属于
盐
(填“酸”“碱”或“盐”),{X}的化学式为NaHCO₃
。(2) {NaCl}中的正离子为
Na⁺
(填符号)。(3) 本反应涉及
3
种盐,2
种氧化物。
答案:
14.
(1)盐 NaHCO₃
(2)Na⁺
(3)3 2
(1)盐 NaHCO₃
(2)Na⁺
(3)3 2
15. 小明在家中厨房找到一种白色粉末${A}$,到化学实验室进行实验,结果如下图所示,请回答下列问题。

(1) 若${A}$的组成中不含氢元素,则${A}$的名称是
(2) 若${A}$的组成中含有氢元素,则${A}$的名称是
(3) 写出${D}\to{E}$转化的化学反应方程式:

(1) 若${A}$的组成中不含氢元素,则${A}$的名称是
碳酸钠(或纯碱、苏打)
,它与石灰水反应的化学方程式为Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH
。(2) 若${A}$的组成中含有氢元素,则${A}$的名称是
碳酸氢钠(或小苏打)
,它与盐酸反应的化学方程式为NaHCO₃+HCl=NaCl+H₂O+CO₂↑
。(3) 写出${D}\to{E}$转化的化学反应方程式:
Ca(OH)₂+CO₂=CaCO₃↓+H₂O
。
答案:
15.
(1)碳酸钠(或纯碱、苏打) Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH
(2)碳酸氢钠(或小苏打) NaHCO₃+HCl=NaCl+H₂O+CO₂↑
(3)Ca(OH)₂+CO₂=CaCO₃↓+H₂O
(1)碳酸钠(或纯碱、苏打) Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH
(2)碳酸氢钠(或小苏打) NaHCO₃+HCl=NaCl+H₂O+CO₂↑
(3)Ca(OH)₂+CO₂=CaCO₃↓+H₂O
16. 氯化钠是一种重要的化工原料,电解饱和氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下。
${2NaCl + 2H_{2}O\xlongequal{通直流电}2NaOH + H_{2}\uparrow + Cl_{2}\uparrow}$
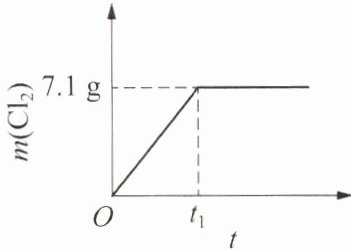
现取一定质量溶质质量分数为$26.5\%$的氯化钠溶液进行电解,反应一段时间后,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
(1) 参加反应的氯化钠的质量(写出计算过程)。
(2) 这些质量的氯化钠可配制$26.5\%$的氯化钠溶液的质量为
${2NaCl + 2H_{2}O\xlongequal{通直流电}2NaOH + H_{2}\uparrow + Cl_{2}\uparrow}$
现取一定质量溶质质量分数为$26.5\%$的氯化钠溶液进行电解,反应一段时间后,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
(1) 参加反应的氯化钠的质量(写出计算过程)。
(2) 这些质量的氯化钠可配制$26.5\%$的氯化钠溶液的质量为
$\frac{11.7}{26.5%}$
${g}$(列式即可)。
答案:
16.
(1)[解]设:参加反应的氯化钠的质量为x。$ 2NaCl+2H₂O\overset{通直流电}=2NaOH+H₂↑+Cl₂↑ 117 71 x 7.1g \frac{117}{71}=\frac{x}{7.1g} x=11.7g $答:参加反应的氯化钠的质量为11.7g。$ (2)\frac{11.7}{26.5%}$
(1)[解]设:参加反应的氯化钠的质量为x。$ 2NaCl+2H₂O\overset{通直流电}=2NaOH+H₂↑+Cl₂↑ 117 71 x 7.1g \frac{117}{71}=\frac{x}{7.1g} x=11.7g $答:参加反应的氯化钠的质量为11.7g。$ (2)\frac{11.7}{26.5%}$
查看更多完整答案,请扫码查看


