第88页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
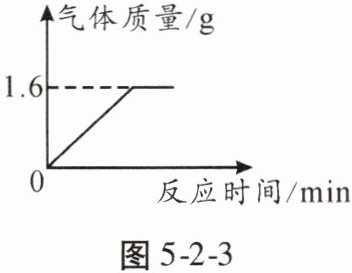
7. 某校九年级综合实践小组用一定量的过氧化氢溶液和二氧化锰来制取氧气,所得气体质量与反应时间的关系如图5-2-3所示。请计算所用过氧化氢溶液中过氧化氢的质量。

答案:
解:设过氧化氢溶液中过氧化氢的质量为x。
${2H_2O_2\xlongequal{{MnO_2}}2H_2O + O_2\uparrow}$
68 32
x 1.6 g
$\frac{68}{32}=\frac{x}{1.6\ g}$
$x=3.4\ g$
答:过氧化氢溶液中过氧化氢的质量为3.4 g。
${2H_2O_2\xlongequal{{MnO_2}}2H_2O + O_2\uparrow}$
68 32
x 1.6 g
$\frac{68}{32}=\frac{x}{1.6\ g}$
$x=3.4\ g$
答:过氧化氢溶液中过氧化氢的质量为3.4 g。
8. 相同质量的铁、磷、镁分别在氧气中完全燃烧,消耗氧气最多的是( )
A.铁
B.磷
C.镁
D.一样多
A.铁
B.磷
C.镁
D.一样多
答案:
B
9. 侯德榜是我国著名的化学家,发明了侯氏制碱法,其反应原理之一如下:$NaCl+CO_2+NH_3+H_2O= NaHCO_3↓+NH_4Cl。$请计算:
(1) 氯化铵中氮元素的质量分数。(计算结果保留一位小数)
(2) 生产8.4t碳酸氢钠,理论上需要氯化钠的质量。
(1) 氯化铵中氮元素的质量分数。(计算结果保留一位小数)
(2) 生产8.4t碳酸氢钠,理论上需要氯化钠的质量。
答案:
(1)氯化铵中氮元素的质量分数为$\frac{14}{53.5}× 100\%\approx 26.2\%$。
(2)解:设生产8.4 t碳酸氢钠,理论上需要氯化钠的质量为x。
${NaCl + CO_2 + NH_3 + H_2O=NaHCO_3\downarrow + NH_4Cl}$
58.5 84
x 8.4 t
$\frac{58.5}{x}=\frac{84}{8.4\ t}$
$x=5.85\ t$
答:生产8.4 t碳酸氢钠,理论上需要氯化钠的质量为5.85 t。
(1)氯化铵中氮元素的质量分数为$\frac{14}{53.5}× 100\%\approx 26.2\%$。
(2)解:设生产8.4 t碳酸氢钠,理论上需要氯化钠的质量为x。
${NaCl + CO_2 + NH_3 + H_2O=NaHCO_3\downarrow + NH_4Cl}$
58.5 84
x 8.4 t
$\frac{58.5}{x}=\frac{84}{8.4\ t}$
$x=5.85\ t$
答:生产8.4 t碳酸氢钠,理论上需要氯化钠的质量为5.85 t。
10. 二氧化硫是一种无色、具有刺激性气味的气体,它进入大气后可形成硫酸型酸雨。用石灰石浆可吸收废气中的二氧化硫,其反应原理是$2CaCO_3+O_2+2SO_2= 2CaSO_4+2CO_2。$若1000kg废气中含有1.6kg二氧化硫,则至少需要多少千克含90%碳酸钙的石灰石才能将1000kg废气中含有的二氧化硫完全吸收?(计算结果保留一位小数)
答案:
解:设需要碳酸钙的质量为x。
${2CaCO_3 + 2SO_2 + O_2=2CaSO_4 + 2CO_2}$
200 128
x 1.6 kg
$\frac{200}{128}=\frac{x}{1.6\ kg}\quad x=2.5\ kg$
需要石灰石的质量=$\frac{2.5}{90\%}\approx 2.8\ kg$
答:需要石灰石的质量约为2.8 kg。
${2CaCO_3 + 2SO_2 + O_2=2CaSO_4 + 2CO_2}$
200 128
x 1.6 kg
$\frac{200}{128}=\frac{x}{1.6\ kg}\quad x=2.5\ kg$
需要石灰石的质量=$\frac{2.5}{90\%}\approx 2.8\ kg$
答:需要石灰石的质量约为2.8 kg。
查看更多完整答案,请扫码查看


