第83页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
15. 某同学欲用①NaOH溶液、②$Na_{2}SO_{4}$溶液、③$Na_{2}CO_{3}$粉末、④铁钉、⑤$Ba(NO_{3})_{2}溶液分别与稀H_{2}SO_{4}$混合来验证复分解反应发生的条件。(如图)
(1)从物质类别和构成的角度分析,铁钉、______与稀$H_{2}SO_{4}$混合的实验没有必要做。
(2)上述物质中,______能与稀硫酸发生复分解反应,但是没有明显现象;为证明两者能够反应,你的做法是______。
(3)$Na_{2}CO_{3}粉末和稀H_{2}SO_{4}$能发生反应,是因为反应中有______生成。
(4)依据常见酸、碱、盐的溶解性表(室温),某物质能与稀$H_{2}SO_{4}$发生中和反应,同时生成水和沉淀,写出反应的化学方程式:______。

(1)从物质类别和构成的角度分析,铁钉、______与稀$H_{2}SO_{4}$混合的实验没有必要做。
(2)上述物质中,______能与稀硫酸发生复分解反应,但是没有明显现象;为证明两者能够反应,你的做法是______。
(3)$Na_{2}CO_{3}粉末和稀H_{2}SO_{4}$能发生反应,是因为反应中有______生成。
(4)依据常见酸、碱、盐的溶解性表(室温),某物质能与稀$H_{2}SO_{4}$发生中和反应,同时生成水和沉淀,写出反应的化学方程式:______。

答案:
(1)$Na_{2}SO_{4}$溶液
(2)$NaOH$溶液 先向$NaOH$溶液中滴加酚酞溶液,后加稀硫酸(合理即可)
(3)气体
(4)$H_{2}SO_{4}+Ba(OH)_{2}=BaSO_{4}\downarrow +2H_{2}O$
(1)$Na_{2}SO_{4}$溶液
(2)$NaOH$溶液 先向$NaOH$溶液中滴加酚酞溶液,后加稀硫酸(合理即可)
(3)气体
(4)$H_{2}SO_{4}+Ba(OH)_{2}=BaSO_{4}\downarrow +2H_{2}O$
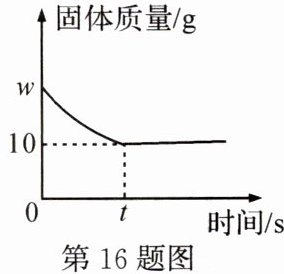
16. 自然界有一种含镁矿石,经处理后得到只含$MgCO_{3}和Mg(OH)_{2}$的混合物,可作生产耐火材料氧化镁的原料。为确定其组成,现各取w g样品两份,第一份样品加过量稀盐酸,生成气体8.8g;第二份样品加热,固体质量与反应时间的变化关系如图所示,化学方程式:$MgCO_{3}\xlongequal{\triangle}MgO+CO_{2}\uparrow$;$Mg(OH)_{2}\xlongequal{\triangle}MgO+H_{2}O\uparrow$。下列说法错误的是( )
A.$MgCO_{3}和Mg(OH)_{2}$的混合物可用作防火材料
B.样品中$MgCO_{3}与Mg(OH)_{2}$的质量比为168:58
C.第二份样品加热后,固体中镁元素的质量分数变大
D.两份样品充分反应后,生成$CO_{2}$气体的质量相等

A.$MgCO_{3}和Mg(OH)_{2}$的混合物可用作防火材料
B.样品中$MgCO_{3}与Mg(OH)_{2}$的质量比为168:58
C.第二份样品加热后,固体中镁元素的质量分数变大
D.两份样品充分反应后,生成$CO_{2}$气体的质量相等
答案:
B
17. 农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素。
(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要施用氮肥来补充,下列属于氮肥的是______(填序号)。
①KCl
②$NH_{4}HCO_{3}$
③$Ca_{3}(PO_{4})_{2}$
(2)“测土配方”技术可以实现“缺什么、补什么”,使用该技术的好处是______。
(3)某同学取“××”牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙所示。试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(反应方程式为$K_{2}SO_{4}+BaCl_{2}= BaSO_{4}\downarrow +2KCl$,杂质不参加反应)

(1)氮是植物生长的重要元素,果园土壤中缺少氮元素,需要施用氮肥来补充,下列属于氮肥的是______(填序号)。
①KCl
②$NH_{4}HCO_{3}$
③$Ca_{3}(PO_{4})_{2}$
(2)“测土配方”技术可以实现“缺什么、补什么”,使用该技术的好处是______。
(3)某同学取“××”牌钾肥(如图甲)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如图乙所示。试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(反应方程式为$K_{2}SO_{4}+BaCl_{2}= BaSO_{4}\downarrow +2KCl$,杂质不参加反应)

答案:
(1)②
(2)能够为农作物提供各种营养元素(合理即可)
(3)设$2.0g$钾肥样品中硫酸钾的质量为$x$,$K_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2KCl$$174$ $233$$x$ $2.33g$$\frac {174}{233}=\frac {x}{2.33g}$$x=1.74g$硫酸钾的质量分数为:$\frac {1.74}{2}×100\% =87\% ,87\% >85\% ,$因此该钾肥中硫酸钾的质量分数符合产品外包装说明。
(1)②
(2)能够为农作物提供各种营养元素(合理即可)
(3)设$2.0g$钾肥样品中硫酸钾的质量为$x$,$K_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2KCl$$174$ $233$$x$ $2.33g$$\frac {174}{233}=\frac {x}{2.33g}$$x=1.74g$硫酸钾的质量分数为:$\frac {1.74}{2}×100\% =87\% ,87\% >85\% ,$因此该钾肥中硫酸钾的质量分数符合产品外包装说明。
查看更多完整答案,请扫码查看


