第64页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
例1 酸、碱、盐在生活、生产中应用广泛,使用时必须十分小心,氢氧化钠具有强烈的______,实验时最好戴防护眼镜,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求回答下列问题:
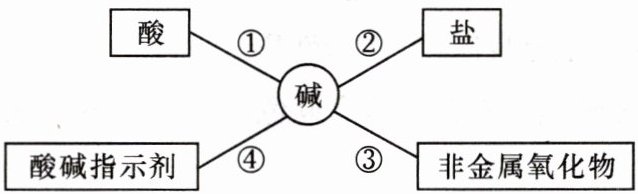
(1) 小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶塞,依据反应③说明$NaOH$必须密封保存,否则在空气中要变质。若该溶液变质,则发生反应的化学方程式为______。
(2) 要检验该氢氧化钠溶液已变质,下列试剂不能达到目的的是______(填字母)。
A. 稀$HCl$
B. 酚酞试液
C. $CaCl_{2}$
D. $Ca(OH)_{2}$
(3) 为了验证反应④,小丽将无色酚酞试液分别滴入$NaOH$溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中能电离出______。
(4) 依据反应②,$KOH$能与下列物质反应的是______(填字母)。
A. $H_{2}SO_{4}$
B. $BaCl_{2}$
C. $CuSO_{4}$
D. $Na_{2}CO_{3}$
发生反应的化学方程式为______。
变式1 如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请你据图回答:

(1) A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是______。
(2) 能同时实现反应①和②的物质可以是______,反应①的实验现象为______。

(1) 小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶塞,依据反应③说明$NaOH$必须密封保存,否则在空气中要变质。若该溶液变质,则发生反应的化学方程式为______。
(2) 要检验该氢氧化钠溶液已变质,下列试剂不能达到目的的是______(填字母)。
A. 稀$HCl$
B. 酚酞试液
C. $CaCl_{2}$
D. $Ca(OH)_{2}$
(3) 为了验证反应④,小丽将无色酚酞试液分别滴入$NaOH$溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中能电离出______。
(4) 依据反应②,$KOH$能与下列物质反应的是______(填字母)。
A. $H_{2}SO_{4}$
B. $BaCl_{2}$
C. $CuSO_{4}$
D. $Na_{2}CO_{3}$
发生反应的化学方程式为______。
变式1 如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请你据图回答:

(1) A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是______。
(2) 能同时实现反应①和②的物质可以是______,反应①的实验现象为______。
答案:
腐蚀性
(1)$2NaOH + CO_{2} = Na_{2}CO_{3} + H_{2}O$
(2)B
(3)$OH^{-}$
(4)C $CuSO_{4} + 2KOH = K_{2}SO_{4} + Cu(OH)_{2}\downarrow$ 变式1
(1)$Cu(OH)_{2}$、$CO_{2}$
(2)$Na_{2}CO_{3}$(碳酸钠) 有气泡(气体)产生
(1)$2NaOH + CO_{2} = Na_{2}CO_{3} + H_{2}O$
(2)B
(3)$OH^{-}$
(4)C $CuSO_{4} + 2KOH = K_{2}SO_{4} + Cu(OH)_{2}\downarrow$ 变式1
(1)$Cu(OH)_{2}$、$CO_{2}$
(2)$Na_{2}CO_{3}$(碳酸钠) 有气泡(气体)产生
例2 某同学利用如图所示装置证明氢氧化钠溶液能与二氧化碳反应(装置气密性良好,实验前$K_{1}$、$K_{2}$均处于关闭状态)。
(1) 打开$K_{1}$,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭$K_{1}$,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为______。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由:______。
(2) 该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开$K_{2}$前A装置需要______;打开$K_{2}$,观察到的现象是______,该过程中多孔玻璃球泡的主要作用是______。
(3) 实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是______。
变式2 某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。实验设计三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器C颈插有两端开口的玻璃导管(伸入瓶内 的一端连有小气球),装置气密性良好。
的一端连有小气球),装置气密性良好。
实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。______
(1) 打开$K_{1}$,将分液漏斗中的溶液全部注入锥形瓶内,立即关闭$K_{1}$,观察到有少量白色浑浊产生。查找原因,该异常现象是因为氢氧化钠饱和溶液中混入了氢氧化钙,产生白色浑浊的一个化学方程式为______。该同学分析后确认,即使所加溶液中氢氧化钙达到饱和,反应后A中仍无氢氧化钙剩余,说明理由:______。

(2) 该同学进一步分析后确定,继续实验仍可证明氢氧化钠溶液能与二氧化碳反应。为利于观察现象,打开$K_{2}$前A装置需要______;打开$K_{2}$,观察到的现象是______,该过程中多孔玻璃球泡的主要作用是______。
(3) 实验后,将A中物质过滤,向滤液中滴加酚酞溶液,变红。对滤液进行无害化处理,需加入的一种试剂是______。
变式2 某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。实验设计三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器C颈插有两端开口的玻璃导管(伸入瓶内
 的一端连有小气球),装置气密性良好。
的一端连有小气球),装置气密性良好。实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。______
答案:
(1)$Ca(OH)_{2} + CO_{2} = CaCO_{3}\downarrow + H_{2}O$或$Na_{2}CO_{3} + Ca(OH)_{2} = CaCO_{3}\downarrow + 2NaOH$ 氢氧化钙的溶解度远小于氢氧化钠,所加溶液中即使氢氧化钙饱和,其含量也远小于其中氢氧化钠的量,溶液中的氢氧化钙既能与二氧化碳反应,又能与生成的碳酸钠反应,故反应后氢氧化钙不会剩余
(2)充分静置 烧杯中的氯化钙溶液倒流进锥形瓶A中,锥形瓶A的上层清液中有大量白色沉淀生成 减缓倒流液体对锥形瓶A中溶液的冲击,防止对A锥形瓶中已沉淀的碳酸钙产生干扰
(3)稀盐酸 变式2 开始氢氧化钠与二氧化碳反应导致瓶内压强变小,气球变大,后来盐酸与碳酸钠反应生成二氧化碳,导致瓶内的压强增大,气球变瘪。
(1)$Ca(OH)_{2} + CO_{2} = CaCO_{3}\downarrow + H_{2}O$或$Na_{2}CO_{3} + Ca(OH)_{2} = CaCO_{3}\downarrow + 2NaOH$ 氢氧化钙的溶解度远小于氢氧化钠,所加溶液中即使氢氧化钙饱和,其含量也远小于其中氢氧化钠的量,溶液中的氢氧化钙既能与二氧化碳反应,又能与生成的碳酸钠反应,故反应后氢氧化钙不会剩余
(2)充分静置 烧杯中的氯化钙溶液倒流进锥形瓶A中,锥形瓶A的上层清液中有大量白色沉淀生成 减缓倒流液体对锥形瓶A中溶液的冲击,防止对A锥形瓶中已沉淀的碳酸钙产生干扰
(3)稀盐酸 变式2 开始氢氧化钠与二氧化碳反应导致瓶内压强变小,气球变大,后来盐酸与碳酸钠反应生成二氧化碳,导致瓶内的压强增大,气球变瘪。
查看更多完整答案,请扫码查看


