第65页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1.某兴趣实验小组用如图所示实验探究 CO₂ 能否与 NaOH 溶液发生反应。实验时,先将浓氢氧化钠溶液挤入盛有 CO₂ 的具支小试管中,振荡;然后将止水夹 K 打开。
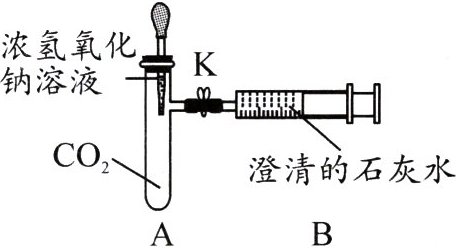
(1)打开止水夹 K 之前,A 中发生反应的化学方程式为______________________
______________________________。
(2)打开止水夹 K 后,注射器 B 中的液体能进入 A 中的原因是______________________
______________________,A 中还可观察到的现象是______________________。
(3)实验结束后,A 中的液体显__________(填“酸性”“碱性”或“中性”)。

(1)打开止水夹 K 之前,A 中发生反应的化学方程式为______________________
______________________________。
(2)打开止水夹 K 后,注射器 B 中的液体能进入 A 中的原因是______________________
______________________,A 中还可观察到的现象是______________________。
(3)实验结束后,A 中的液体显__________(填“酸性”“碱性”或“中性”)。
答案:
$CO_{2}+2NaOH = Na_{2}CO_{3}+H_{2}O$@@$CO_{2}$气体减少,压强减小@@A中液体变浑浊@@碱性
2.(2024·临夏州)化学兴趣小组的同学以中和反应的实验为主题进行探究活动,邀请你一起参与。

【发现问题】
取一定量氢氧化钾溶液于试管中,向其中加入一定量稀硫酸,发现无明显现象,那么稀硫酸和 KOH 溶液是否发生了化学反应?
【分析讨论】
(1)同学们讨论后认为,可以用两种思路探究上述反应是否发生。
思路Ⅰ:验证反应物减少或消失;
思路Ⅱ:验证______________。
(2)甲同学向实验的剩余溶液中(如图 2 所示)滴加酚酞溶液,溶液为______色,结论是稀硫酸和 KOH 溶液发生了化学反应,判断依据是溶液中__________(填离子符号)一定被完全消耗了。
【猜想与假设】
(3)乙同学对剩余溶液的溶质成分作出如下猜想:
猜想一:只有 K₂SO₄;
猜想二:有 K₂SO₄ 和 H₂SO₄;
猜想三:有 K₂SO₄ 和 KOH。
根据甲同学的实验,猜想______一定错误。
【进行实验】
(4)验证猜想,同学们选用 Fe₂O₃ 粉末、BaCl₂ 溶液,进行如下探究并完善表格。
|实验方案|实验操作|实验现象|实验结论|
|----|----|----|----|
|方案一|| |猜想二正确|
|方案二||产生白色沉淀|猜想二正确|
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(5)分析上述反应,说明稀硫酸能与金属氧化物、某些碱和某些______反应。
(6)丙同学针对上述方案提出疑问,认为方案二是不合理的,理由:______________________
______________________(用化学方程式表示)。
(7)丁同学认为方案一中的 Fe₂O₃ 粉末可以用铁粉代替,也能得到同样的实验结论,其化学方程式为______________________。

【发现问题】
取一定量氢氧化钾溶液于试管中,向其中加入一定量稀硫酸,发现无明显现象,那么稀硫酸和 KOH 溶液是否发生了化学反应?
【分析讨论】
(1)同学们讨论后认为,可以用两种思路探究上述反应是否发生。
思路Ⅰ:验证反应物减少或消失;
思路Ⅱ:验证______________。
(2)甲同学向实验的剩余溶液中(如图 2 所示)滴加酚酞溶液,溶液为______色,结论是稀硫酸和 KOH 溶液发生了化学反应,判断依据是溶液中__________(填离子符号)一定被完全消耗了。
【猜想与假设】
(3)乙同学对剩余溶液的溶质成分作出如下猜想:
猜想一:只有 K₂SO₄;
猜想二:有 K₂SO₄ 和 H₂SO₄;
猜想三:有 K₂SO₄ 和 KOH。
根据甲同学的实验,猜想______一定错误。
【进行实验】
(4)验证猜想,同学们选用 Fe₂O₃ 粉末、BaCl₂ 溶液,进行如下探究并完善表格。
|实验方案|实验操作|实验现象|实验结论|
|----|----|----|----|
|方案一|| |猜想二正确|
|方案二||产生白色沉淀|猜想二正确|
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(5)分析上述反应,说明稀硫酸能与金属氧化物、某些碱和某些______反应。
(6)丙同学针对上述方案提出疑问,认为方案二是不合理的,理由:______________________
______________________(用化学方程式表示)。
(7)丁同学认为方案一中的 Fe₂O₃ 粉末可以用铁粉代替,也能得到同样的实验结论,其化学方程式为______________________。
答案:
有新物质生成@@无@@$OH^{-}$@@三@@固体粉末逐渐溶解,溶液由无色变黄色@@盐@@$K_{2}SO_{4}+BaCl_{2}=BaSO_{4}\downarrow +2KCl$@@$Fe+H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$
查看更多完整答案,请扫码查看


