第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
1. 金刚石、石墨、${C_{60}}$


答案:
1.最硬 导电性能
2. 木炭、活性炭:疏松多孔,都具有
吸附
能力,如木炭用来吸附工业产品里的色素和消除异味,活性炭用在防毒面具中吸附毒气,吸附过程发生的是物理
变化。
答案:
2.吸附 物理
3. 碳单质的化学性质
(1)稳定性:碳的单质在常温下化学性质
(2)可燃性
完全燃烧(氧气充足):${C + O_{2}\xlongequal{点燃}}$
不完全燃烧(氧气不充足):
(3)与某些氧化物反应
①与氧化铜反应
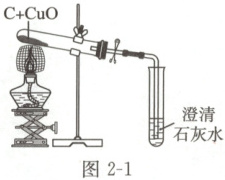
a. 实验装置:如图,装置中弹簧夹的作用是
b. 实验现象:黑色固体逐渐变成
c. 化学方程式:
②与二氧化碳反应:${CO_{2} + C\xlongequal{高温}}$
③与氧化铁反应:
【注意】
在酒精灯上加网罩是为了使火焰集中并提高温度。
(1)稳定性:碳的单质在常温下化学性质
不活泼
。如用墨书写或绘制的字画能够保存很长时间而不变色。(2)可燃性
完全燃烧(氧气充足):${C + O_{2}\xlongequal{点燃}}$
CO₂
。不完全燃烧(氧气不充足):
2
${C + O_{2}\xlongequal{点燃}}$2CO
。(3)与某些氧化物反应
①与氧化铜反应
a. 实验装置:如图,装置中弹簧夹的作用是
防止空气进入试管使Cu再次氧化
。b. 实验现象:黑色固体逐渐变成
红色
,澄清石灰水变浑浊
。c. 化学方程式:
2
${CuO + C\xlongequal{高温}}$2Cu+CO₂↑
。②与二氧化碳反应:${CO_{2} + C\xlongequal{高温}}$
2CO
。③与氧化铁反应:
$3C+2Fe₂O₃\stackrel{高温}{=\!=\!=}4Fe+3CO₂↑$
【注意】
在酒精灯上加网罩是为了使火焰集中并提高温度。

答案:
3.
(1)不活泼
(2)CO₂ 2 2CO
(3)①a.防止空气进入试管使Cu再次氧化
b.红色 浑浊
c.2 2Cu+CO₂↑
$②2CO ③3C+2Fe₂O₃\stackrel{高温}{=\!=\!=}4Fe+3CO₂↑$
(1)不活泼
(2)CO₂ 2 2CO
(3)①a.防止空气进入试管使Cu再次氧化
b.红色 浑浊
c.2 2Cu+CO₂↑
$②2CO ③3C+2Fe₂O₃\stackrel{高温}{=\!=\!=}4Fe+3CO₂↑$
1. 物理性质
无
色、无臭的气体,能
溶于水,密度比空气的大
,加压降温的情况下,二氧化碳气体会变成固体,固态二氧化碳叫“干冰
”。干冰能吸热升华变成二氧化碳气体。
答案:
1.无 能 大 干冰
2. 化学性质
(1)一般情况下,既不能燃烧也不支持燃烧。
(2)与水反应:化学方程式为
(${H_{2}CO_{3}}$能使紫色石蕊溶液变成红色;碳酸很不稳定,容易分解,反应的化学方程式为
(3)与碱反应
①与澄清石灰水反应的现象:
化学方程式:
应用:实验室常利用该反应原理检验二氧化碳。
②与氢氧化钠反应的化学方程式:
应用:实验室常利用该反应原理吸收或除去二氧化碳。
(4)与碳反应的化学方程式:${C + CO_{2}\xlongequal{高温}}$
(5)参与光合作用。
(1)一般情况下,既不能燃烧也不支持燃烧。
(2)与水反应:化学方程式为
CO₂+H₂O=\!=\!=H₂CO₃
(${H_{2}CO_{3}}$能使紫色石蕊溶液变成红色;碳酸很不稳定,容易分解,反应的化学方程式为
H₂CO₃=\!=\!=CO₂↑+H₂O
)。(3)与碱反应
①与澄清石灰水反应的现象:
澄清石灰水变浑浊
。化学方程式:
CO₂+Ca(OH)₂=\!=\!=CaCO₃↓+H₂O
。应用:实验室常利用该反应原理检验二氧化碳。
②与氢氧化钠反应的化学方程式:
CO₂+2NaOH=\!=\!=Na₂CO₃+H₂O
。应用:实验室常利用该反应原理吸收或除去二氧化碳。
(4)与碳反应的化学方程式:${C + CO_{2}\xlongequal{高温}}$
2CO
。(5)参与光合作用。
答案:
2.
(2)CO₂+H₂O=\!=\!=H₂CO₃
H₂CO₃=\!=\!=CO₂↑+H₂O
(3)①澄清石灰水变浑浊
CO₂+Ca(OH)₂=\!=\!=CaCO₃↓+H₂O
②CO₂+2NaOH=\!=\!=Na₂CO₃+H₂O
(2)CO₂+H₂O=\!=\!=H₂CO₃
H₂CO₃=\!=\!=CO₂↑+H₂O
(3)①澄清石灰水变浑浊
CO₂+Ca(OH)₂=\!=\!=CaCO₃↓+H₂O
②CO₂+2NaOH=\!=\!=Na₂CO₃+H₂O
4. 工业制法
高温煅烧石灰石:
高温煅烧石灰石:
$CaCO₃\stackrel{高温}{=\!=\!=}CaO+CO₂↑$
。
答案:
4.CaCO₃===高温CaO+CO₂↑
4.CaCO₃===高温CaO+CO₂↑
查看更多完整答案,请扫码查看


