2025年新中考集训测试评估卷九年级化学全一册鲁教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新中考集训测试评估卷九年级化学全一册鲁教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第83页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
9. 某同学为了探究相关金属的化学性质,做了下列实验:
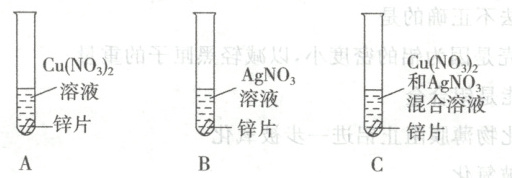
(1)A 试管中实验现象是
(2)只通过 A 和 B 实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是
A. $Cu$、$Ag$、稀盐酸
B. $Cu$、$AgNO_3$ 溶液
(3)实验 C 中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想,其中明显不合理的是
A. $Zn$、$Cu$、$Ag$
B. $Zn$、$Cu$
C. $Cu$、$Ag$
D. $Ag$

(1)A 试管中实验现象是
锌片上附着一层红色的物质,溶液由蓝色变为无色
。(2)只通过 A 和 B 实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是
B
(填字母,下同)。A. $Cu$、$Ag$、稀盐酸
B. $Cu$、$AgNO_3$ 溶液
(3)实验 C 中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想,其中明显不合理的是
B
。A. $Zn$、$Cu$、$Ag$
B. $Zn$、$Cu$
C. $Cu$、$Ag$
D. $Ag$
答案:
9.
(1)锌片上附着一层红色的物质,溶液由蓝色变为无色
(2)B
(3)B
解析:
(1)锌的活动性比铜的强,故锌能和硝酸铜反应,生成铜和硝酸锌,故现象为锌片上附着一层红色的物质,溶液由蓝色变为无色。
(2)通过实验A可知锌的活动性比铜强,通过实验B可知锌的活动性比铁强,还需要证明铜和银的活动性强弱。Cu、Ag、稀盐酸之间不能反应,故A无法证明;Cu插入AgNO₃溶液中反应,可以证明铜的活动性比银强,故B可以达到实验目的。
(3)锌片放入硝酸铜和硝酸银的溶液中,先进行的反应是锌和硝酸银的反应,硝酸银反应结束,再进行锌和硝酸铜的反应,若锌是过量的,得到的金属为锌、银、铜,A项符合题意;若锌和硝酸铜、硝酸银恰好反应,得到的金属是铜和银,C项符合题意;若锌是少量的,得到的金属为银,D项符合题意;在此反应的过程中一定有银析出,B项不符合题意。
(1)锌片上附着一层红色的物质,溶液由蓝色变为无色
(2)B
(3)B
解析:
(1)锌的活动性比铜的强,故锌能和硝酸铜反应,生成铜和硝酸锌,故现象为锌片上附着一层红色的物质,溶液由蓝色变为无色。
(2)通过实验A可知锌的活动性比铜强,通过实验B可知锌的活动性比铁强,还需要证明铜和银的活动性强弱。Cu、Ag、稀盐酸之间不能反应,故A无法证明;Cu插入AgNO₃溶液中反应,可以证明铜的活动性比银强,故B可以达到实验目的。
(3)锌片放入硝酸铜和硝酸银的溶液中,先进行的反应是锌和硝酸银的反应,硝酸银反应结束,再进行锌和硝酸铜的反应,若锌是过量的,得到的金属为锌、银、铜,A项符合题意;若锌和硝酸铜、硝酸银恰好反应,得到的金属是铜和银,C项符合题意;若锌是少量的,得到的金属为银,D项符合题意;在此反应的过程中一定有银析出,B项不符合题意。
10. 白铜是铜、镍(Ni)合金,某学习小组同学欲利用废弃的白铜回收铜、镍两种金属。
(1)先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌
(2)接下来,同学们设计了如下实验流程回收铜和镍。

上图中,固体 A 是
(3)要验证 Ni、Zn、Cu 的金属活动性顺序,用下列各组试剂进行实验,不能达到目的的是
A. Ni、Zn、Cu、稀盐酸
B. Ni、Cu、$ZnSO_4$ 溶液
C. Zn、Cu、$NiSO_4$ 溶液
D. Ni、$ZnSO_4$ 溶液、$CuSO_4$ 溶液
(1)先向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,观察到都有气泡产生,且锌粉与稀硫酸反应更剧烈,镍粉与稀硫酸反应后的溶液为绿色,说明镍的金属活动性比锌
弱
(填“强”或“弱”)。查阅资料可知,镍与稀硫酸反应的化学方程式为 $Ni + H_2SO_4 = NiSO_4 + H_2 \uparrow$。(2)接下来,同学们设计了如下实验流程回收铜和镍。

上图中,固体 A 是
Cu
,②中反应的化学方程式是Zn+H₂SO₄=ZnSO₄+H₂↑(或Zn+NiSO₄=Ni+ZnSO₄)
(写一个)。(3)要验证 Ni、Zn、Cu 的金属活动性顺序,用下列各组试剂进行实验,不能达到目的的是
B
(填字母)。A. Ni、Zn、Cu、稀盐酸
B. Ni、Cu、$ZnSO_4$ 溶液
C. Zn、Cu、$NiSO_4$ 溶液
D. Ni、$ZnSO_4$ 溶液、$CuSO_4$ 溶液
答案:
10.
(1)弱
(2)Cu Zn+H₂SO₄=ZnSO₄+H₂↑(或Zn+NiSO₄=Ni+ZnSO₄)
(3)B
解析:
(1)分析实验现象可知,向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,都有气泡产生,且锌粉与稀硫酸反应更剧烈,则两种金属的活动性强弱是Zn>Ni,即镍的金属活动性比锌弱。
(2)根据金属活动性顺序,铜排在氢的后面,与酸不反应,因此固体A为铜;Ni+H₂SO₄=NiSO₄+H₂↑,硫酸过量,因此溶液B中含有硫酸和硫酸镍,锌与硫酸反应生成硫酸锌和氢气,化学方程式为Zn+H₂SO₄=ZnSO₄+H₂↑,锌比镍活泼,可以将镍置换出来,锌与硫酸镍反应生成硫酸锌和镍,化学方程式为Zn+NiSO₄=Ni+ZnSO₄。
(3)锌和稀盐酸反应速率比镍快,说明锌比镍活泼,铜不能和稀盐酸反应,说明活动性锌>镍>铜,A项能够达到实验目的;镍、铜都不能和硫酸锌反应,说明锌最活泼,但不能比较镍和铜的活动性,B项不能达到实验目的;锌能和硫酸镍反应,说明锌比镍活泼,铜不能和硫酸镍反应,说明活动性锌>镍>铜,C项能够达到实验目的。
(1)弱
(2)Cu Zn+H₂SO₄=ZnSO₄+H₂↑(或Zn+NiSO₄=Ni+ZnSO₄)
(3)B
解析:
(1)分析实验现象可知,向盛有等量镍粉和锌粉的两支试管中分别加入溶质质量分数相同的稀硫酸,都有气泡产生,且锌粉与稀硫酸反应更剧烈,则两种金属的活动性强弱是Zn>Ni,即镍的金属活动性比锌弱。
(2)根据金属活动性顺序,铜排在氢的后面,与酸不反应,因此固体A为铜;Ni+H₂SO₄=NiSO₄+H₂↑,硫酸过量,因此溶液B中含有硫酸和硫酸镍,锌与硫酸反应生成硫酸锌和氢气,化学方程式为Zn+H₂SO₄=ZnSO₄+H₂↑,锌比镍活泼,可以将镍置换出来,锌与硫酸镍反应生成硫酸锌和镍,化学方程式为Zn+NiSO₄=Ni+ZnSO₄。
(3)锌和稀盐酸反应速率比镍快,说明锌比镍活泼,铜不能和稀盐酸反应,说明活动性锌>镍>铜,A项能够达到实验目的;镍、铜都不能和硫酸锌反应,说明锌最活泼,但不能比较镍和铜的活动性,B项不能达到实验目的;锌能和硫酸镍反应,说明锌比镍活泼,铜不能和硫酸镍反应,说明活动性锌>镍>铜,C项能够达到实验目的。
1. 铜绿是铜生锈后的产物,其成分是 $Cu_2(OH)_2CO_3$,下列空气中的物质与铜生锈没有直接关系的是(
A.氮气
B.氧气
C.水蒸气
D.二氧化碳
A
)A.氮气
B.氧气
C.水蒸气
D.二氧化碳
答案:
1.A 解析:由质量守恒定律可知,化学反应前后元素的种类不变。Cu₂(OH)₂CO₃中不含氮元素,因此氮气与铜生锈没有直接关系。
查看更多完整答案,请扫码查看


