2025年新中考集训测试评估卷九年级化学全一册鲁教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新中考集训测试评估卷九年级化学全一册鲁教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第71页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
3. $NaOH$ 是常见的碱,其在不同温度下的溶解度如下表所示。下列有关说法正确的是(

A.$20^{\circ}C$ 时,$200g$ 水中能溶解 $218g$ $NaOH$
B.$NaOH$ 的溶解度随温度的升高而减小
C.将 $40^{\circ}C$ 的 $NaOH$ 饱和溶液升温至 $60^{\circ}C$,其质量分数增大
D.将 $80^{\circ}C$ 的 $NaOH$ 饱和溶液降温至 $20^{\circ}C$,析出晶体 $205g$
A
)
A.$20^{\circ}C$ 时,$200g$ 水中能溶解 $218g$ $NaOH$
B.$NaOH$ 的溶解度随温度的升高而减小
C.将 $40^{\circ}C$ 的 $NaOH$ 饱和溶液升温至 $60^{\circ}C$,其质量分数增大
D.将 $80^{\circ}C$ 的 $NaOH$ 饱和溶液降温至 $20^{\circ}C$,析出晶体 $205g$
答案:
3.A 解析:20℃时,氢氧化钠的溶解度为109g,该温度下,200g 水中能溶解218g氢氧化钠,A项正确;由题表可知,氢氧化钠的溶解度随温度的升高而增加,B项错误;将40℃的NaOH饱和溶液升温至60℃,溶解度增加,变为不饱和溶液,溶质和溶剂的质量不变,故溶质质量分数不变,C项错误;将80℃的NaOH饱和溶液降温至20℃,氢氧化钠的溶解度减小,有溶质析出,但是溶液的质量未知,析出晶体的质量无法确定,D项错误。
4. 如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法正确的是(
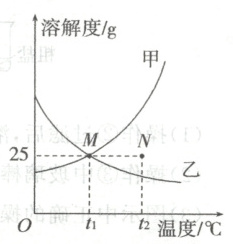
A.甲的溶解度比乙的溶解度大
B.在 $t_1^{\circ}C$ 时,甲溶液和乙溶液的溶质质量分数相等
C.在 $t_1^{\circ}C$ 时,$100g$ 甲物质的饱和溶液中溶质的质量是 $25g$
D.在 $t_2^{\circ}C$ 时,欲将 $N$ 点的甲物质溶液变为饱和溶液可采用恒温蒸发水的方法
D
)
A.甲的溶解度比乙的溶解度大
B.在 $t_1^{\circ}C$ 时,甲溶液和乙溶液的溶质质量分数相等
C.在 $t_1^{\circ}C$ 时,$100g$ 甲物质的饱和溶液中溶质的质量是 $25g$
D.在 $t_2^{\circ}C$ 时,欲将 $N$ 点的甲物质溶液变为饱和溶液可采用恒温蒸发水的方法
答案:
4.D 解析:在比较物质的溶解度时,需要指明温度,温度不确定,溶解度也不能确定,A项错误;在t₁℃时,甲溶液和乙溶液的状态不能确定,所以溶液中的溶质质量分数也不能确定,B 项错误;在t₁℃时,甲物质的溶解度是25g,所以125g甲物质的饱和溶液中溶质的质量是25g,C项错误;在t₂℃时,欲将N点的甲物质溶液变为饱和溶液可采用恒温蒸发水的方法,
D项正确。
D项正确。
5. $t^{\circ}C$ 时,向一支盛有 $0.15g$ 熟石灰的烧杯中加入 $50g$ 水,充分振荡后静置,烧杯底部仍有未溶解的白色固体。下列相关叙述正确的是(
A.升高温度上层清液变为不饱和溶液
B.$t^{\circ}C$ 时,熟石灰的溶解度为 $0.3g$
C.烧杯中溶液的质量小于 $50.15g$
D.上层清液中溶质质量分数大于 $0.3\%$
C
)A.升高温度上层清液变为不饱和溶液
B.$t^{\circ}C$ 时,熟石灰的溶解度为 $0.3g$
C.烧杯中溶液的质量小于 $50.15g$
D.上层清液中溶质质量分数大于 $0.3\%$
答案:
5.C 解析:烧杯底部有白色固体,故得到的溶液为饱和溶液,升高温度熟石灰的溶解度降低,溶液仍为饱和,故A错误;由于0.15g熟石灰没有完全溶解在50g水中,故烧杯中溶液的质量小于50.15g,由此可以确定,t℃时,熟石灰的溶解度小于0.3g,故B错误,C正确;若0.15g熟石灰全部溶于50g水中,上层清液中溶质质量分数小于0.3%,且没有完全溶解,则溶质质量分数小于0.3%,故D错误。
6. 硝酸钾的溶解度曲线如下图所示,回答下列问题。

(1) 图中 $P$ 点所表示的 $KNO_3$ 溶液
(2) 将 $KNO_3$ 的饱和溶液变为不饱和溶液,可采用的方法有
(3) $20^{\circ}C$ 时,将 $20g$ $KNO_3$ 固体加入 $50g$ 水中,充分溶解,所得溶液的质量为

(1) 图中 $P$ 点所表示的 $KNO_3$ 溶液
不饱和
(填“饱和”或“不饱和”)。(2) 将 $KNO_3$ 的饱和溶液变为不饱和溶液,可采用的方法有
加水(或升高温度或加入不饱和的硝酸钾溶液)
(写一种即可)。(3) $20^{\circ}C$ 时,将 $20g$ $KNO_3$ 固体加入 $50g$ 水中,充分溶解,所得溶液的质量为
65.8
g。
答案:
6.
(1)不饱和
(2)加水(或升高温度或加入不饱和的硝酸钾溶液)
(3)65.8
解析:
(1)P点在KNO₃溶解度曲线的下方,属于KNO₃的不饱和溶液。
(2)从题图可知,硝酸钾的溶解度随温度的升高而升高,因此将KNO₃的饱和溶液变为不饱和溶液,可采用的方法有加水或升高温度或加入不饱和的硝酸钾溶液。
(3)20℃时硝酸钾的溶解度为31.6g,因此50g水中最多溶解15.8g,20℃时,将20gKNO₃固体加入50g水中,充分溶解,所得溶液的质量为50g + 15.8g = 65.8g。
(1)不饱和
(2)加水(或升高温度或加入不饱和的硝酸钾溶液)
(3)65.8
解析:
(1)P点在KNO₃溶解度曲线的下方,属于KNO₃的不饱和溶液。
(2)从题图可知,硝酸钾的溶解度随温度的升高而升高,因此将KNO₃的饱和溶液变为不饱和溶液,可采用的方法有加水或升高温度或加入不饱和的硝酸钾溶液。
(3)20℃时硝酸钾的溶解度为31.6g,因此50g水中最多溶解15.8g,20℃时,将20gKNO₃固体加入50g水中,充分溶解,所得溶液的质量为50g + 15.8g = 65.8g。
7. (2024·临沂模拟)如图所示是甲、乙、丙三种物质的溶解度曲线,在 $20^{\circ}C$ 时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液中分别加入等质量的相应固体物质,再将温度升高到 $40^{\circ}C$,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
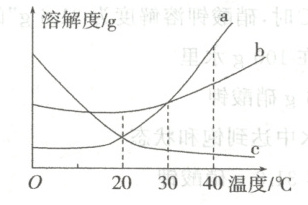
(1) 写出甲、乙、丙三种物质对应的溶解度曲线:
(2) $40^{\circ}C$ 时,等质
(3) 当温度在 $20\sim30^{\circ}C$ 时,三种物质的溶解度由小到大的顺序是
(4) $40^{\circ}C$ 时,a 溶液中溶质质量分数

(1) 写出甲、乙、丙三种物质对应的溶解度曲线:
a、c、b
(用“a”“b”“c”填空,下同)。(2) $40^{\circ}C$ 时,等质
量
饱
和
溶液中含水最少的是a
物质。(3) 当温度在 $20\sim30^{\circ}C$ 时,三种物质的溶解度由小到大的顺序是
c<a<b
。(4) $40^{\circ}C$ 时,a 溶液中溶质质量分数
不一定
(填“一定”或“不一定”)大于 b 溶液中溶质质量分数。
答案:
7.
(1)a、c、b
(2)a
(3)c<a<b
(4)不一定
解析:
(1)通过分析溶解度曲线可知,温度由20℃升高到40℃,a、b的溶解度增大,c的溶解度减小,故向20℃时等质量的三种物质的饱和溶液中,加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,说明甲、丙两物质的溶解度随着温度的升高而增大,且甲的溶解度受温度的影响最大;故乙物质的溶解度应随着温度的升高而减小,所以甲、乙、丙三种物质对应的溶解度曲线分别为a、c、b。
(2)40℃时,a物质的溶解度最大,故等质量饱和溶液中含水最少的是a。
(3)当温度在20~30℃时,三种物质的溶解度由小到大的顺序是c<a<b。
(4)未指明溶液是否饱和,无法比较两溶液中溶质的质量分数,则40℃时,a溶液中溶质质量分数不一定大于b溶液中溶质质量分数。
(1)a、c、b
(2)a
(3)c<a<b
(4)不一定
解析:
(1)通过分析溶解度曲线可知,温度由20℃升高到40℃,a、b的溶解度增大,c的溶解度减小,故向20℃时等质量的三种物质的饱和溶液中,加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,说明甲、丙两物质的溶解度随着温度的升高而增大,且甲的溶解度受温度的影响最大;故乙物质的溶解度应随着温度的升高而减小,所以甲、乙、丙三种物质对应的溶解度曲线分别为a、c、b。
(2)40℃时,a物质的溶解度最大,故等质量饱和溶液中含水最少的是a。
(3)当温度在20~30℃时,三种物质的溶解度由小到大的顺序是c<a<b。
(4)未指明溶液是否饱和,无法比较两溶液中溶质的质量分数,则40℃时,a溶液中溶质质量分数不一定大于b溶液中溶质质量分数。
查看更多完整答案,请扫码查看


